
『2025年改訂版 心不全診療ガイドライン』における左室駆出率別分類と治療アルゴリズム
サイトへ公開:2025年07月30日 (水)
クイックリンク
『2025年改訂版 心不全診療ガイドライン』では、心不全のステージ分類、左室駆出率(LVEF)での分類、治療アルゴリズム等が更新されました。エビデンスとともに紹介します。

『2025年改訂版 心不全診療ガイドライン』のポイント
心不全診療においては、生命予後の改善に加え、生活の質(QOL)の維持や向上が求められます。
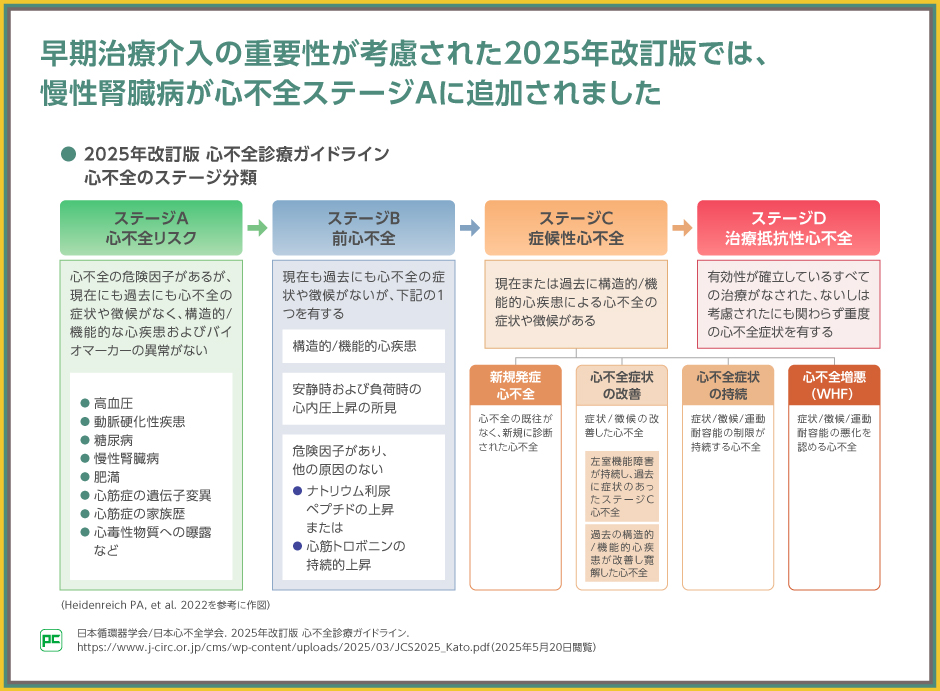
『2025年改訂版 心不全診療ガイドライン』では、心不全のステージ分類が更新されました。心不全への進展防止や早期に治療介入の重要性が考慮された新しいステージ分類では、ステージAに心不全の危険因子として慢性腎臓病(CKD)が追加され、疾患管理が重要であることが示されました。
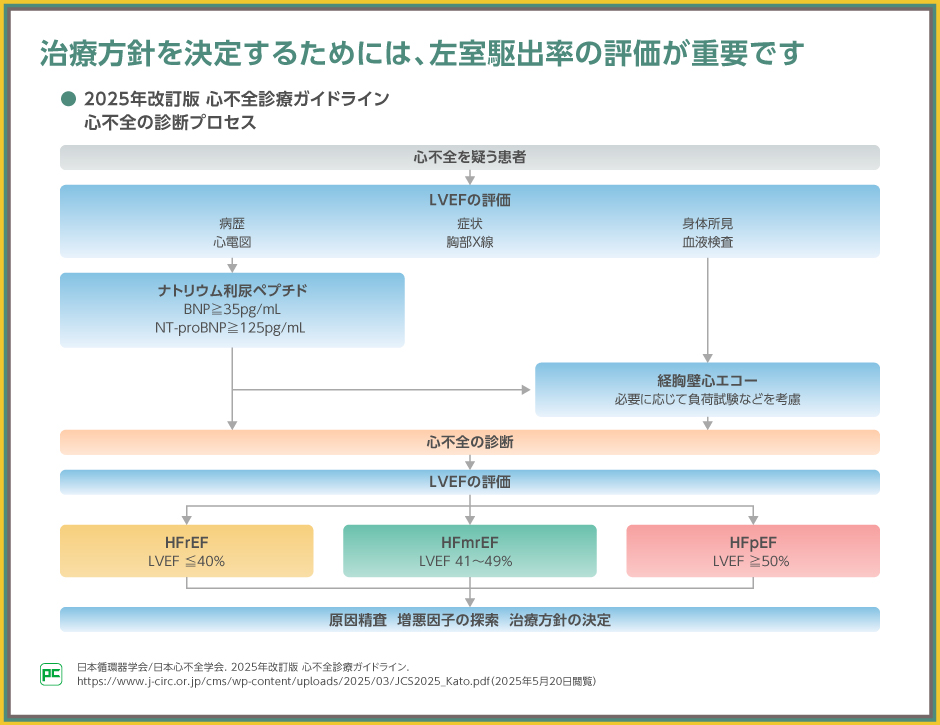
心不全の診断プロセスにおいては、次の2点が大きく更新されました。
①BNP/NT-proBNPのカットオフ値の更新
日本心不全学会が2023年に発表した「BNP/NT-proBNP を用いた心不全診断や循環器専門医への紹介基準のカットオフ値」を受け、心不全を疑うカットオフ値が、BNP≧100pg/mLからBNP≧35pg/mLに、NT-proBNP≧400pg/mLからNT-proBNP≧125pg/mLに変更されました。
②左室駆出率(LVEF)の評価の追加
近年、LVEF別の臨床試験によるエビデンスが構築されたことを受け、LVEF別の分類によって、生命予後を改善させる治療へ反応する患者群を区別できることが示されました。その結果、診断プロセスにおいてもLVEFの評価が追加され、LVEF別に治療方針を決定することが推奨されました。

LVEFによる分類は、初回評価時のLVEFに加え、LVEFの経時変化を考慮し、以下の4つにまとめられました。
2021年アップデート版では、初回評価時の3つの分類に加え、経時的変化による3つの分類が記載されていましたが、2025年改訂版では、経時的変化による分類が治療方針の決定に必要な1つに絞られました。
①HFrEF(LVEF≦40%)
LVEFの低下した心不全とされ、初回評価時にLVEFが低下している患者さんに加え、初回評価時のLVEFが保たれていても経時的に低下し、LVEF≦40%となった患者さんもHFrEFに分類されます。
②HFmrEF(LVEF 41~49%)
LVEFの経度低下した心不全とされ、HFrEFまたはHFpEFのいずれかに明確に分類することが難しいとされています。
③HFpEF(LVEF≧50%)
LVEFが保たれた心不全とされ、近年、高齢化などの影響を受け、増加している病態です。
④HFimpEF(Heart Failure with improved Ejection Fraction)
経時的変化によりLVEFの改善した心不全で、初回評価時はHFrEFと診断された患者さんのLVEFが10%以上増加し、LVEF>40%となった場合と定義されています。LVEF疾患の根治や投薬が不要となることを意味しているわけではないため、継続的な治療が必要です。
なお、LVEFが初回評価時から経時的に変化したがHFimpEFに該当しない場合は、最新のLVEFを用いて①~③に分類します。
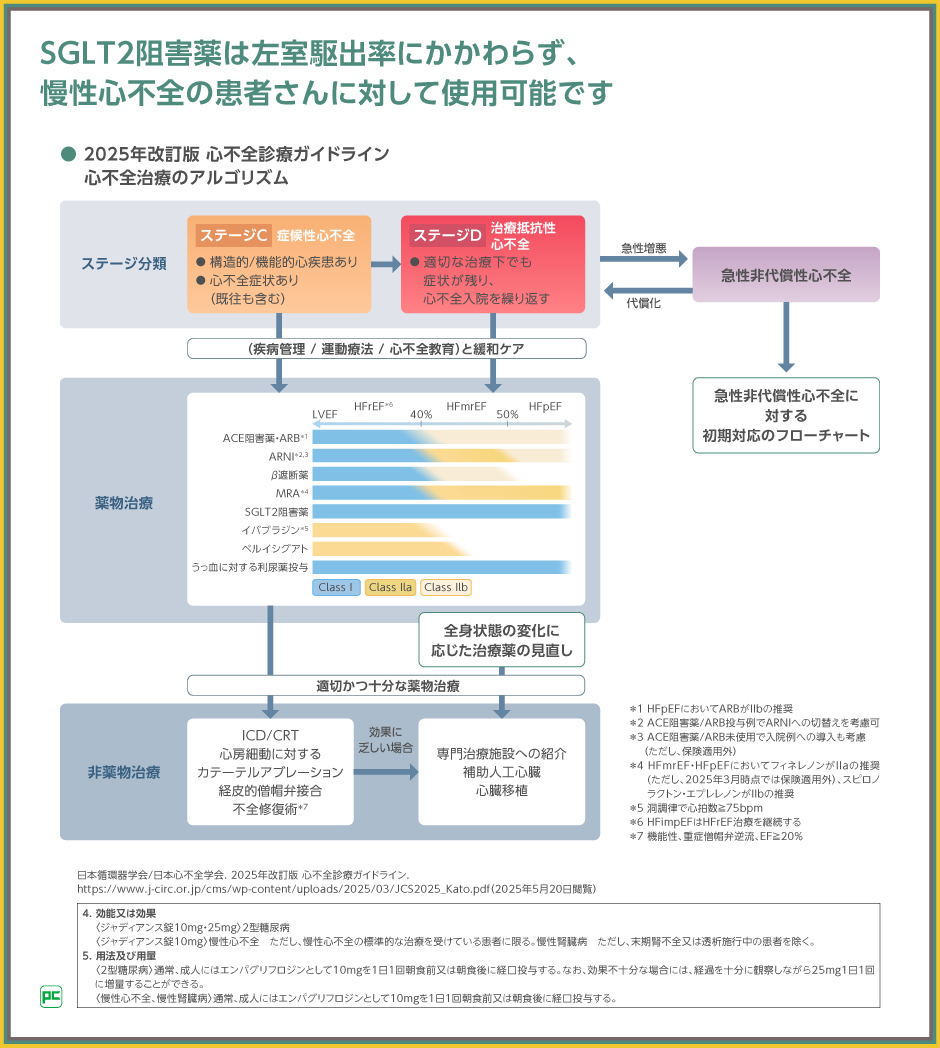
2025年改訂版では、心不全治療のアルゴリズムも更新されました。
新しいアルゴリズムでは、LVEFがグラデーションで示され、従来版では記載されていなかったHFmrEFの治療方針についても示されました。
HFpEFの治療に関しては、従来版ではうっ血に対する利尿薬の使用と併存症に対する治療が推奨されているだけでした1)。しかし、今回は、症候性のHFpEFに対する心血管死または心不全入院の抑制を目的としたSGLT2阻害薬(エンパグリフロジン、ダパグリフロジン)の投与が推奨クラスⅠ、エビデンスAとされました2)。
また、HFrEFに対するGDMT(診療ガイドラインに基づいた標準治療)は、基本となる4種類の薬剤(ACE阻害薬・ARB・ARNI、β遮断薬、MRA、SGLT2阻害薬)を中心に、必要に応じて初期用量(低用量)で開始することです3)。糖尿病の有無にかかわらず、症候性のHFrEFに対するSGLT2阻害薬(エンパグリフロジン、ダパグリフロジン)の投与は、推奨クラスⅠ、エビデンスレベルAとされました4)。
なお、HFimpEFに対しては、最新のLVEFにかかわらず、基本的に、HFrEFの治療を継続します。
1) 日本循環器学会/日本心不全学会. 2025年改訂版 心不全診療ガイドライン. p74.
2) 日本循環器学会/日本心不全学会. 2025年改訂版 心不全診療ガイドライン. p77.
3) 日本循環器学会/日本心不全学会. 2025年改訂版 心不全診療ガイドライン. p63.
4) 日本循環器学会/日本心不全学会. 2025年改訂版 心不全診療ガイドライン. p73.
https://www.j-circ.or.jp/cms/wp-content/uploads/2025/03/JCS2025_Kato.pdf(2025年5月20日閲覧)
腎機能が低下するほど、心血管死のリスクが上昇します
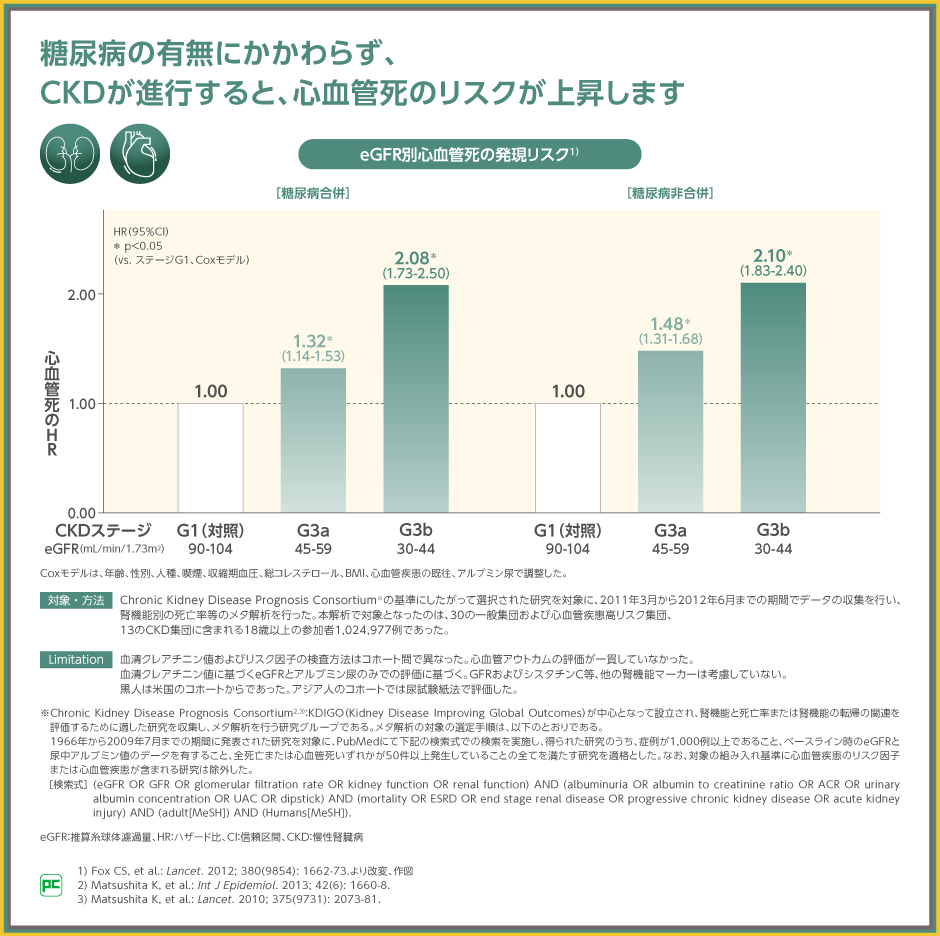
2025年改訂版においてCKDが心不全リスクのステージAに追加されたように、腎機能の低下は、心血管イベントリスクにつながることが疫学データでも示されています。
30の一般集団または心血管疾患高リスク集団、13のCKD集団に含まれた合計100万例以上を対象としたメタアナリシスでは、eGFR 60mL/min/1.73m2未満の場合、糖尿病の有無にかかわらず、eGFR 90mL/min/1.73m2以上104mL/min/1.73m2以下の腎機能が低下していない例よりも心血管死の発現リスクが高いことが報告されました(p<0.05、Coxモデル)。
心血管イベントの発現を抑制するためにも、腎機能低下の抑制を考慮した治療を行う必要があります。

また、心不全の患者さんを対象として、LVEF別と合併症別に予後を検討した疫学調査では、全死亡または心不全による入院のハザード比が、CKDを併発したHFpEFで2.54、CKDを併発したHFrEFで1.43と報告されました。
心不全治療のアルゴリズムが更新されたことから、HFpEFの予後改善のためには、最新のガイドラインを踏まえた適切な心不全治療およびCKD治療が求められます。
ジャディアンスの慢性心不全※1に対するエビデンス
EMPEROR-Reduced試験/EMPEROR-Preserved試験
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。

ここから、慢性心不全に対する有効性を検討したEMPEROR-Reduced試験とEMPEROR-Preserved試験を紹介します。
HFrEFを対象としたEMPEROR-Reduced試験では、ジャディアンス10mgを1日1回経口投与した時の有効性および安全性のプラセボ群との比較検討を、全体集団解析に加え、CKD合併とCKD非合併に分けた事前規定されたサブグループ解析で行いました。
なお、CKD合併の定義は、eGFR<60mL/min/1.73m2または尿中アルブミン/クレアチニン比(UACR)>300mg/gとしました。

LVEF>40%の慢性心不全患者(HFpEF)を対象としたEMPEROR-Preserved試験でも、ジャディアンス10mgを1日1回経口投与した時の有効性および安全性のプラセボ群と比較検討を、全体集団解析に加え、CKD合併とCKD非合併に分けた事前規定されたサブグループ解析で行いました。
なお、CKD合併の定義はEMPEROR-Reduced試験同様、eGFR<60mL/min/1.73m2またはUACR>300mg/gとしました。
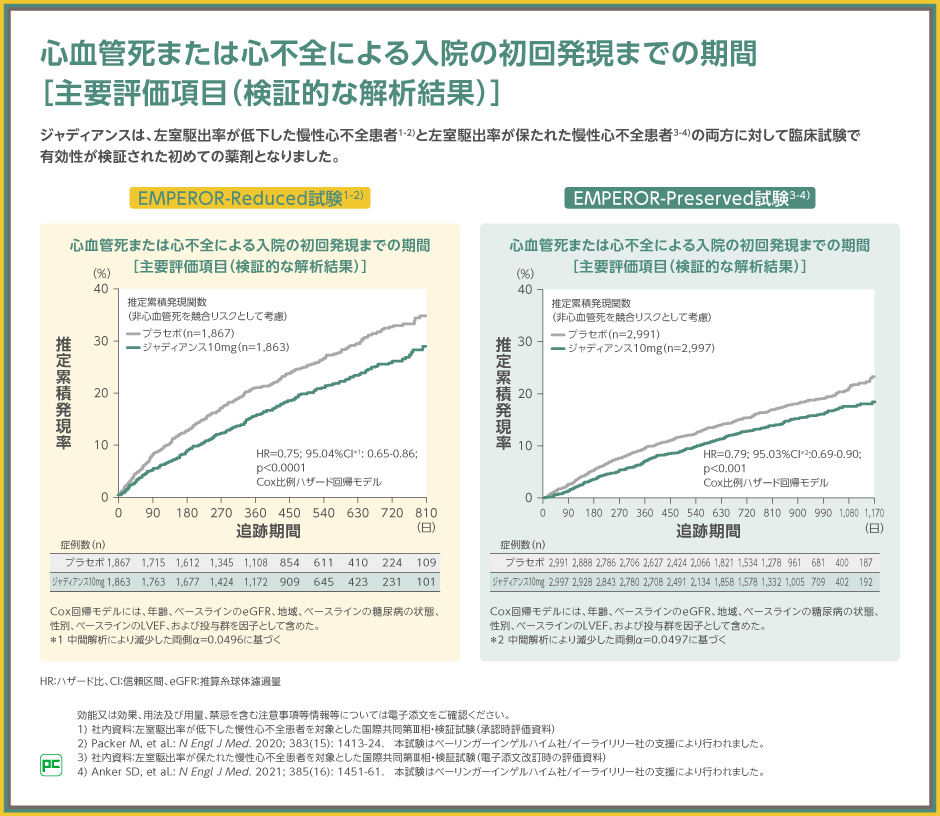
EMPEROR-Reduced試験の全体集団における、心血管死または心不全による入院の初回発現までの期間のプラセボ群に対するジャディアンス10mg群のハザード比は0.75(95.04%CI:0.65~0.86)、p<0.0001(Cox比例ハザード回帰モデル)であり、ジャディアンス10mg群の優越性が検証されました。
また、EMPEROR-Preserved試験の全体集団における、心血管死または心不全による入院の初回発現までの期間のプラセボ群に対するジャディアンス10mg群のハザード比は0.79(95.03%CI:0.69~0.90)、p<0.001(Cox比例ハザード回帰モデル)であり、ジャディアンス10mg群の優越性が検証されました。
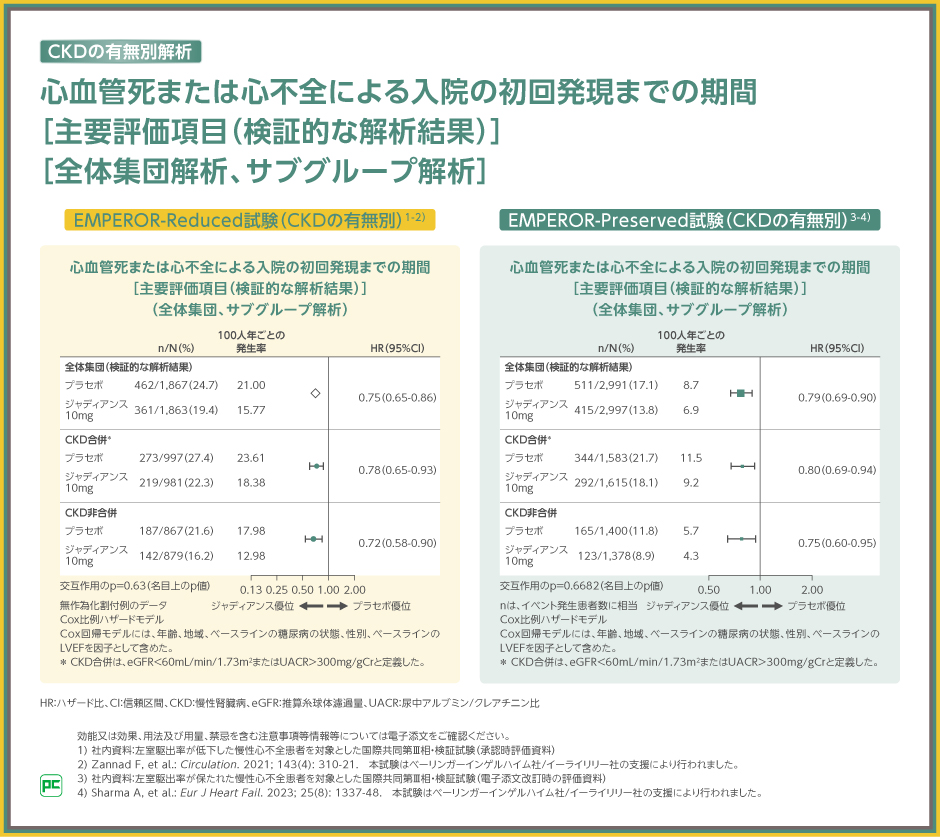
両試験では、主要評価項目である心血管死または心不全による入院の初回発現までの期間について、CKDの合併の有無別にサブグループ解析を行いました。
EMPEROR-Reduced試験の主要評価項目について、CKD合併でのプラセボ群に対するジャディアンス10mg群のハザード比は0.78(95%CI:0.65~0.93)、CKD非合併でのプラセボ群に対するジャディアンス10mg群のハザード比は0.72(95%CI:0.58~0.90)(交互作用のp値:0.63、名目上のp値)でした。
EMPEROR-Preserved試験の主要評価項目について、CKD合併におけるプラセボ群に対するジャディアンス10mg群のハザード比は0.80(95%CI:0.69~0.94)、CKD非合併でのプラセボ群に対するジャディアンス10mg群のハザード比は0.75(95%CI:0.60~0.95)(交互作用のp値:0.6682、名目上のp値)でした。
【参考情報】
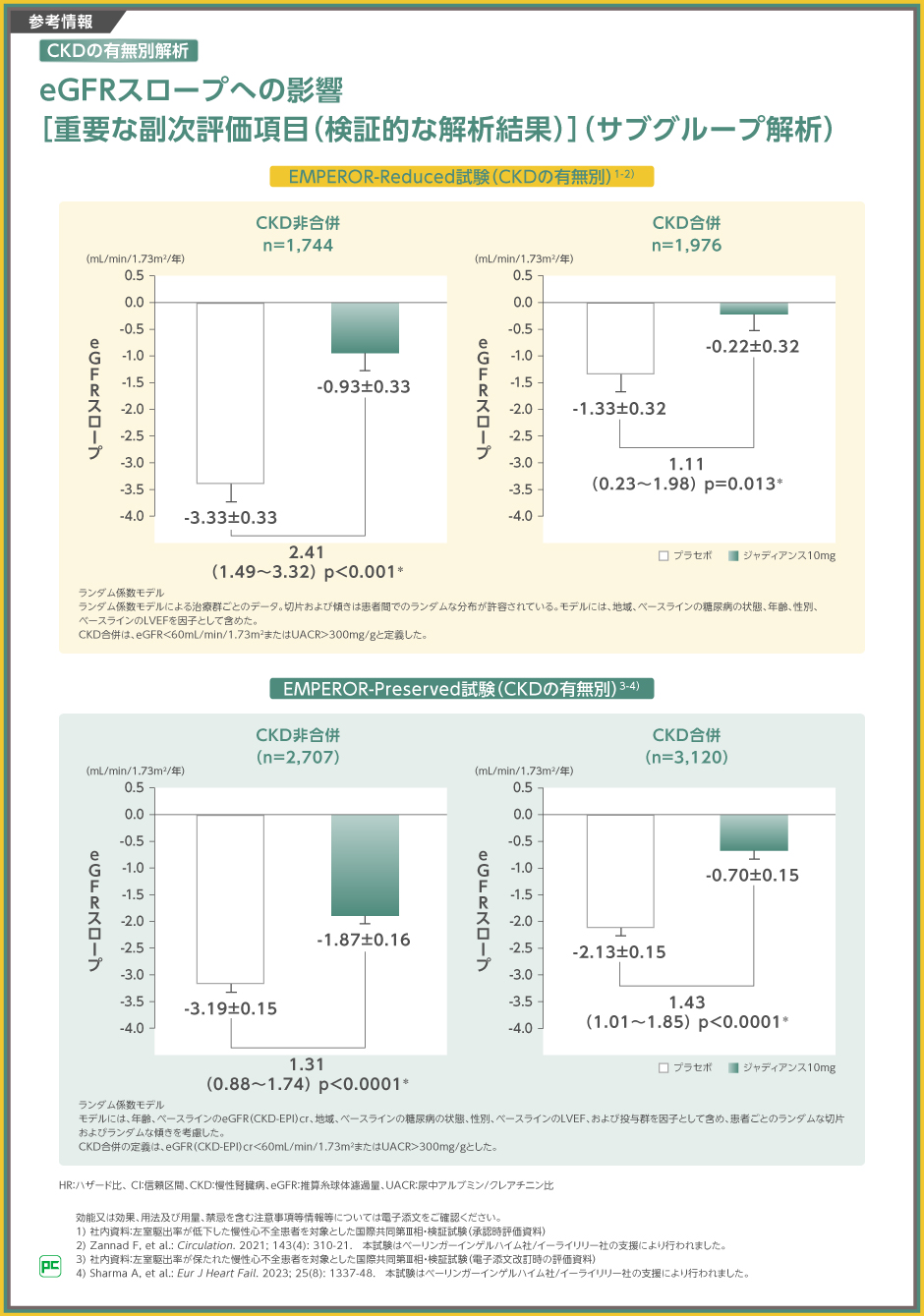
慢性心不全の患者さんに対するジャディアンス10mgの腎機能への影響について、eGFRスロープ(eGFRの低下速度)を検討しました。
EMPEROR-Reduced試験のCKD合併群において、ジャディアンス10mg群は、プラセボ群よりもeGFRの低下速度を1.11mL/min/1.73m2/年緩やかにしました。EMPEROR-Preserved試験のCKD合併群において、ジャディアンス10mg群は、プラセボ群よりもeGFRの低下速度を1.43mL/min/1.73m2/年緩やかにしました。

EMPEROR-Reduced試験における有害事象の発現割合はジャディアンス10mg群で76.2%でした。
主な有害事象は、ジャディアンス10mg群で心不全17.8%、低血圧7.0%、腎機能障害5.6%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で心不全332例、心室性頻脈55例、肺炎53例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。

EMPEROR-Preserved試験における有害事象の発現割合はジャディアンス10mg群で85.9%でした。
主な有害事象は、ジャディアンス10mg群で心不全15.0%、尿路感染7.9%、低血圧7.7%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で心不全448例、肺炎100例、心房細動92例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
ジャディアンスの慢性腎臓病※2に対するエビデンス
EMPA-KIDNEY試験
※2 ただし、末期腎不全又は透析施行中の患者を除く。

慢性心不全※1の治療薬であるジャディアンス10mgは、慢性腎臓病※2への適応も有しています。
慢性腎臓病に対する効果のエビデンスとなったEMPA-KIDNEY試験は、糖尿病合併の有無にかかわらず、腎疾患進行のリスクのある慢性腎臓病患者を対象とし、ジャディアンス10mgを1日1回経口投与した時の有効性および安全性をプラセボと比較検討しました。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。

全体集団において、ジャディアンス10mgの投与により、腎疾患進行または心血管死の初回発現までの期間のハザード比は0.73(99.83%CI:0.59~0.89)、p<0.0001(vs. プラセボ群、Cox回帰モデル)であり、ジャディアンス10mg群の優越性が検証されました。
日本人集団においても、ジャディアンス10mgの投与により、主要評価項目のリスクが56%低下しました(p=0.0004、名目上のp値、Cox回帰モデル)。
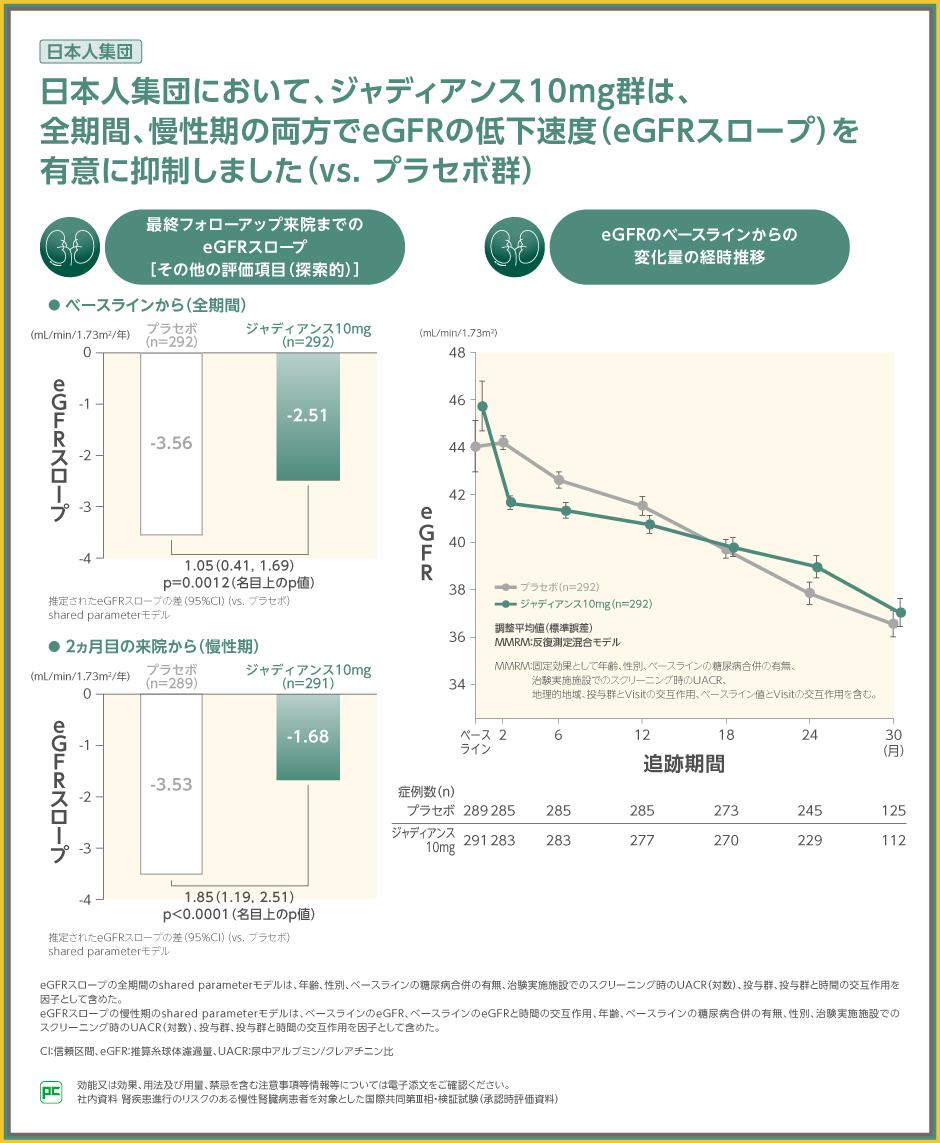
EMPA-KIDNEY試験では、eGFRの低下速度に対する作用としてeGFRスロープを検討しました。
日本人集団では、ベースラインから最終フォローアップ来院まで(全期間)において、ジャディアンス投与により、eGFRの低下速度を1.05mL/min/1.73m2/年緩やかにしました(vs.プラセボ群、p=0.0012、名目上のp値、shared parameterモデル)。
2ヵ月目の来院から最終フォローアップ来院まで(慢性期)において、ジャディアンス投与により、eGFRの低下速度を1.85mL/min/1.73m2/年緩やかにしました(vs.プラセボ群、p<0.0001、名目上のp値、shared parameterモデル)。
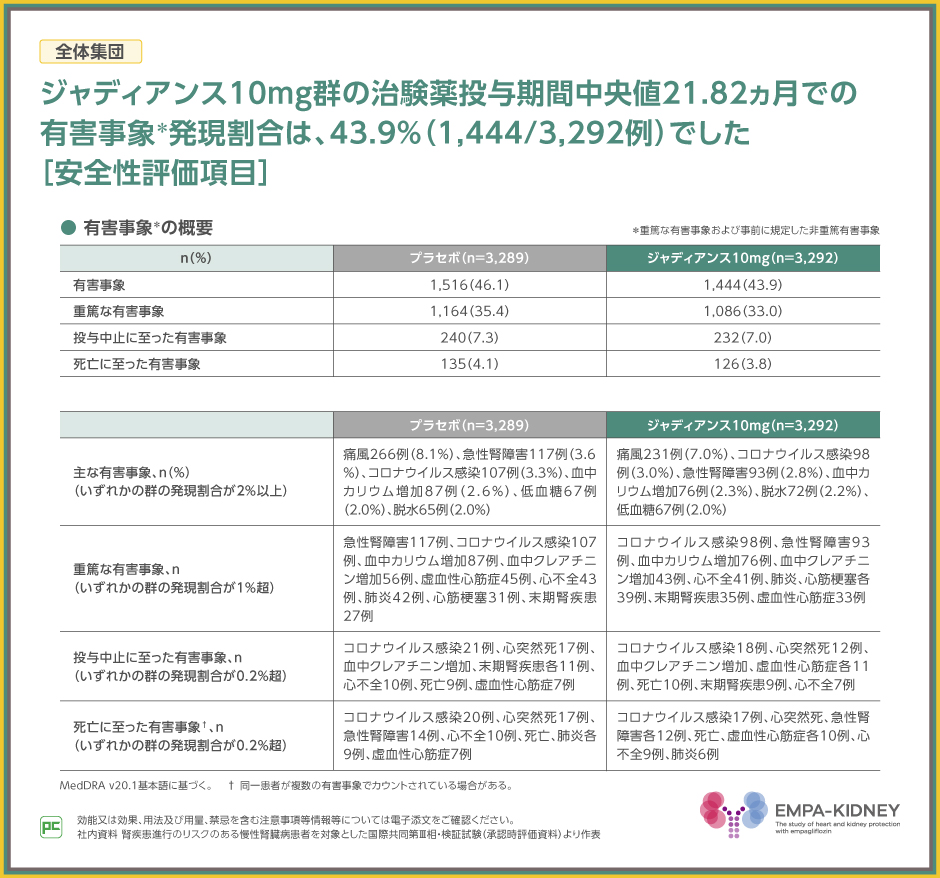
EMPA-KIDNEY試験において、重篤な有害事象および事前に規定した非重篤有害事象に限定して有害事象を収集した結果、全体集団での発現割合はジャディアンス10mg群で43.9%でした。
主な有害事象は、ジャディアンス10mg群で痛風7.0%、コロナウイルス感染3.0%、急性腎障害2.8%等でした。
また、重篤な有害事象は、ジャディアンス10mg群でコロナウイルス感染98例、急性腎障害93例、血中カリウム増加76例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。

EMPA-KIDNEY試験における日本人集団での有害事象の発現割合はジャディアンス10mg群で37.7%でした。
主な有害事象は、ジャディアンス10mg群で低血糖3.1%、白内障手術2.7%、脱水2.1%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で白内障手術8例、末期腎疾患5例、動静脈シャント手術4例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした
慢性心不全※1、慢性腎臓病※2の両方に適応を持つジャディアンス10mg
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。
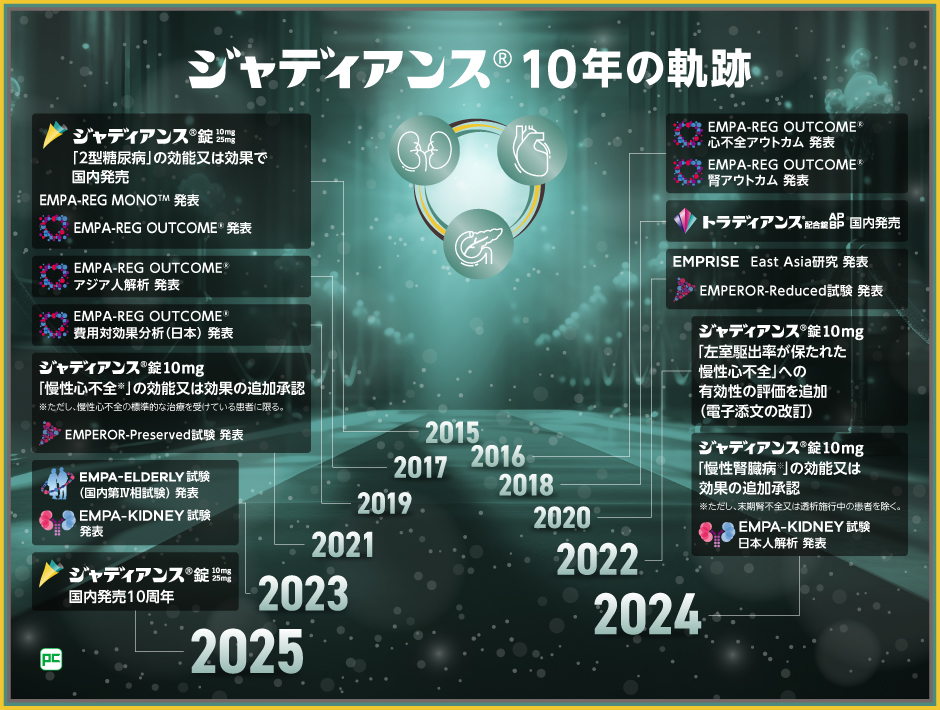
ジャディアンス錠10mg・25mgは、2015年に2型糖尿病の治療薬として国内で発売されました。その後、ジャディアンス錠10mgは2021年に慢性心不全※1、2024年に慢性腎臓病※2への効能又は効果、用法及び用量が追加承認されました。
今日までの10年間、ジャディアンスは毎年臨床成績の発表等を行い、血糖管理・心保護・腎保護の3領域についてのエビデンスを構築してきました。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。
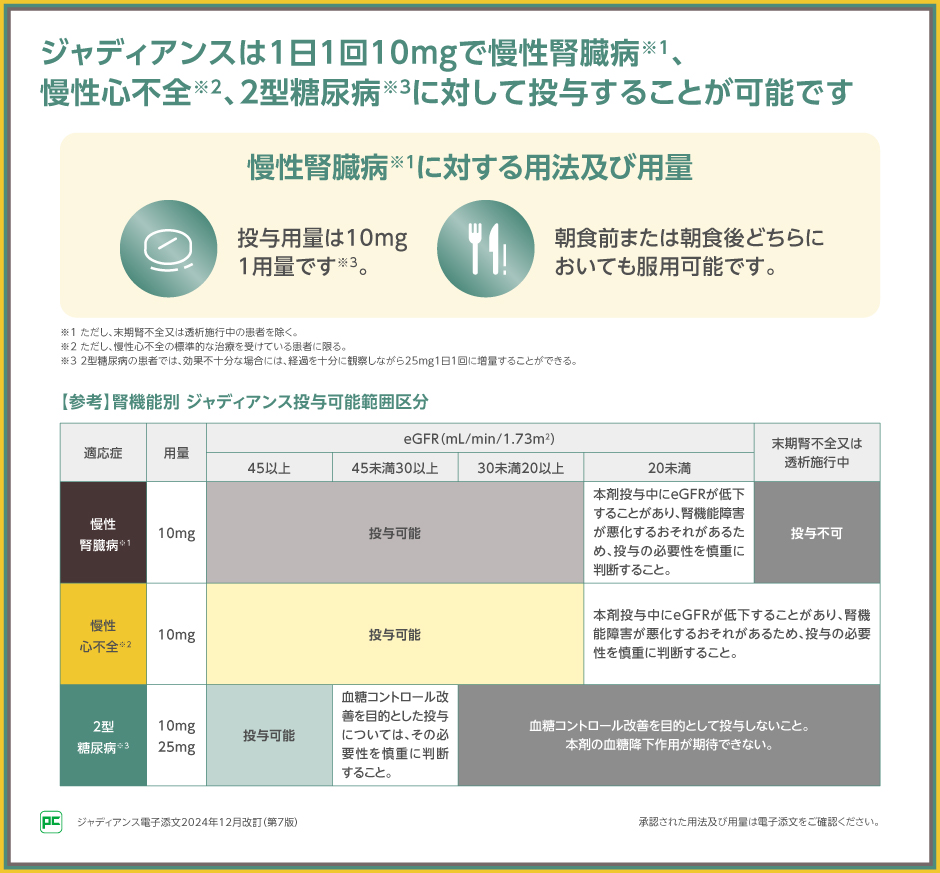
ジャディアンスの、慢性心不全※1、慢性腎臓病※2に対する用量設定は1日1回10mgであり、朝食前または朝食後どちらにおいても服用可能です。
なお、2型糖尿病に対しては1日1回10mgまたは25mgの用量が設定されており、治療強化が可能です。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。

ジャディアンス錠10mgは、EMPEROR-Reduced試験、EMPEROR-Preserved試験において心不全に対する有効性が評価されており、左室駆出率を問わず慢性心不全※1への処方が可能です。
また、EMPA-KIDNEY試験により、慢性腎臓病に対する有効性も評価されました。
今回の心不全診療ガイドラインの改訂に関連する、慢性心不全※1および慢性腎臓病※2の両方に適応を持つジャディアンス錠10mgを、治療選択肢の一つとしてご検討ください。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。
その他の関連情報


心血管イベントを考慮したCKD治療の4つの戦略とジャディアンスの臨床成績
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



