
多発性筋炎/皮膚筋炎に伴う間質性肺疾患(PM/DM-ILD)に対する治療戦略 ~膠原病に伴う間質性肺疾患(CTD-ILD)診断・治療指針2025より~(静止画)
サイトへ公開:2025年07月04日 (金)
クイックリンク

2025年4月、日本呼吸器学会・日本リウマチ学会の共同編集による「膠原病に伴う間質性肺疾患 診断・治療指針 2025」(以下、CTD-ILD診断・治療指針2025年版)が発刊されました1)。CTD-ILD診断・治療指針2025年版では、多発性筋炎/皮膚筋炎に伴う間質性肺疾患(PM/DM-ILD)の治療アルゴリズムが改訂されました。
今回は、CTD-ILD診断・治療指針2025年版で改訂されたPM/DM-ILDの治療アルゴリズムを中心に、PM/DMに合併するILDの診断・治療介入の重要性について解説します。
PM/DMおよび進行性線維化を伴うPM/DM-ILDの推定患者数とILD診療の重要性
進行性線維化を伴うPM/DM-ILDの推定患者数
多発性筋炎(PM)/ 皮膚筋炎(DM)は、特発性炎症性筋疾患(IIM)のなかに分類され、骨格筋の炎症による対称性近位筋優位の筋力低下を来す結合組織疾患です1)。ILDは、PM/DMの約40%に合併し、予後に深く関連しています1)。
それでは、わが国において、PM/DM患者さんのうちどのくらいの割合でILDを発症し、また発症したPM/DM-ILDのうちどのくらいの割合が進行性線維化を伴う間質性肺疾患(PF-ILD)に進展するのでしょうか。
令和5年度末現在、特定医療費(指定難病)受給者証を交付された約2.7万人2)のPM/DM患者さんのうち、約40%1)にあたる約1万人がILDを発症すると予想されます。さらに、日本を含む7ヵ国の呼吸器専門医、リウマチ専門医、内科医を対象としたアンケート調査では、関節リウマチおよび全身性強皮症を除くCTD-ILD患者さんのうち24%がPF-ILDに進展すると推定されたため3)、わが国のPM/DM-ILD患者さん約1万人のうち約2千人がPF-ILDに該当する可能性があると概算できるでしょう(図1)。
図1 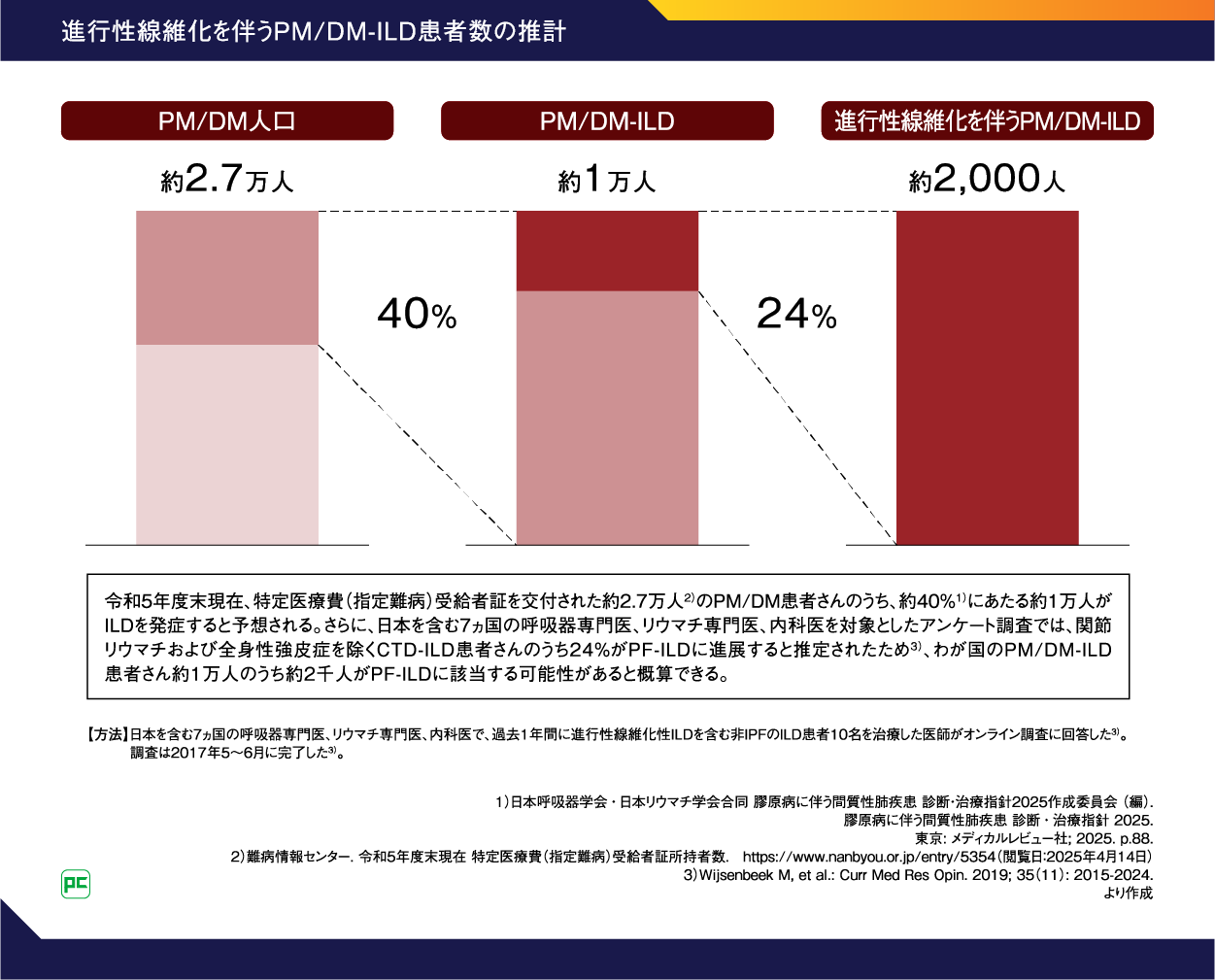
併発するILDの症状・身体所見
PM/DM-ILDでは、50~80%に息切れや乾性咳嗽といった呼吸器症状がみられ、fine crackles は90%以上で聴取されます1, 4, 5)。また、疾患初期や病変部が限局している場合には無症候性のことが多いため、呼吸機能検査や胸部CT検査による他覚的検査でILD の評価を行うことが重要です1, 6, 7)。
筋炎特異的自己抗体
PM/DMでは、さまざまな細胞成分に対する自己抗体が検出されます。浜松医科大学病院で1996~2015年の間に診断されたPM/DM-ILD患者60例を対象とした研究では、PM/DM-ILD患者60例中、いずれかの抗アミノアシルtRNA合成酵素(ARS)抗体陽性26例(43.3%)、抗メラノーマ分化関連遺伝子5(MDA5)抗体陽性15例(25%)、筋炎特異的自己抗体(MSA)陰性は15例(25%)でした(図2)6)。
図2 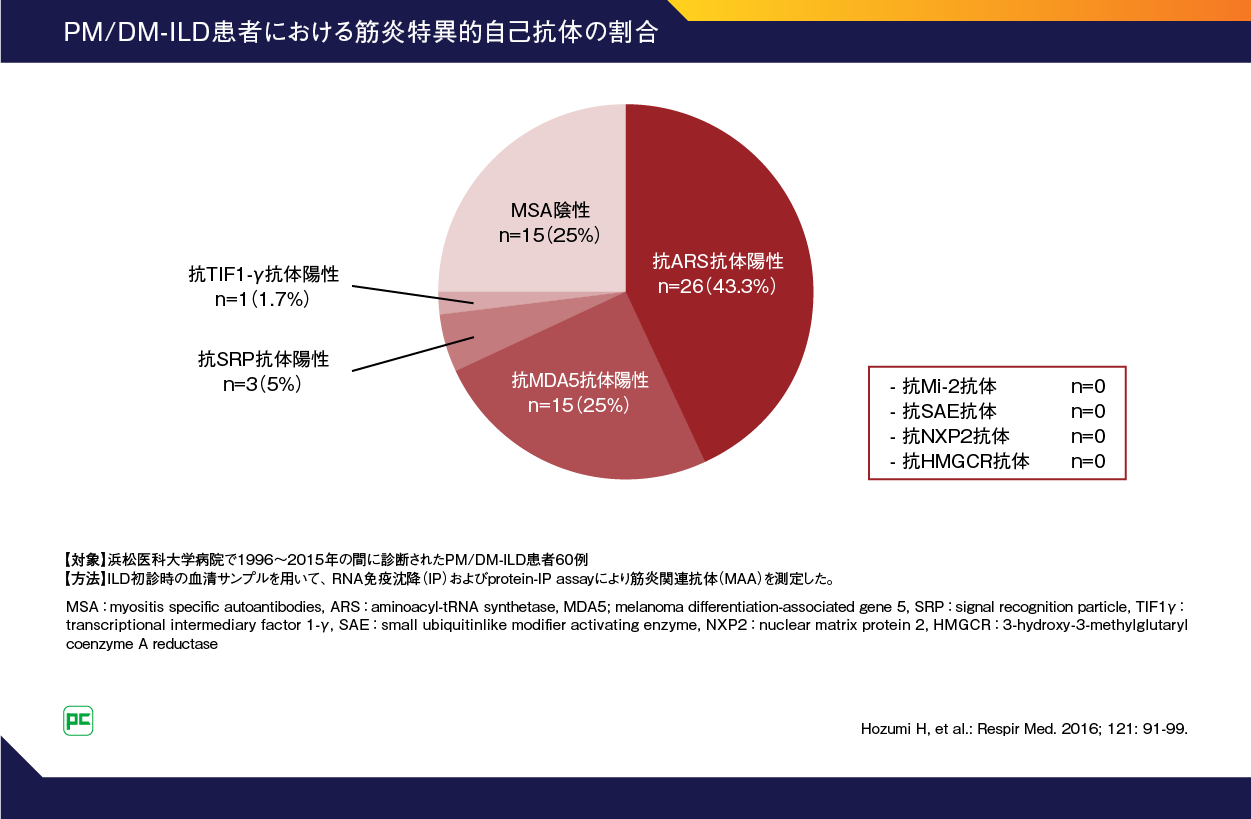
ILDの予後
ILDの病型別の予後では、国内の単施設後ろ向きコホートにおけるPM/DM-ILD 114例の検討において、5年生存率は、急性/亜急性ILDは52%、慢性ILDは87%と、急性/亜急性ILDで有意に予後不良でした(図3-A)4)。
また、抗MDA5抗体陽性例は急速に進行し、抗ARS抗体陽性例は慢性に進行することがわかります(図3-C)8)。ただ、抗ARS抗体陽性ILDの一部では急性~亜急性に発症することもあるほか、一次治療反応性が良好であっても治療経過中に再燃を来す症例9-12)などもしばしば存在します。
図3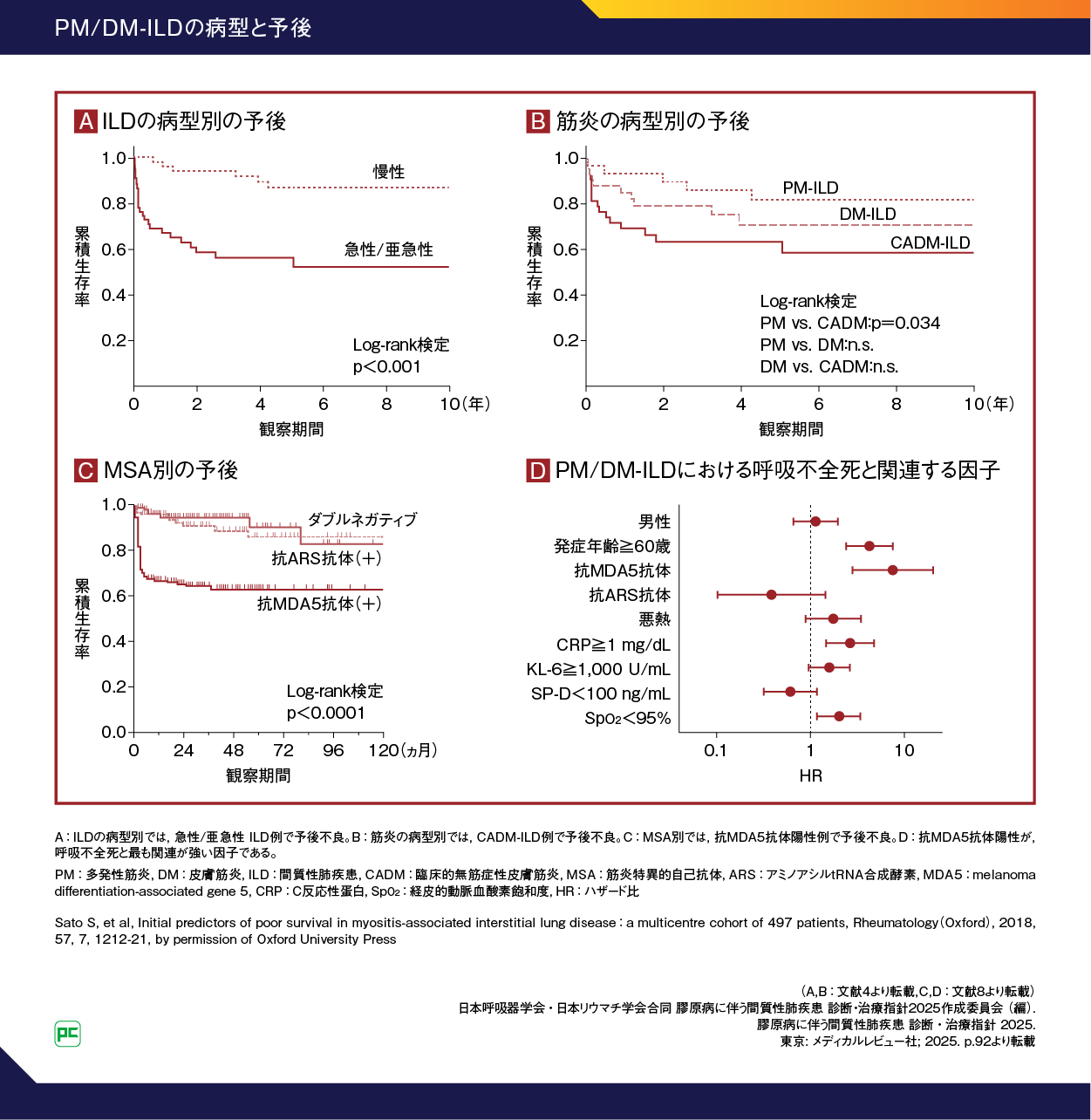
抗ARS抗体陽性群は、陰性群と比較して再発例が顕著に多く、ILDの経過に有意差があることも報告されており(p<0.01)(図4)12)、慎重にフォローアップする必要があります。
PM/DM-ILDでは、MSAの種類にかかわらず、疾患挙動に応じて治療介入を検討することが重要です。
図4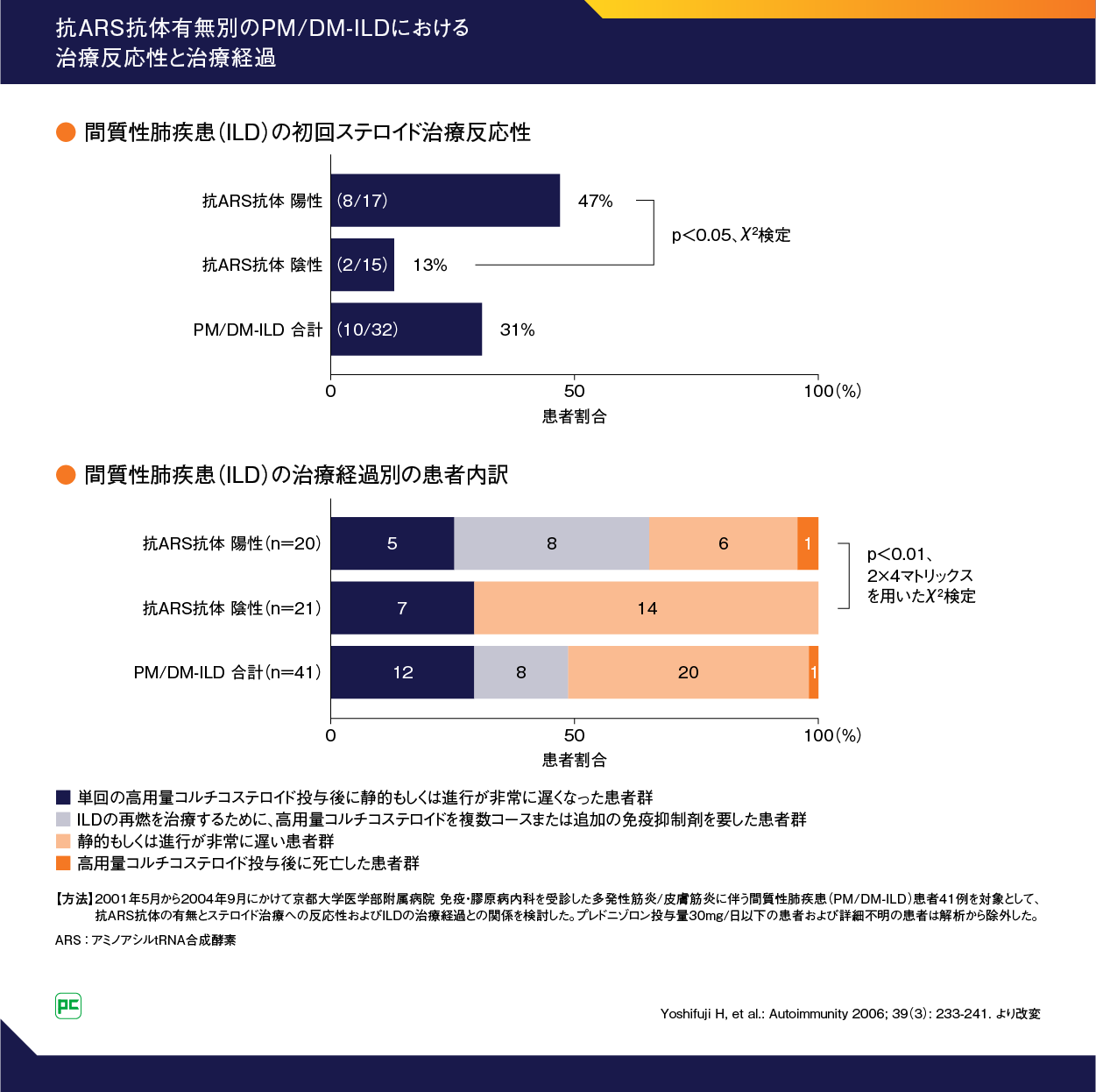
予後予測に関するバイオマーカー
PM/DM-ILD の予後予測に関するバイオマーカーの報告は、きわめて多岐にわたります。実臨床で使用可能な予後予測マーカーとして、血清フェリチン、KL-6、C反応性蛋白(CRP)、PaO2、SpO2などの有用性が後ろ向き解析により示されています4, 13-15)。抗MDA5抗体陽性例に限定した検討では、血清フェリチン高値、KL-6高値、PaO2低値、抗MDA5抗体価高値、血清IFN-λ3高値は予後不良と関連することが報告されています(表1)6, 8, 13-25)。
表1 
CTD-ILD診断・治療指針2025年版におけるPM/DM -ILDの治療アルゴリズム
PM/DM-ILDの発症様式や臨床経過は不均一なため、治療介入のタイミングを逃さないことが重要です。まず、診断時の臨床経過・画像所見からILDが慢性型(進行性、非進行性)、急性/ 亜急性型のいずれかを判断します1)。
治療介入を検討するための胸部画像所見
PM/DM-ILD における胸部HRCT所見では、浸潤影やすりガラス影が高頻度にみられ、分布は胸膜直下や気管支血管束周囲が主体です。牽引性気管支拡張や網状影も比較的高頻度に認められます4, 26-28)。蜂巣肺の頻度は10%以下で、他のCTD-ILDと比較して少なくなっています。抗ARS抗体陽性例の胸部HRCT所見では、主に下葉の気管支血管束周囲に分布する牽引性気管支拡張を伴う浸潤影と周囲のすりガラス影が特徴的です27, 29)(図5)。胸部HRCT検査はILDの検出に優れていますので、積極的に実施するとよいでしょう。
図5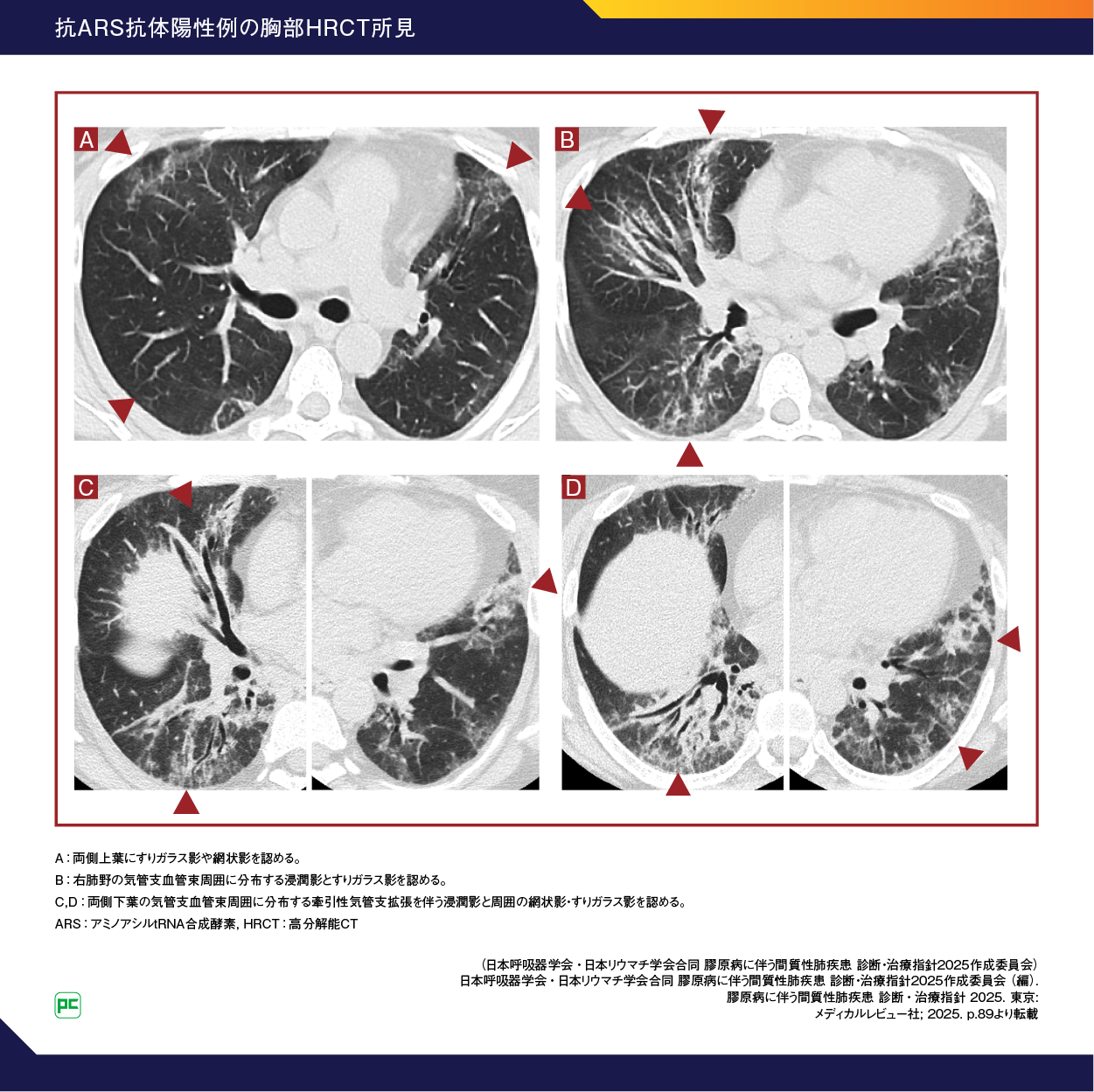
呼吸症状を把握するための患者報告型アウトカム尺度(PROMs)
CTD-ILDの症状について最も評価されるのは呼吸困難です。CTD-ILDで使用されるPROMsの代表的なものとしては表2に示されている尺度があり1, 30-62)、修正MRC息切れ質問票スケール(mMRC)やCOPD Assessment Test(CAT)などがあります。
表2 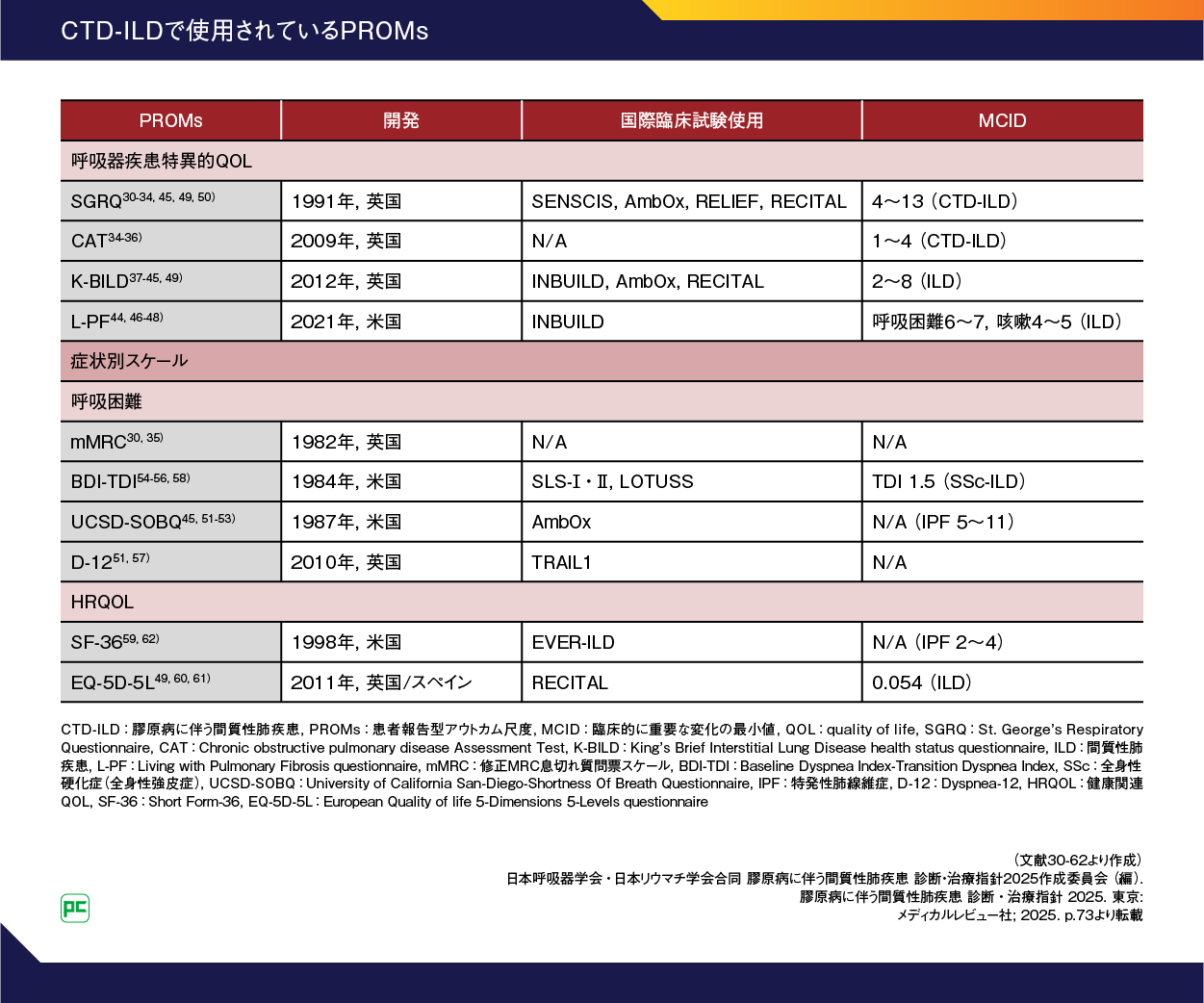
寛解導入時の治療アルゴリズム
図6にPM/DM-ILD の寛解導入時の治療アルゴリズムをお示しします1)。
図6 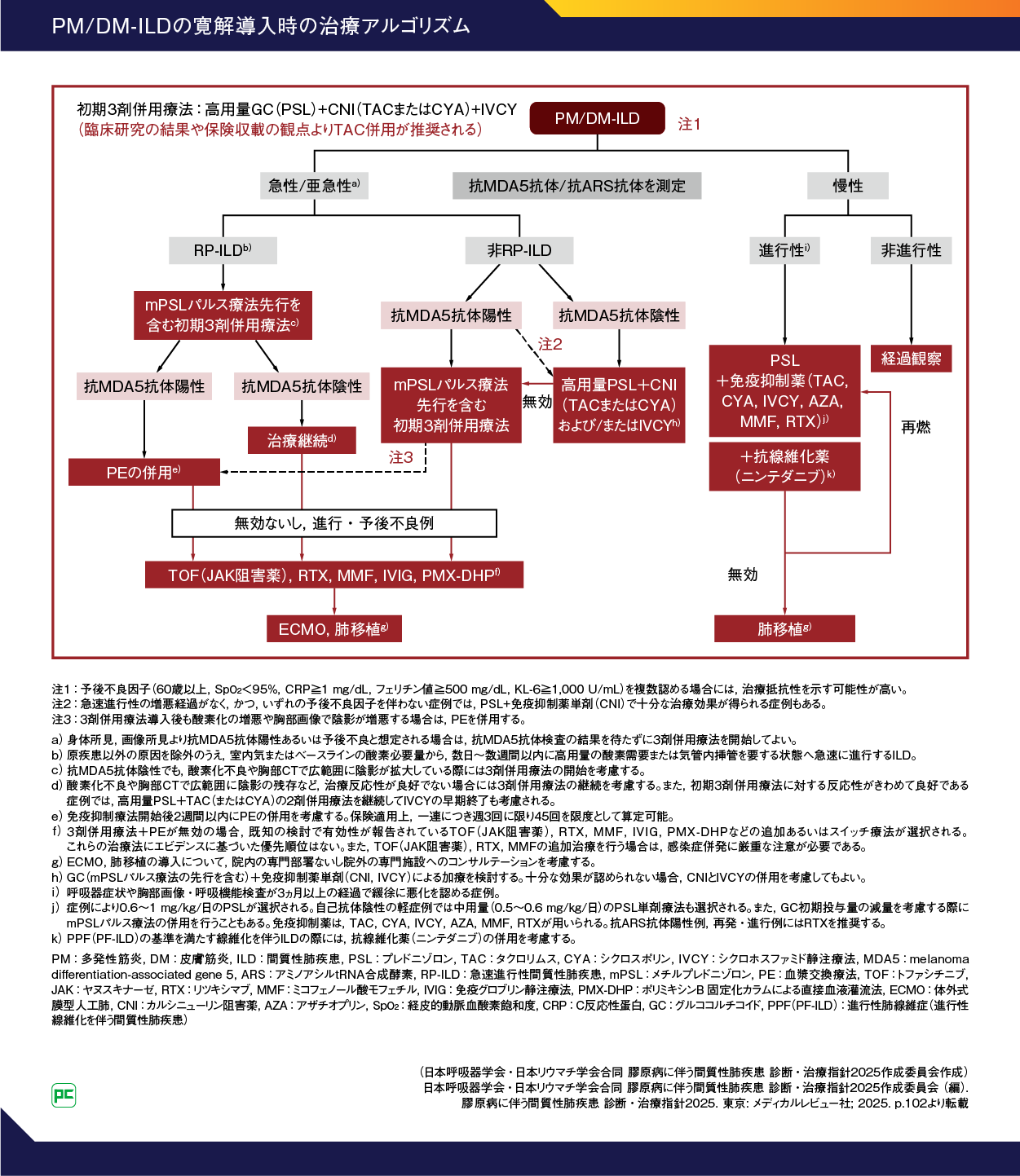
慢性型、急性/亜急性型の定義
CTD-ILD診断・治療指針2025年版では、慢性型、亜急性型、急性型(急速進行型[RP-ILD])は、以下のように定義されています1)。
慢性型:ILDに伴う呼吸器症状または画像所見が3ヵ月以上にわたって緩徐に進行する症例
亜急性型:1〜3ヵ月で呼吸器症状や画像所見の悪化を認める症例
急性型(急速進行型、RP-ILD):初発症状から4週間以内に日単位で急速な呼吸状態の悪化や胸部陰影の増悪を認める症例
ILDが急性/亜急性の場合
急性/亜急性型では、原疾患以外の原因を除外し、初発症状から4週間以内に日単位で急速な呼吸状態の悪化(酸素投与を要する)や胸部陰影の増悪を認めるRP-ILDの有無を確認すると同時に、抗MDA5抗体および抗ARS抗体の検査を行います。
RP-ILDでは、MSAの結果を問わずmPSLパルス療法を先行させ、高用量のグルココルチコイド(GC[PSL])+カルシニューリン阻害薬[CNI](タクロリムス[TAC]またはシクロスポリン[CYA])+シクロホスファミド点滴静注(IVCY)で治療を開始します。急性/ 亜急性型ILD(非RP-ILD)で抗MDA5抗体陽性の場合は、3剤併用療法(GC+CNI+IVCY)を考慮します。抗ARS抗体陽性、抗ARS抗体・抗MDA5抗体両者陰性の非RP-ILD例では、GC+免疫抑制薬単剤(CNI、IVCY)による治療を検討します。十分な効果が認められない場合には、CNIとIVCYの2剤併用療法を考慮してもよいでしょう。
ILDが慢性の場合
慢性型ILDで経過中に胸部画像・呼吸機能検査に悪化を認める場合は、GC(PSL)+ 免疫抑制薬(TAC、CYA、IVCY、AZA、MMF)の2剤併用療法で治療を開始します。また、GC初期投与量の減量を考慮する際に、mPSLパルス療法の併用を行うこともあります。慢性型抗MDA5抗体陽性例では、低酸素血症やフェリチン高値などの予後不良因子を認めなければ、GC+CNIの2剤併用療法を実施しますが、治療開始後も急速進行性の増悪経過の有無には注意が必要です。抗ARS抗体陽性例では、GC 減量とともにしばしば再燃がみられるため、初期より免疫抑制薬を併用します。
抗線維化薬投与の考慮
一次治療に奏効しても経過で緩徐に肺線維化が進行し、PPF(PF-ILD)の基準を満たす場合には、ニンテダニブ(オフェブ)の投与を考慮します。
進行性線維化を伴う間質性肺疾患(PF-ILD)におけるオフェブの有効性と安全性を検討した国際共同第Ⅲ相試験(INBUILD試験)において、全体集団における投与52週までのFVCの年間減少率(ランダム係数回帰モデルにより推定)(主要評価項目)は、オフェブ群-80.8mL/年、プラセボ群-187.8mL/年(群間差:107.0mL/年、95%CI:65.4–148.5、p<0.0001)でした(検証的な解析結果)44)。
そのほか、抗ARS抗体陽性RP-ILD例などに対するオフェブ投与に関する報告も、リアルワールドでみられるようになってきており、今後の研究等報告の蓄積が重要となります。
米国リウマチ学会(ACR)のガイドライン
ACRのガイドラインでは、オフェブはファーストライン治療にもかかわらず進行がみられた場合の治療選択肢として条件付きで推奨されています(図7)63)。
図7 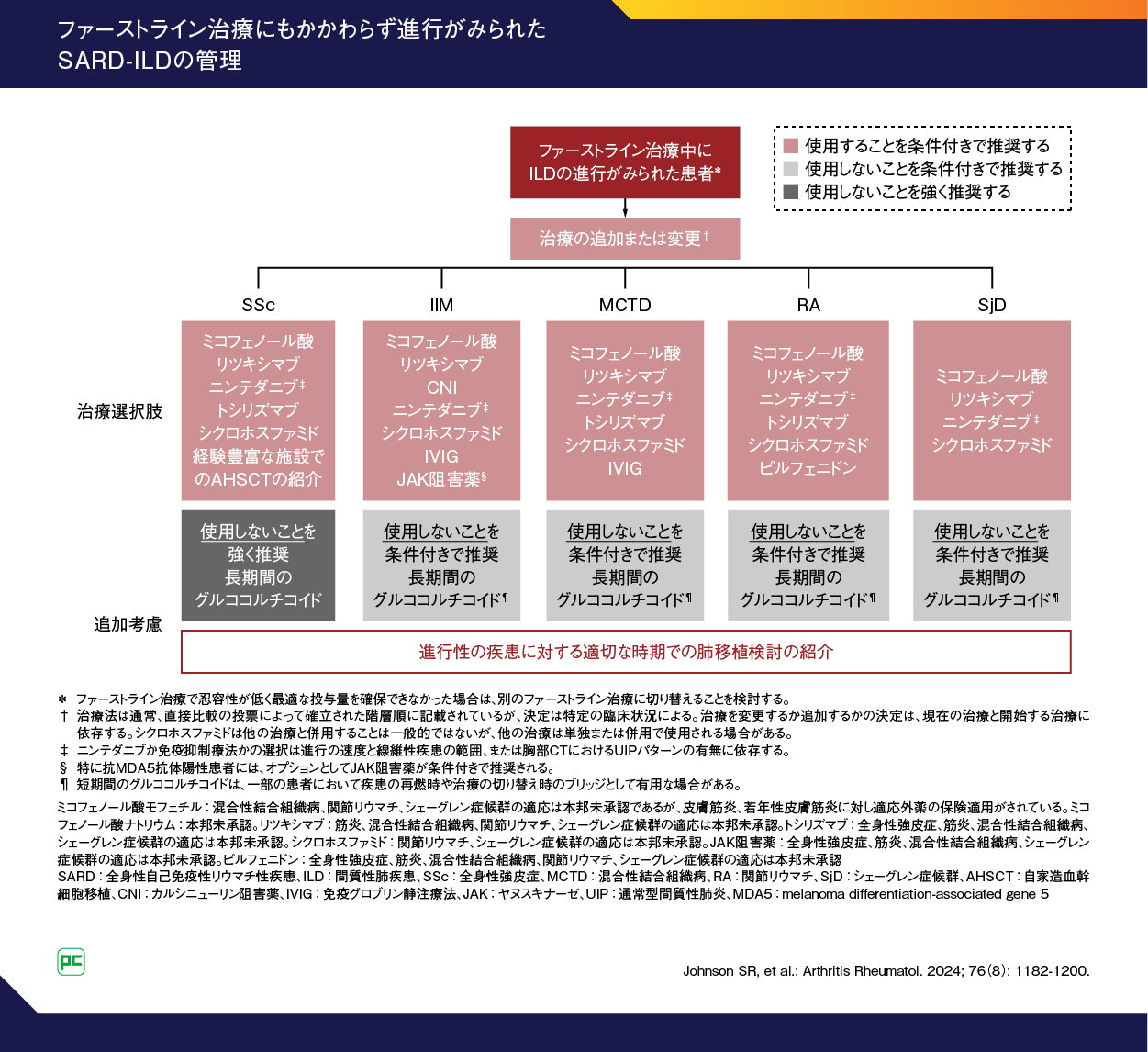
国際共同第Ⅲ相試験 INBUILD試験
試験概要
進行性線維化を伴う間質性肺疾患(PF-ILD)におけるオフェブの有効性と安全性を検討した国際共同第Ⅲ相試験(INBUILD試験)(図8)の試験概要です。
図8 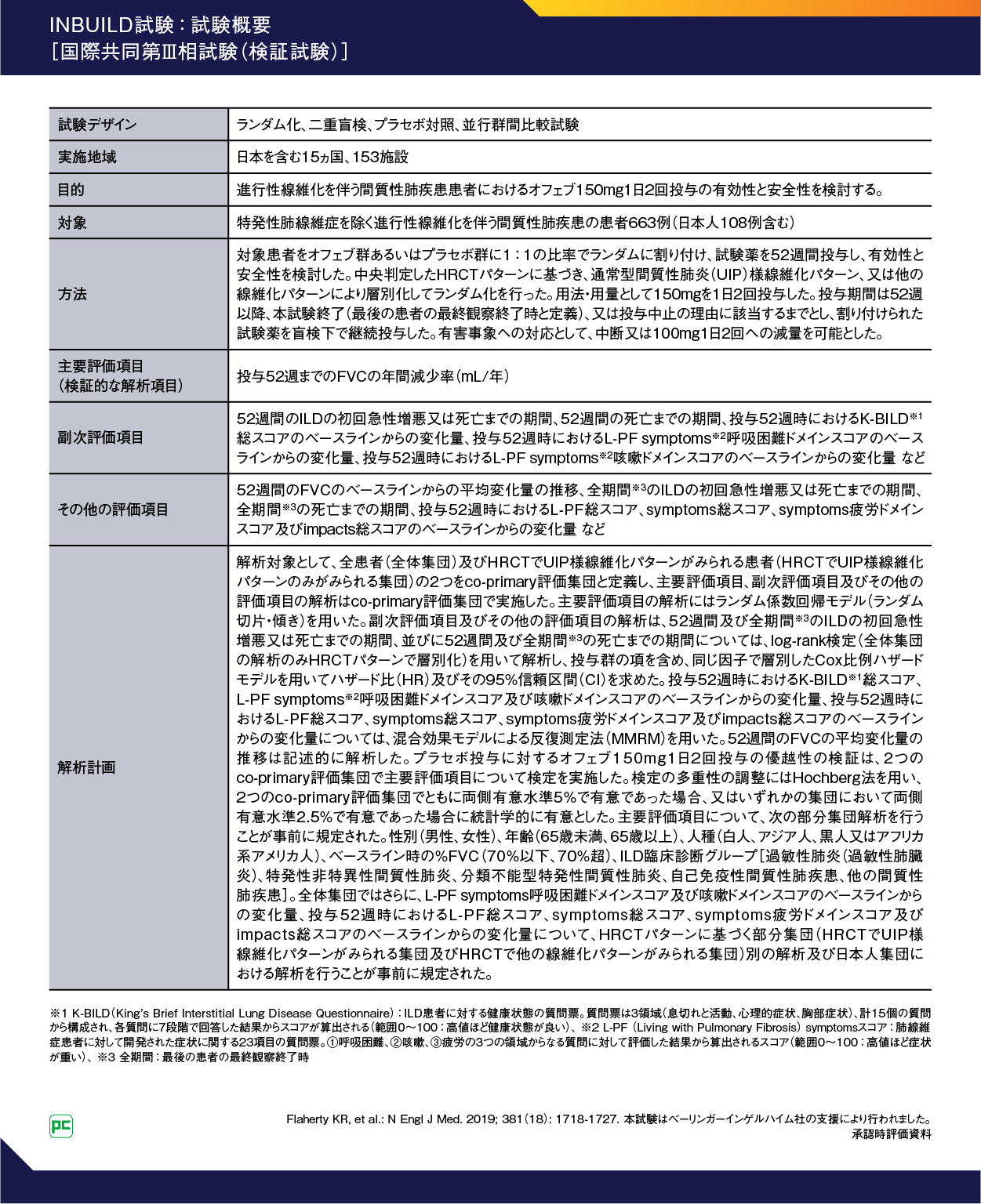
試験デザイン
本試験は、特発性肺線維症(IPF)以外の間質性肺疾患(ILD)と診断され、スクリーニング前の24ヵ月以内に医師により適切と考えられた疾患管理を行ったにもかかわらず、図9に示すILDの進行性の基準のいずれかを満たす患者663例を対象に行われました。スクリーニングされた患者は、オフェブ群あるいはプラセボ群にランダムに1:1で割り付けられました(図9)。
図9 
オフェブの呼吸機能低下抑制効果
全体集団における投与52週までのFVCの年間減少率(ランダム係数回帰モデルにより推定)(主要評価項目)は、オフェブ群-80.8mL/年、プラセボ群-187.8mL/年(群間差:107.0mL/年、95%CI:65.4–148.5、p<0.0001)でした(検証的な解析結果)(図10左)。
また、52週までのFVCのベースラインからの変化量は、右側の図のように推移しました(図10右)。
図10 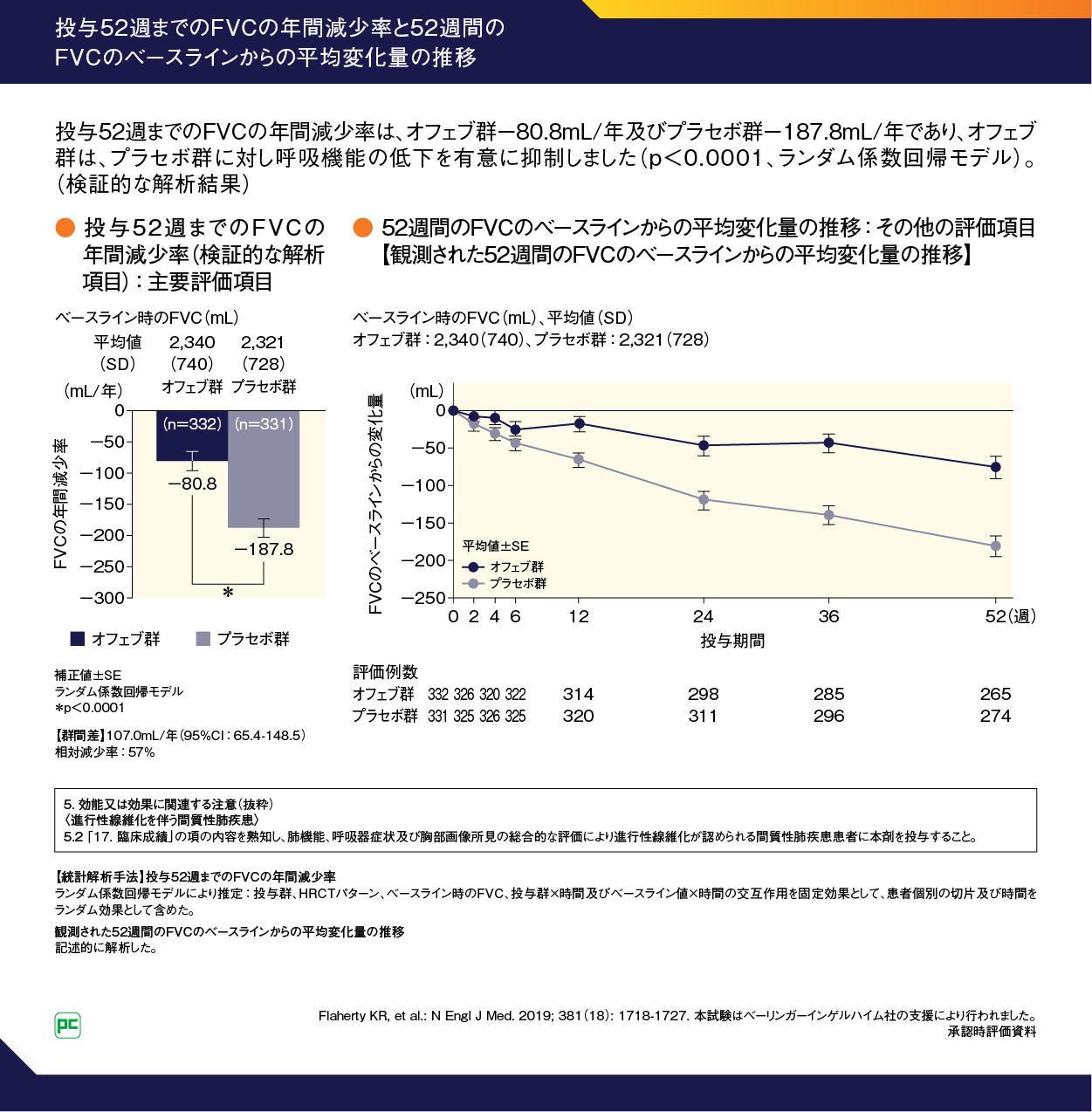
また、ベースライン時の%FVC別にみた投与52週までのFVCの年間減少率は、図11のとおりでした。
図11 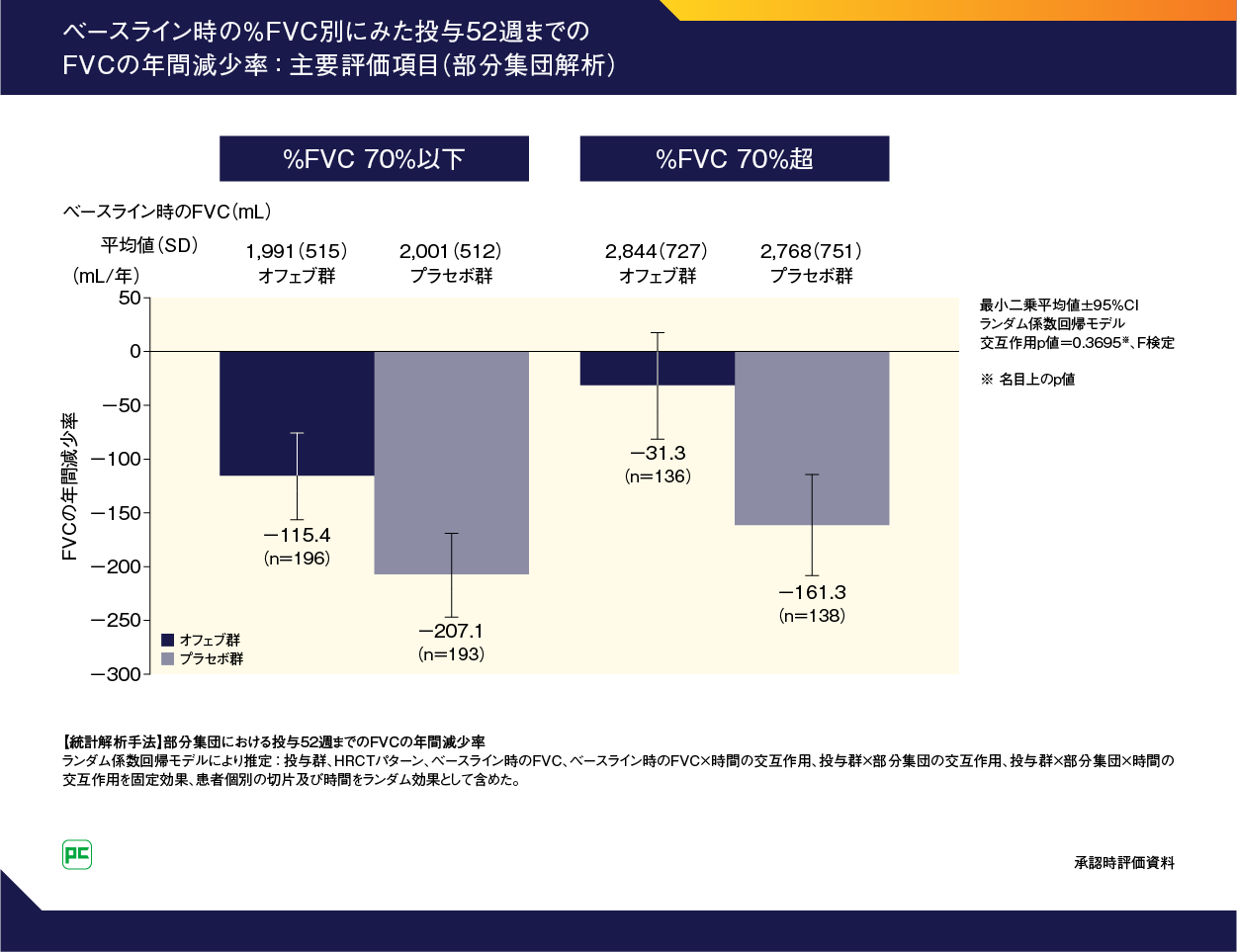
オフェブの呼吸器症状に対する影響
INBUILD試験では、オフェブの呼吸器症状に対する影響について、L-PFスコアを用いて検討されました。L-PFスコアは、肺線維症患者さんにおける症状に関する評価指標であり、symptomsとimpactsという2つのモジュールからなる44項目の質問で構成されます。なお、symptomsモジュールは、呼吸困難、咳嗽、疲労の3つのドメインで構成されています。SymptomsおよびimpactsスコアからL-PF総スコアが計算されます。
総スコアおよびドメインスコアの範囲は0~100であり、スコアが高値であるほど、症状が重いことを示します。
ベースライン時のL-PFスコアをお示しします。(表3)。
表3 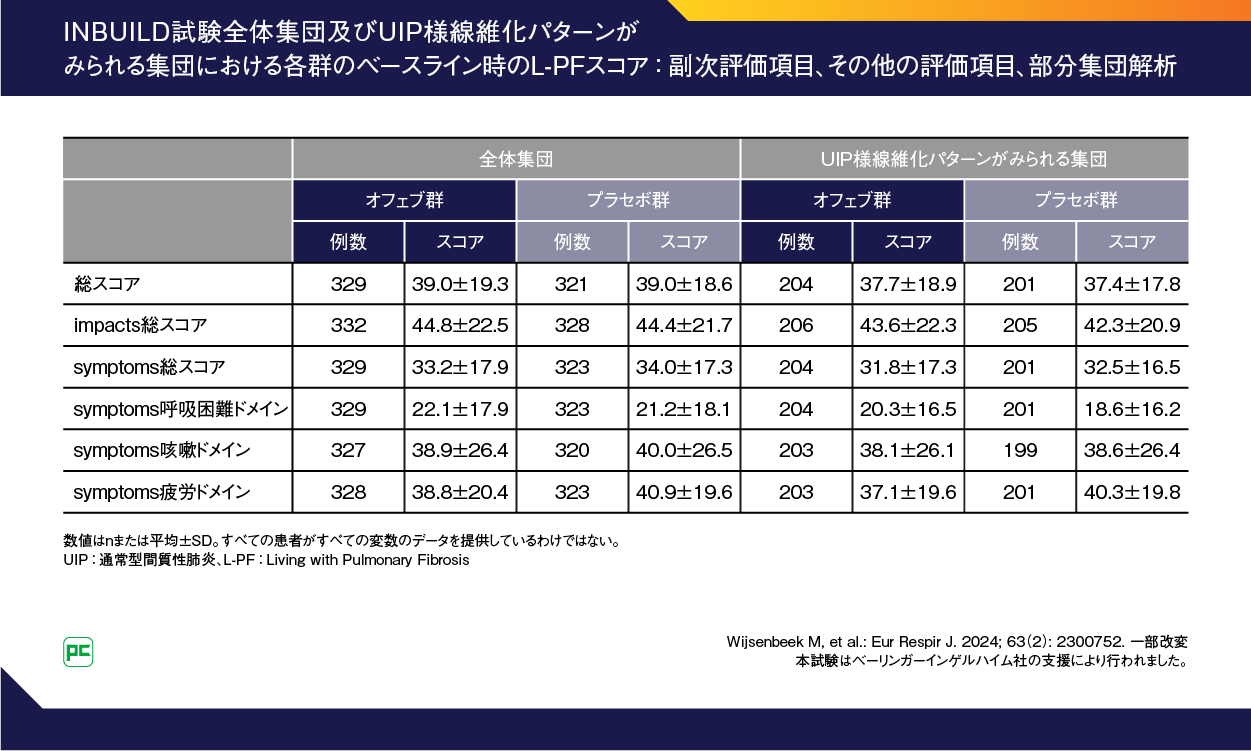
INBUILD試験全体集団の投与52週時におけるL-PF総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群0.5、プラセボ群5.1、群間差は-4.6(95%CI:-7.1--2.2)でした(p=0.0002、名目上のP値)(図12)。L-PF impacts総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群-0.2、プラセボ群4.6、群間差は-4.9(95%CI:-7.7--2.0)でした(p=0.0008、名目上のP値)。L-PF symptoms総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群1.3、プラセボ群5.3、群間差は-4.0(95%CI:-6.4--1.6)でした(p=0.0011、名目上のP値)。symptoms呼吸困難ドメインスコア、symptoms咳嗽ドメインスコア、symptoms疲労ドメインスコアについては、図12のとおりです。
図12 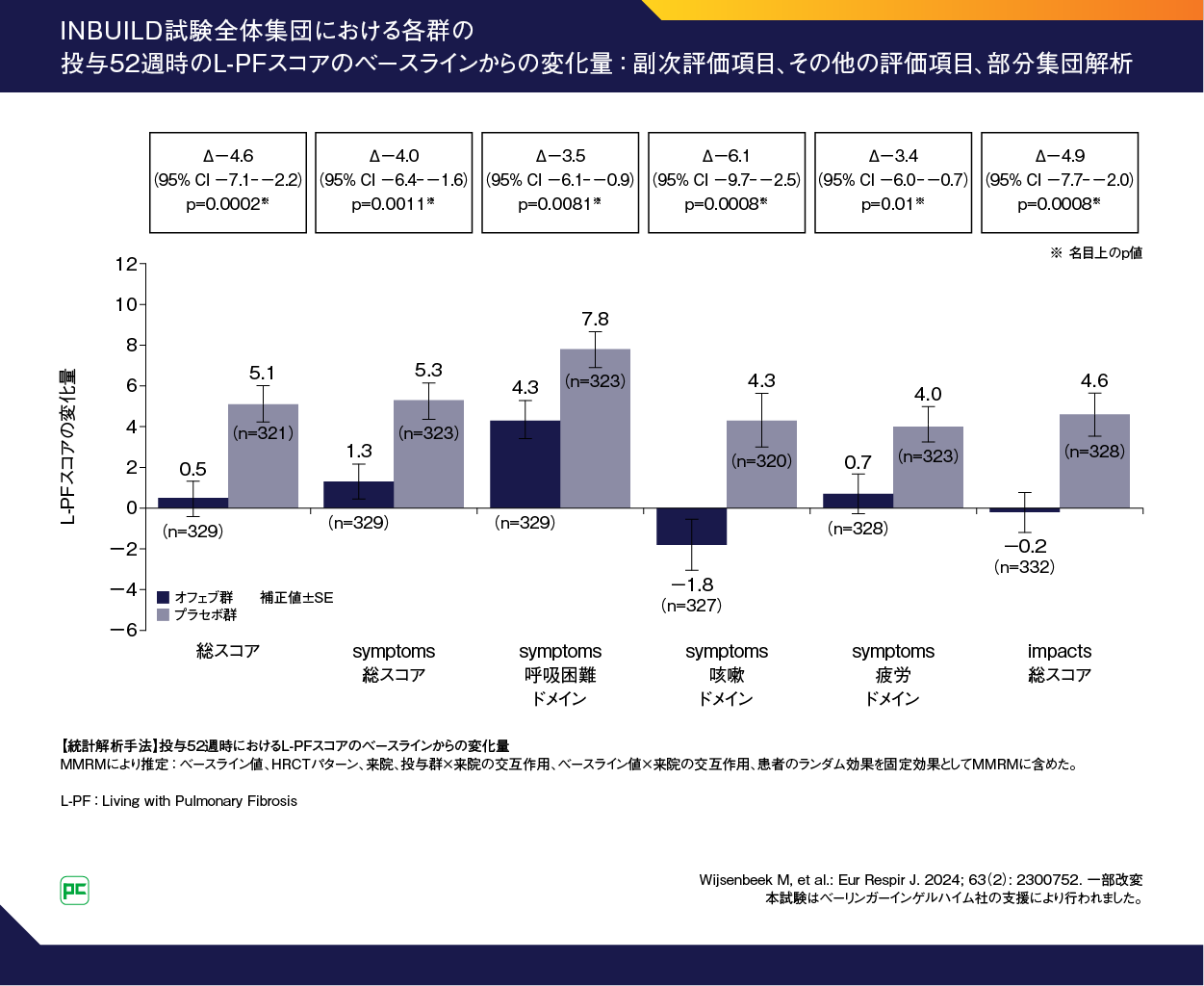
HRCTにおいてUIP様線維化パターンがみられる集団(co-primary評価集団・部分集団解析)の投与52週時におけるL-PF総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群0.2、プラセボ群5.5、群間差は-5.3(95%CI:-8.3--2.2)でした(p=0.0008、名目上のP値)(図13)。L-PF impacts総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群-0.2、プラセボ群4.9、群間差は-5.1(95%CI:-8.7--1.5)でした(p=0.0053、名目上のP値)。L-PF symptoms総スコアのベースラインからの平均変化量(MMRMにより推定)は、オフェブ群0.9、プラセボ群5.7、群間差は-4.9(95%CI:-7.9--1.8)でした(p=0.0019、名目上のP値)。symptoms呼吸困難ドメインスコア、symptoms咳嗽ドメインスコア、symptoms疲労ドメインスコアについては、図13のとおりです。
図13 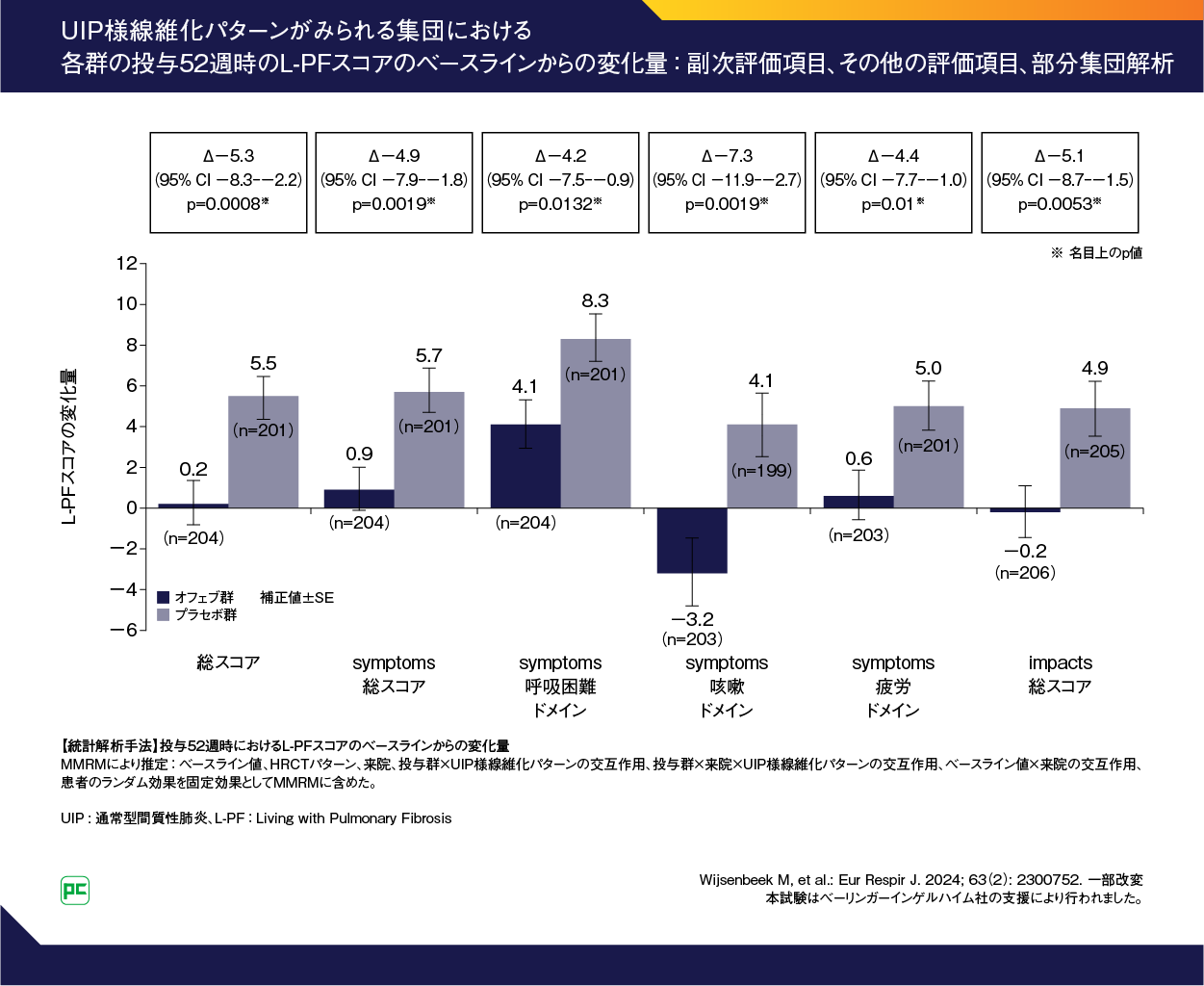
オフェブの安全性
INBUILD試験の全期間における有害事象は、オフェブ群で326例(98.2%)、プラセボ群で308例(93.1%)に認められました。オフェブ群における重篤な有害事象として主なものは肺炎24例、間質性肺疾患19例、急性呼吸不全16例などでした。オフェブ群において投与中止に至った有害事象は下痢21例、ALT増加6例、薬物性肝障害5例などであり、死亡に至った有害事象は、急性呼吸不全4例、呼吸不全3例などでした(表4)。
表4 
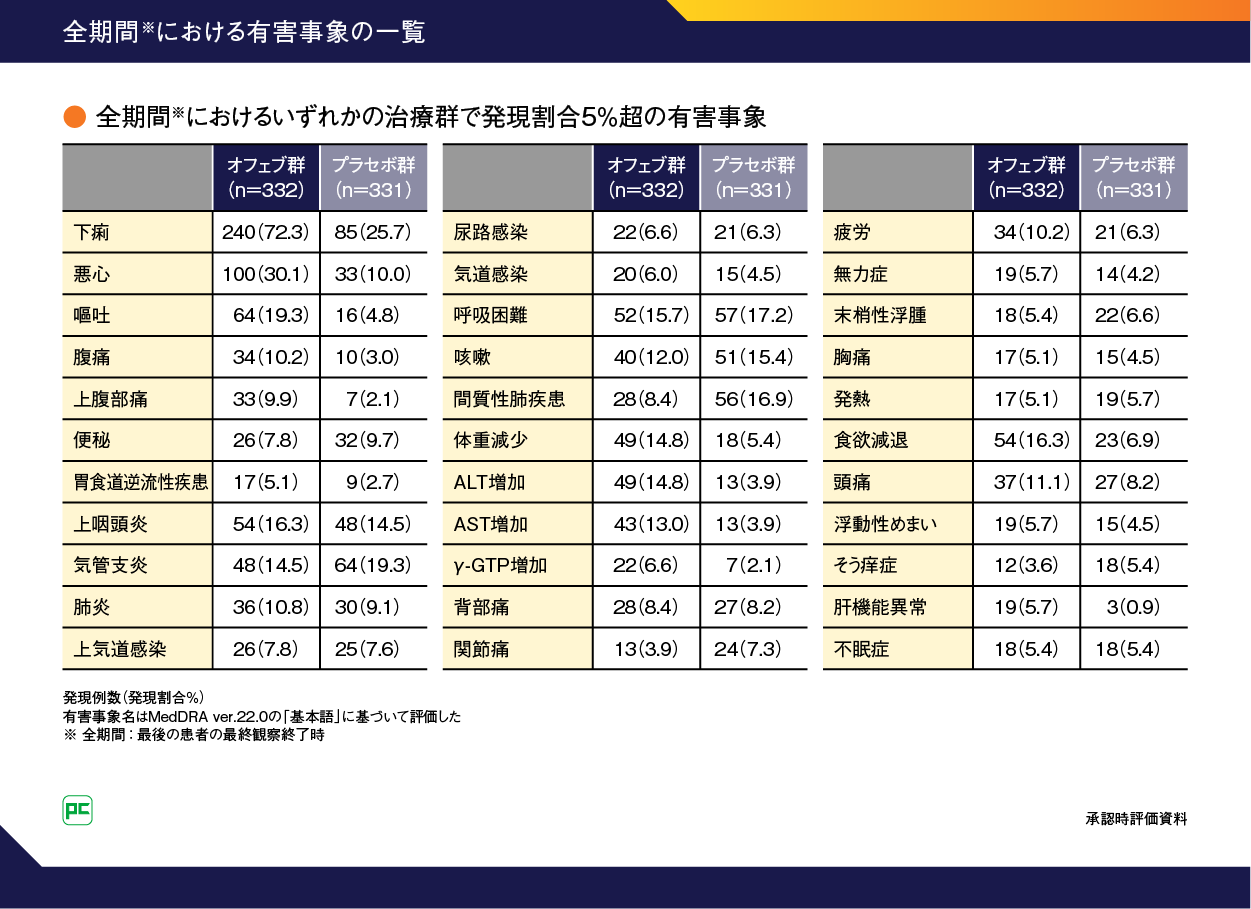
主な有害事象は、発現頻度が高い順にオフェブ群で下痢240例(72.3%)、悪心100例(30.1%)、嘔吐64例(19.3%)など、プラセボ群で下痢85例(25.7%)、気管支炎64例(19.3%)、呼吸困難57例(17.2%)などでした(表5)。
表5
まとめ
PM/DM-ILDの発症様式や臨床経過は不均一であるため、適切なタイミングで治療介入することが重要です。そのためには、呼吸器症状の有無、呼吸機能検査や胸部画像所見の増悪の有無などに注意しながら、慎重にフォローアップする必要があります。ILDが慢性で初期治療に奏効しても経過で緩徐に肺線維化が進行し、PPF(PF-ILD)の基準を満たす場合には、オフェブの投与をご検討ください。
今回ご紹介した内容を、PM/DM-ILD患者さんのご診療にお役立ていただけますと幸いです。
その他の関連情報


特発性肺線維症および進行性肺線維症 国際診療ガイドライン2022(静止画)
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



