
ジャディアンス10年の軌跡と心腎代謝疾患治療への貢献
サイトへ公開:2025年04月01日 (火)
クイックリンク
1) Mosenzon O, et al.: Cardiovasc Diabetol. 2021; 20(1): 92.
2) 日本老年医学会・日本糖尿病学会編・著: 高齢者糖尿病診療ガイドライン2017. 南江堂, 2017.
3) 日本循環器学会/日本心不全学会. 2021年 JCS/JHFS ガイドライン フォーカスアップデート版 急性・慢性心不全診療.
4) 日本糖尿病学会コンセンサスステートメント策定に関する委員会. 糖尿病. 2023; 66(10): 715-33.
5) 日本腎臓学会編: CKD診療ガイド2024, 東京医学社, 2024.
6) 社内資料 EMPA-REG EXTEND MONO(承認時評価資料)
7) Roden M, et al.: Cardiovasc Diabetol. 2015; 14:154. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
8) Zinman B, et al.: N Engl J Med. 2015; 373(22): 2117-28. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
9) 社内資料 左室駆出率が低下した慢性心不全患者を対象とした国際共同第Ⅲ相・検証試験(承認時評価資料)
10) Packer M, et al.: N Engl J Med. 2020; 383(15): 1413-24. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
11) 社内資料 左室駆出率が保たれた慢性心不全患者を対象とした国際共同第Ⅲ相・検証試験(電子添文改訂時の評価資料)
12) Anker SD, et al.: N Engl J Med. 2021; 385(16): 1451-61. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
13) Yabe D, et al.: Diabetes Obes Metab. 2023; 25(12): 3538-48.より改変 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
14) 社内資料 腎疾患進行のリスクのある慢性腎臓病患者を対象とした国際共同第Ⅲ相・検証試験(承認時評価資料)
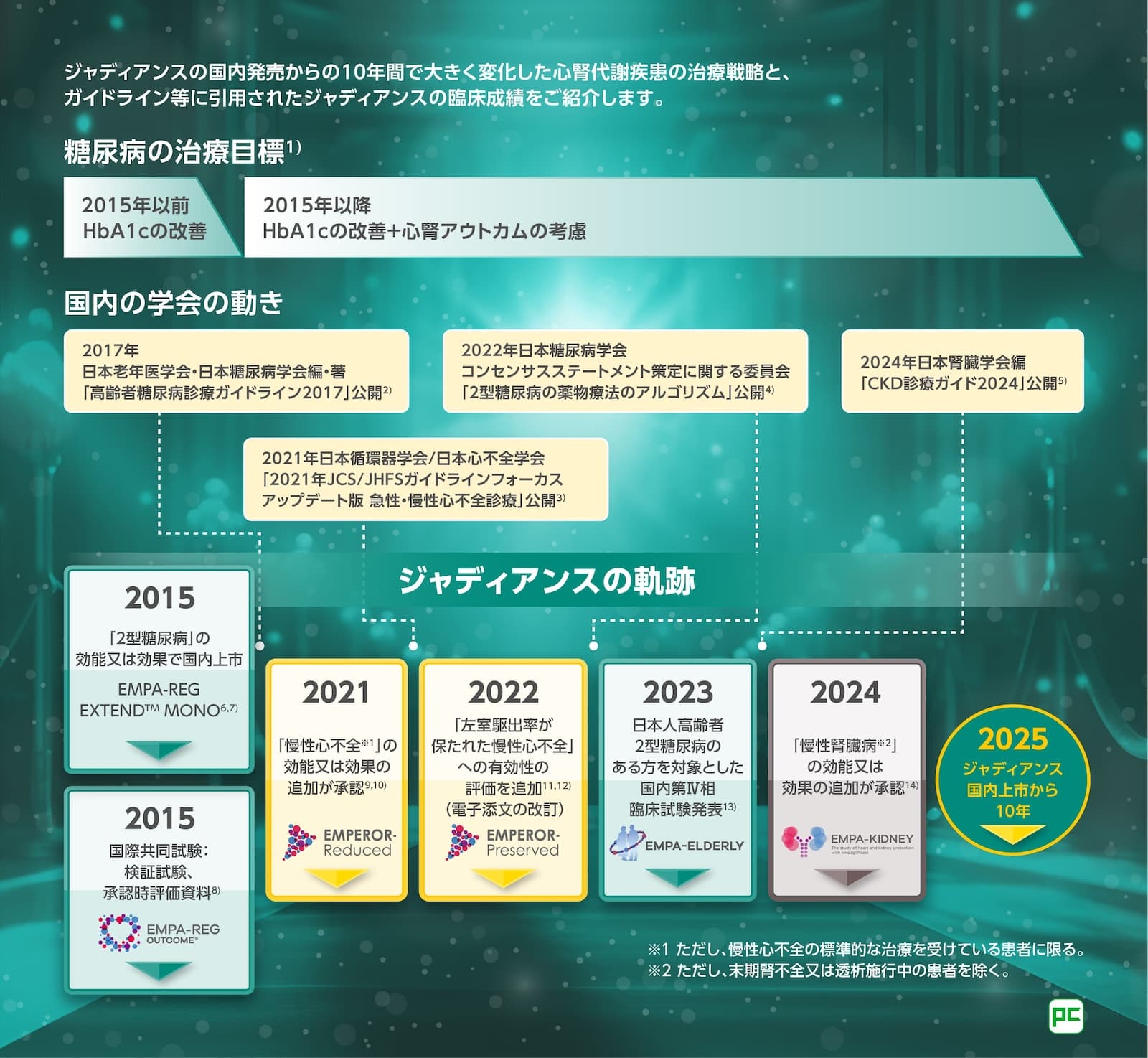
2015年
2型糖尿病のある方におけるHbA1c低下作用が評価されたジャディアンスは、 2015年2月に「2型糖尿病」の効能又は効果で国内発売
心腎代謝疾患の治療戦略は、様々なエビデンスの蓄積により、年々進歩しています。まずはその一角である2型糖尿病についての知見として、ジャディアンスの臨床成績をご紹介します。
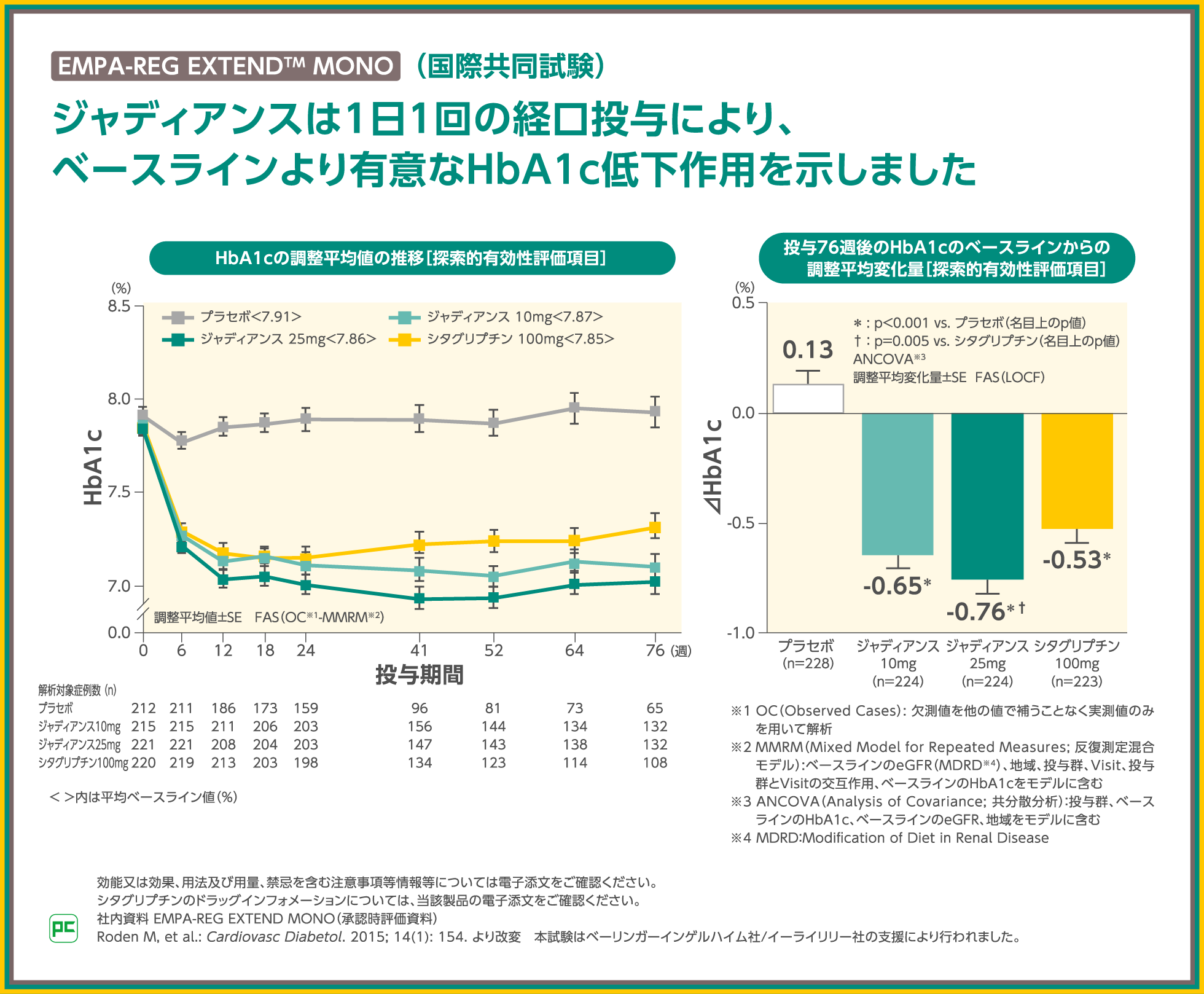
ジャディアンス国内発売に評価されたEMPA-REG MONOTM 1)の52週間延長試験であるEMPA-REG EXTENDTM MONOでは、ジャディアンスの長期投与による有効性と安全性を検討しました。
1) Eilbracht J. et al.: 社内資料 日本人2型糖尿病患者を含む国際共同第Ⅲ相24週投与試験(承認時評価資料)

76週後のHbA1cのベースラインからの調整平均変化量は、プラセボ群で0.13%、ジャディアンス10mg群で-0.65%、25mg群で-0.76%であり、プラセボ群と比較して、ジャディアンス10mg群、25mg群ともにHbA1cが有意に低下しました(いずれもp<0.001、名目上のp値、ANCOVA)。
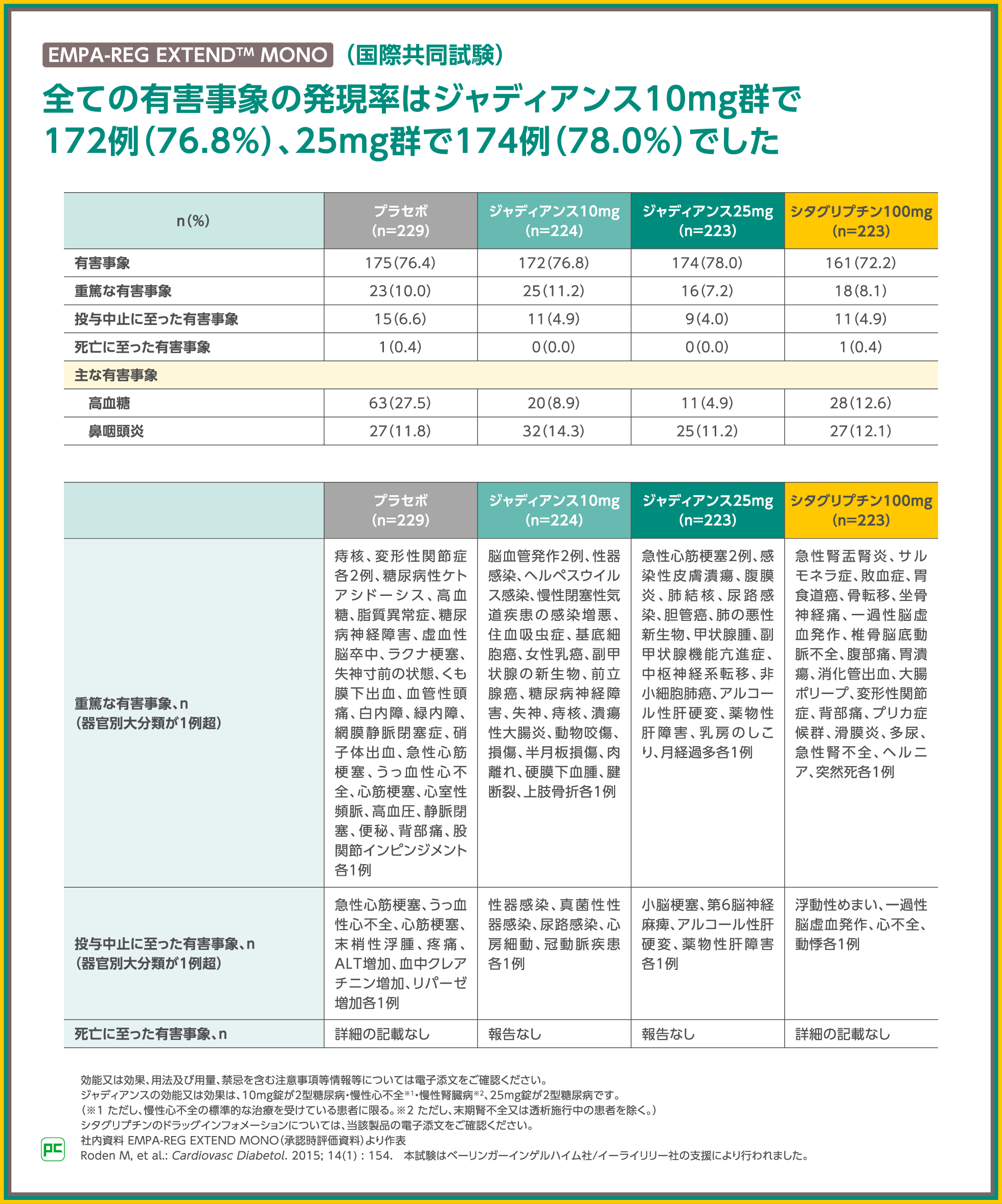
EMPA-REG EXTENDTM MONOにおける有害事象の発現率は、ジャディアンス10mg群で76.8%、25mg群で78.0%でした。
主な有害事象は、高血糖(ジャディアンス10mg群:8.9%、25mg群:4.9%)と鼻咽頭炎(ジャディアンス10mg群:14.3%、25mg群:11.2%)でした。
また、重篤な有害事象は、ジャディアンス10mg群で脳血管発作2例等、25mg群で急性心筋梗塞2例等でした。
投与中止、死亡に至った有害事象は表のとおりでした。
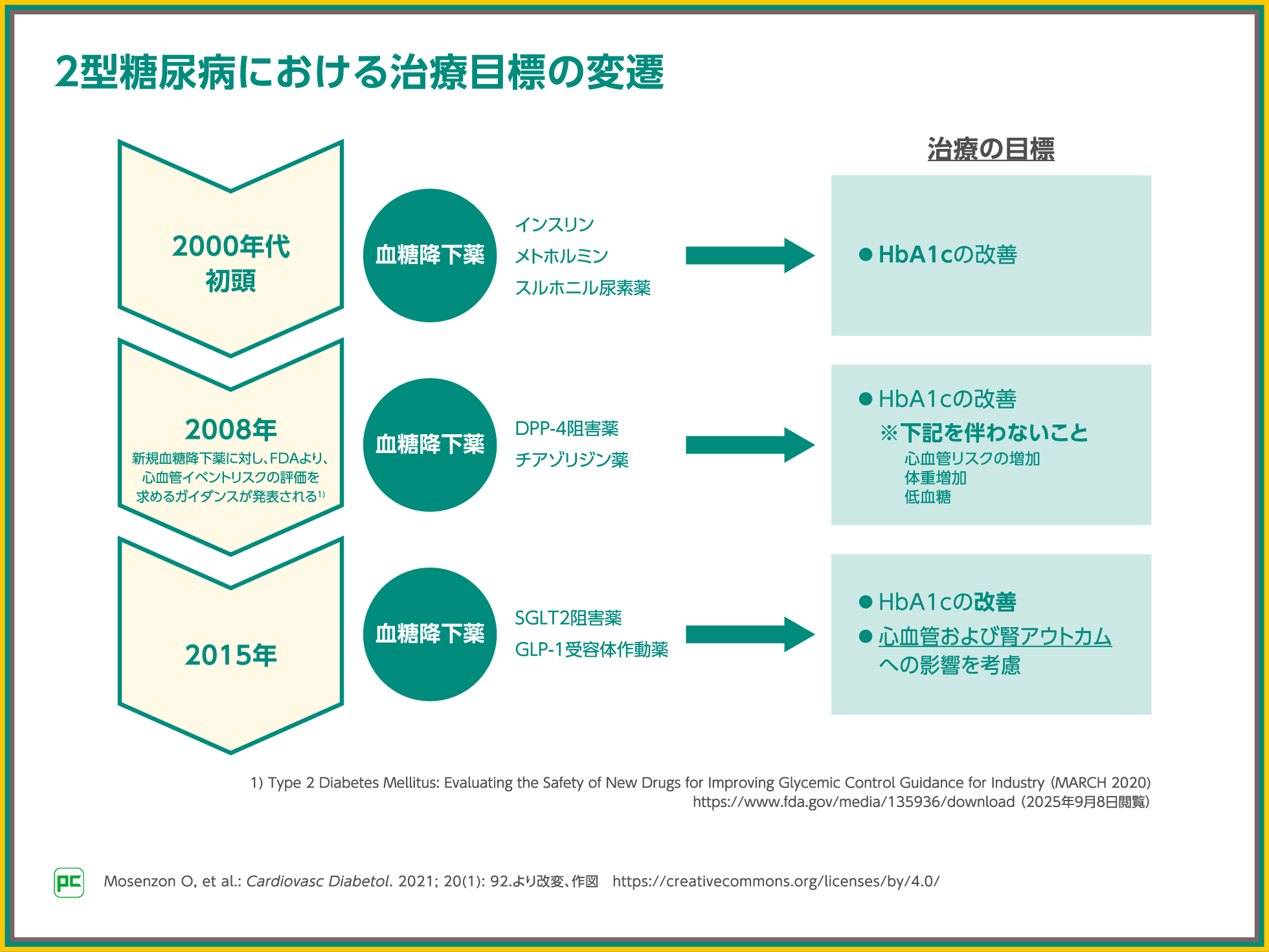
2015年以降、2型糖尿病の治療戦略は、世界的に大きく変化しました。
2015年以降の心血管および腎アウトカムに関するエビデンスの構築を受け、2型糖尿病の治療目標の世界の潮流が変化*
*Mosenzon O, et al.: Cardiovasc Diabetol. 2021; 20(1): 92.
様々な血糖降下薬が開発される中、米国FDAは2008年に新規血糖降下薬に対して心血管イベントリスクの評価を求めるガイダンスを発表、血糖降下薬には、HbA1cの改善だけでなく、心血管リスクの増加や体重増加、低血糖を伴わないことが求められるようになりました。
米国FDAのガイダンスを受けて、血糖降下薬は心血管および腎アウトカムへの影響を検討する臨床試験を開始、2015年以降、SGLT2阻害薬やGLP-1受容体作動薬における心血管および腎アウトカムへの影響に関する臨床成績が続々と発表されました。
これらのエビデンスにより、世界の2型糖尿病の治療戦略は、HbA1cの改善に加えて、心血管および腎アウトカムへの影響を考慮した薬剤選択を行うという方向に舵が切られました2)。日本においても、現在、血糖降下薬の選択は、安全性および糖尿病の併存症(動脈硬化性心血管疾患、心不全、慢性腎臓病など)に対する有用性、患者背景を総合的に勘案することが推奨されています3)。
2) Mosenzon O, et al.: Cardiovasc Diabetol. 2021; 20(1): 92.
3) 日本糖尿病学会 編・著. 糖尿病診療ガイドライン2024. 南江堂. 2024, p86.
SGLT2阻害薬の心血管および腎アウトカムの一つとして、
2015年に発表されたEMPA-REG OUTCOME®をご紹介します。
2015年発表、2型糖尿病のある方の
心血管および腎アウトカムへの影響を示したEMPA-REG OUTCOME®
EMPA-REG OUTCOME®では、心血管イベントのリスクを有する2型糖尿病のある方を対象とし、標準治療にジャディアンスを上乗せした場合の影響を検討しました。

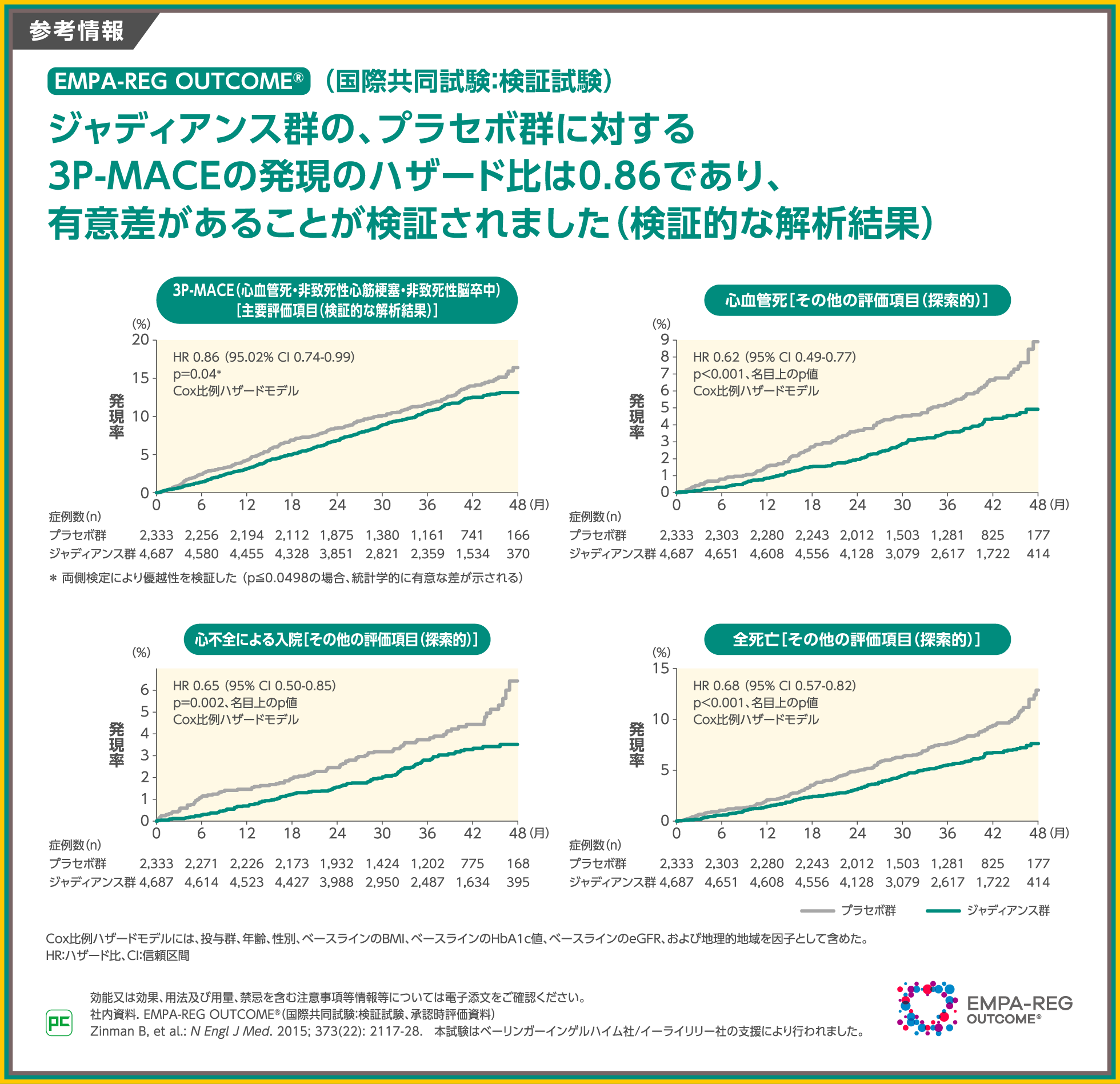
【参考情報】
主要評価項目であるジャディアンス群の3P-MACE(心血管死、非致死性心筋梗塞、非致死性脳卒中)の発現のハザード比は0.86であり、有意差があることが検証されました(vs. プラセボ、p=0.04、Cox比例ハザードモデル)。
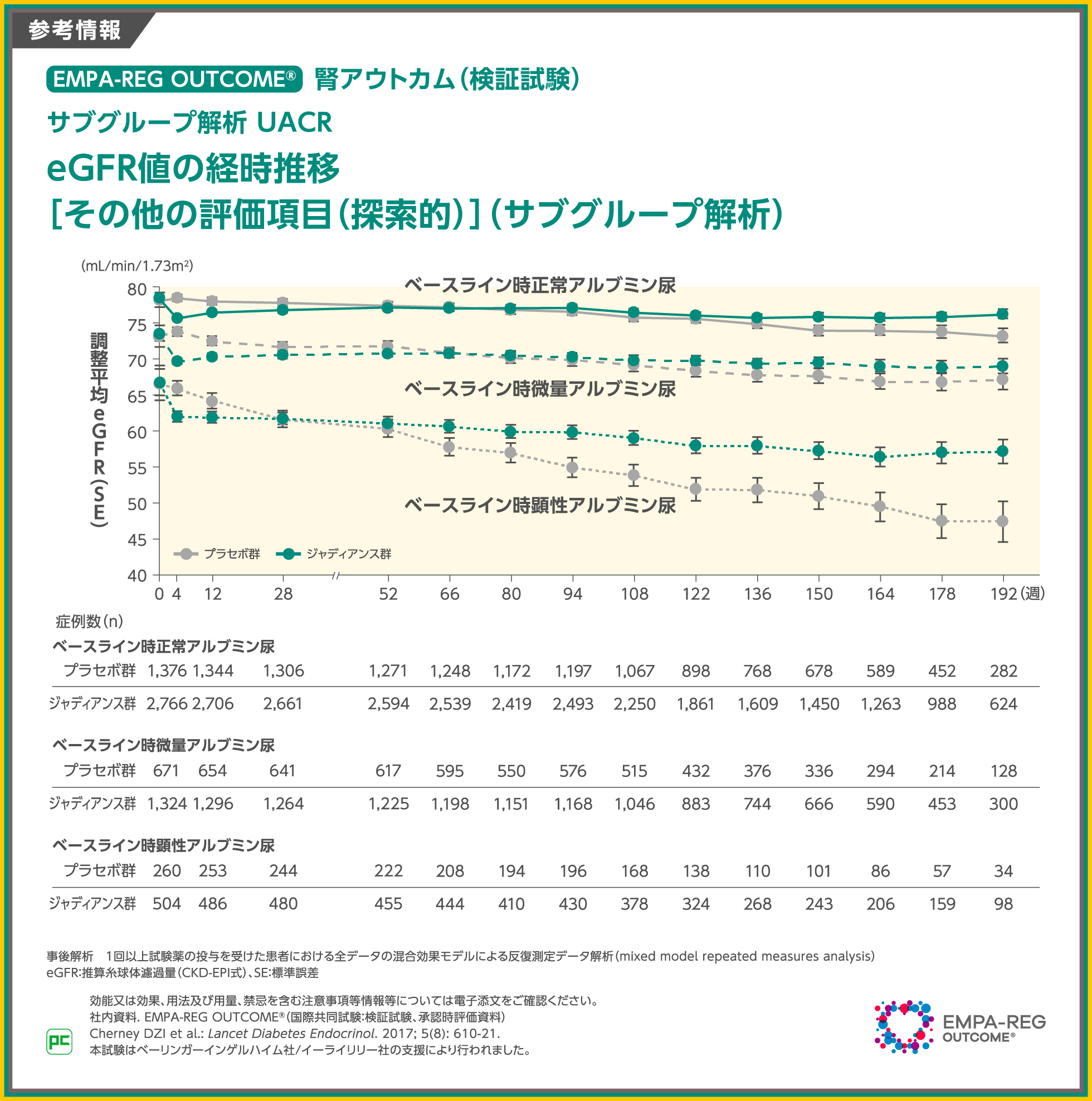
【参考情報】
また、事前規定されたUACR別のサブグループ解析において、正常アルブミン尿群、微量アルブミン尿群、顕性アルブミン尿群それぞれにおけるeGFR値は経時的に図のように推移しました。
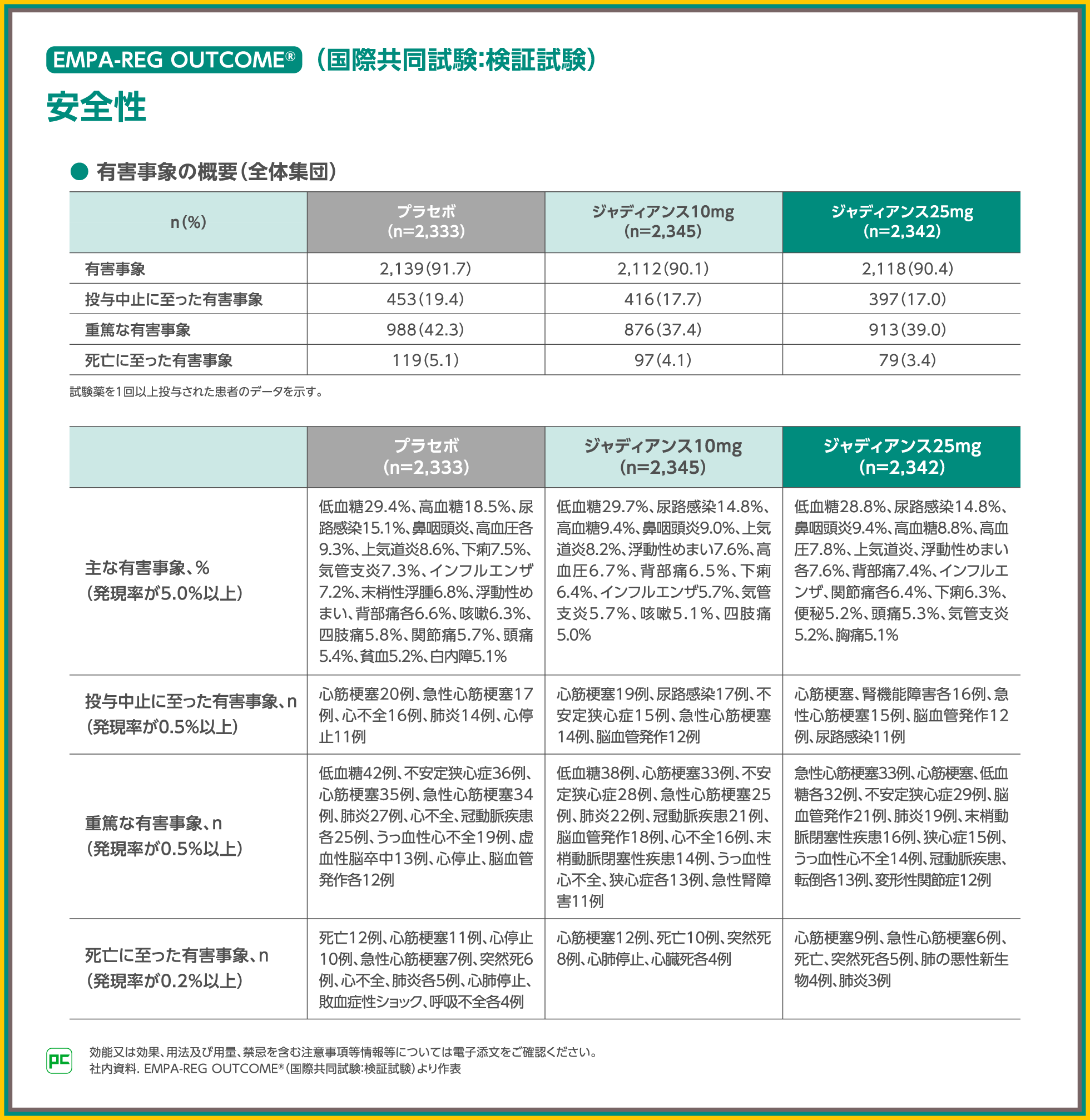
EMPA-REG OUTCOME®における有害事象の発現率は、ジャディアンス10mg群で90.1%、25mg群で90.4%でした。
主な有害事象は、ジャディアンス10mg群で低血糖29.7%、尿路感染14.8%、高血糖9.4%等、25mg群で低血糖28.8%、尿路感染14.8%、鼻咽頭炎9.4%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で低血糖38例、心筋梗塞33例、不安定狭心症28例等、25mg群で急性心筋梗塞33例、心筋梗塞、低血糖各32例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
2型糖尿病治療の薬剤選択の際に心血管および腎アウトカムを考慮する点は、
日本においても重視され、2022年に初版が公開された
『2型糖尿病の薬物療法のアルゴリズム』にも記載されています4)。
加えて、日本には、日本独自の2型糖尿病治療の課題があります。
4) 日本糖尿病学会コンセンサスステートメント策定に関する委員会. 糖尿病. 2023; 66(10): 715-33.
日本では、2型糖尿病のある高齢者への対策も課題に
超高齢化社会を迎えた日本では、2015年に高齢者糖尿病の治療向上のための日本糖尿病学会と日本老年医学会の合同委員会が設置され、2017年に『高齢者糖尿病診療ガイドライン2017』が公開されました5)。
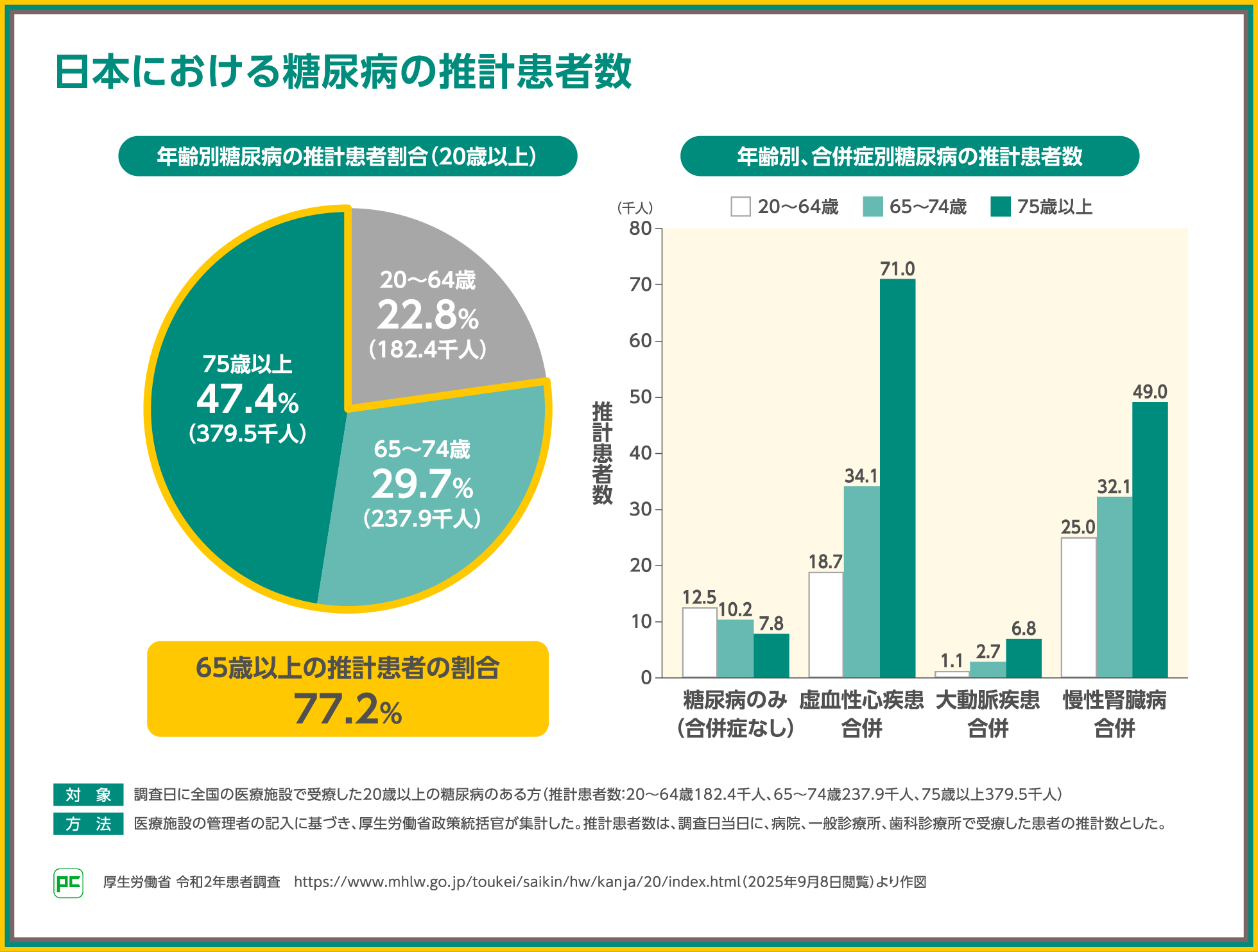
2020年の患者調査では、糖尿病のある方のうち77.2%は65歳以上の高齢者であることが報告されました。また、同調査では年齢が上がるほど虚血性心疾患や慢性腎臓病を併発する患者さんが増加することも示されており、高齢者への対応は、日本における糖尿病治療の課題の一つとなっています。
5) 日本老年医学会・日本糖尿病学会編・著: 高齢者糖尿病診療ガイドライン2017. 南江堂, 2017.
続けて、日本の臨床課題である65歳以上の2型糖尿病のある方を対象として実施した
EMPA-ELDERLY試験をご紹介します。
2023年
日本人の2型糖尿病のある高齢者を対象としたEMPA-ELDERLY試験
2023年、日本人の2型糖尿病のある高齢者を対象に、ジャディアンス10mgの長期投与による血糖降下作用と安全性を検討したEMPA-ELDERLY試験を発表しました。

日本人の65歳以上で2型糖尿病のある方129例を対象に、ジャディアンス10mgを1日1回52週間経口投与した結果、プラセボと比較して有意なHbA1c低下作用が認められました(p<0.0001、名目上のp値、MMRM)。
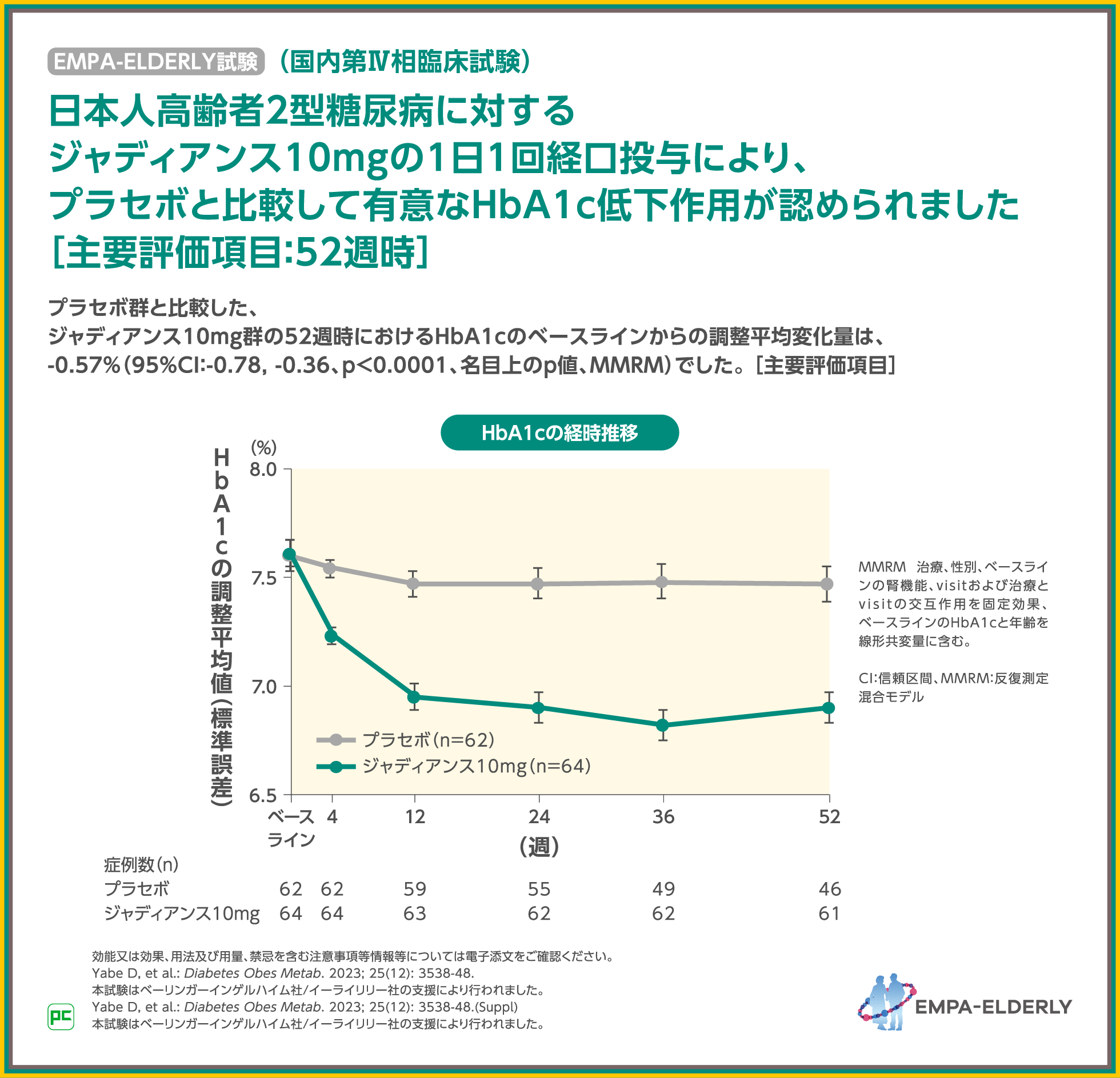
【参考情報】
また、52週時における体重、体組成、握力等の変化は、図のとおりでした。
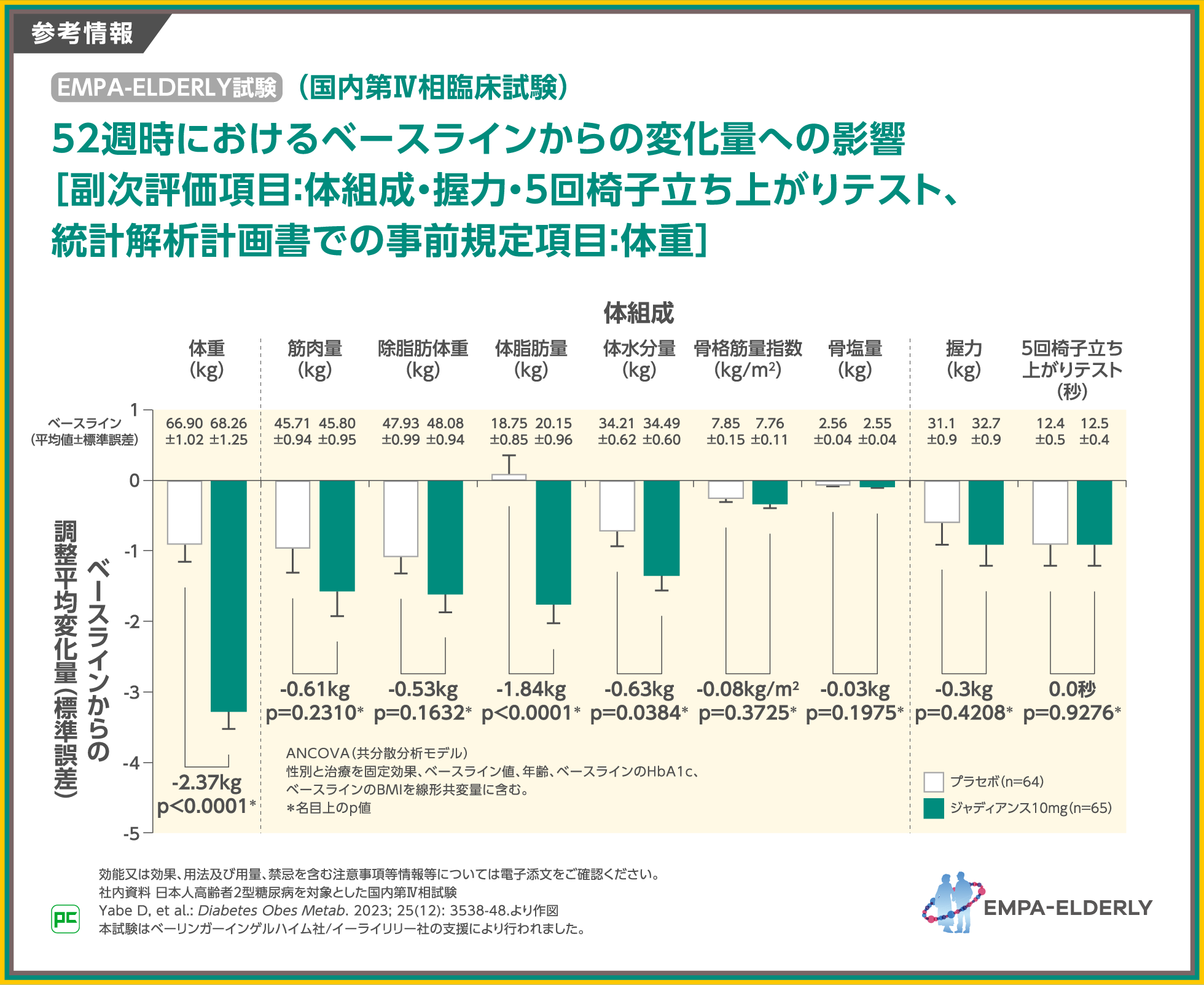
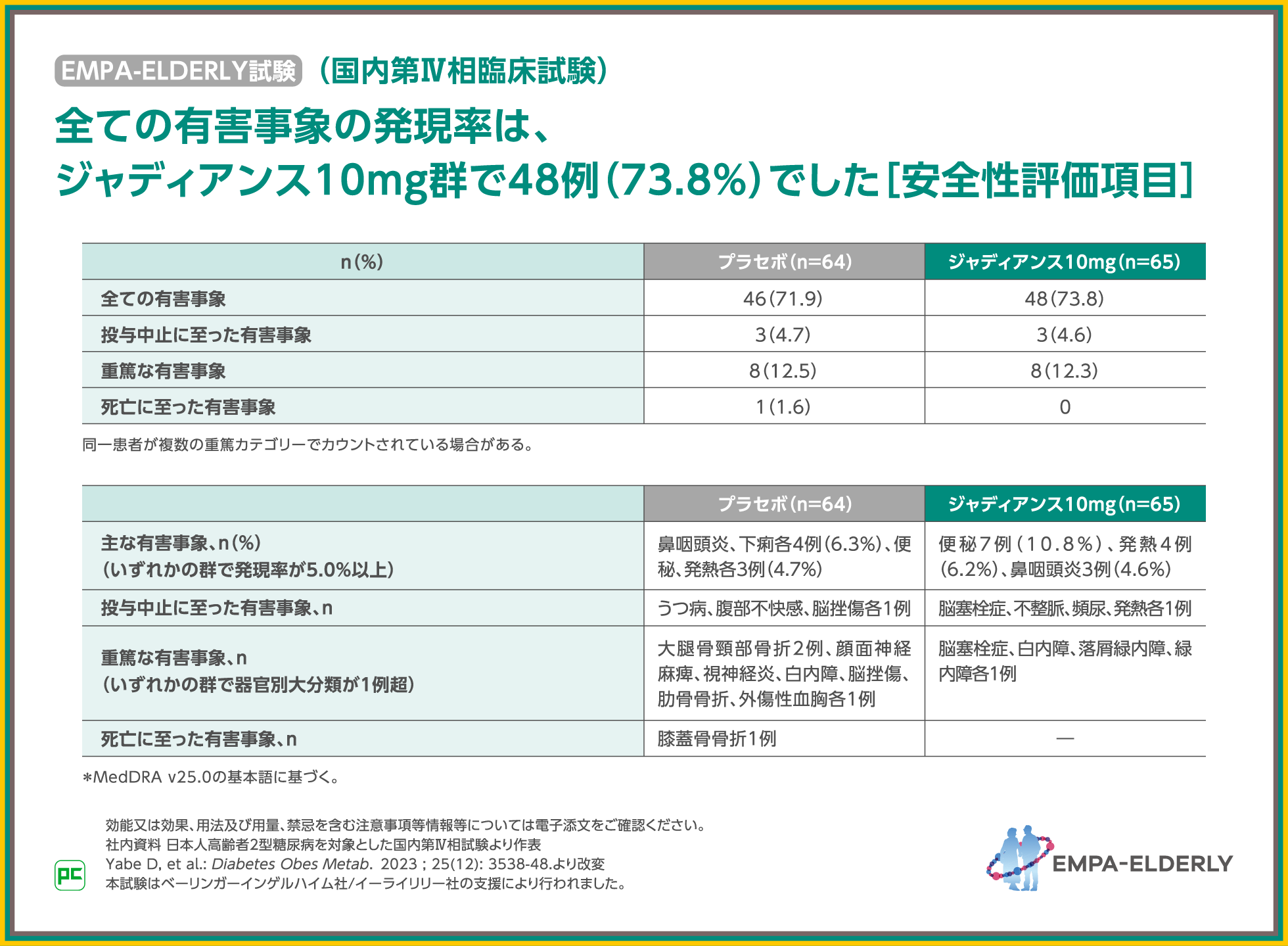
EMPA-ELDERLY試験における有害事象の発現率は、ジャディアンス10mg群で73.8%でした。
主な有害事象は、ジャディアンス10mg群で便秘10.8%、発熱6.2%、鼻咽頭炎4.6%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で脳塞栓症、白内障、落屑緑内障、緑内障各1例でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
ジャディアンスは、日本の2型糖尿病治療の臨床課題に向き合った臨床試験の実施と並行して、
EMPA-REG OUTCOME®で得られた心血管および腎アウトカムを発展させて慢性心不全や慢性腎臓病を対象とした臨床試験を行い、エビデンスを構築しました5)。
5) EMPA-KIDNEY Collaborative Group. Nephrol Dial Transplant. 2022; 37(7): 1317-29.
2024年
近年、心不全や慢性腎臓病の治療薬として注目されるSGLT2阻害薬
2015年以降、SGLT2阻害薬の腎アウトカムに対する影響を示すエビデンスが報告されたことから、SGLT2阻害薬は心不全や慢性腎臓病の治療薬としても注目されています。
日本糖尿病学会の『2型糖尿病の薬物療法のアルゴリズム』では、薬剤選択のStep 3「Additional benefitsを考慮すべき併存疾患」に慢性腎臓病、心不全、心血管疾患を設定しました。SGLT2阻害薬は、3つの疾患全てで候補として記載されました4)
また、現在、『CKD診療ガイド2024』に掲載されている「CKD治療におけるSGLT2阻害薬の適正使⽤に関するrecommendation」では、糖尿病を併発する慢性腎臓病に対して、アルブミン尿の有無にかかわらずeGFR 15mL/min/1.73m2以上でクリニカルエビデンスを有するSGLT2阻害薬を開始することとされています。
2型糖尿病治療薬として開発されたSGLT2阻害薬は、複数の臨床試験で構築されたエビデンスを受けて、慢性心不全治療薬、慢性腎臓病治療薬として、国内のガイドラインに掲載されています6,7)。
4) 日本糖尿病学会コンセンサスステートメント策定に関する委員会. 糖尿病. 2023; 66(10): 715-33.
6) 日本循環器学会/日本心不全学会. 2021年 JCS/JHFS ガイドライン フォーカスアップデート版 急性・慢性心不全診療. p16-20.
7) 日本腎臓学会編. CKD診療ガイド2024. 東京医学社. 2024, p76.
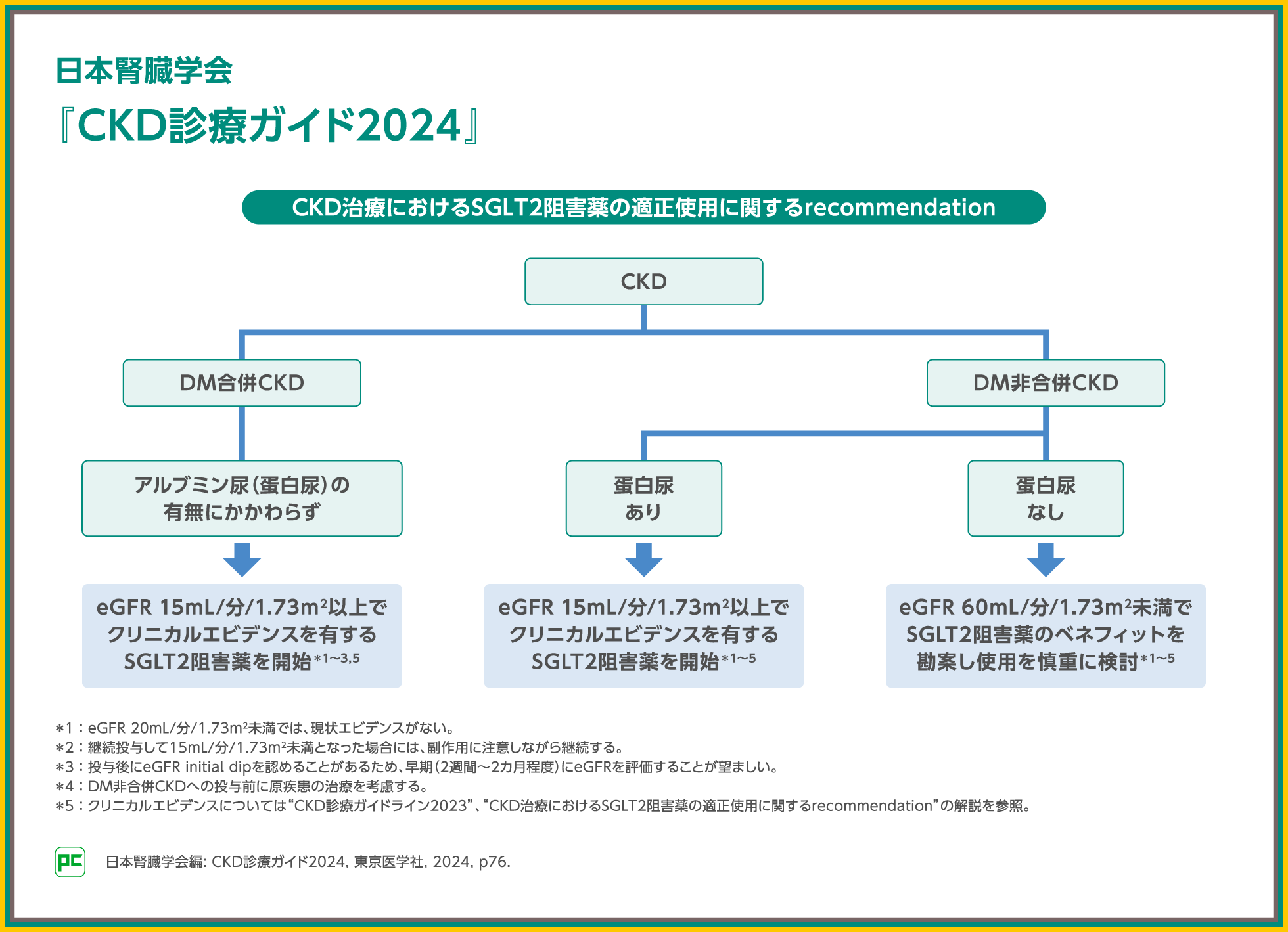
続けて、『エビデンスに基づくCKD診療ガイドライン2023』および『CKD診療ガイド2024』でエビデンスとして引用されたEMPA-KIDNEY試験についてご紹介します。
2024年
糖尿病合併の有無にかかわらず、慢性腎臓病患者を対象としたEMPA-KIDNEY試験
ジャディアンスは、EMPA-KIDNEY試験による慢性腎臓病患者に対する有効性が評価され、2024年2月に慢性腎臓病※1の効能又は効果の追加が承認されました。
EMPA-KIDNEY試験は、糖尿病合併の有無にかかわらず、腎疾患進行のリスクのある慢性腎臓病患者を対象に、ジャディアンス10mgを1日1回経口投与した時の有効性および安全性をプラセボと比較検討した試験です。
※1 ただし、末期腎不全又は透析施行中の患者を除く。

主要評価項目である腎疾患進行または心血管死のリスクは、全体集団において、27%低下し(HR=0.73、99.83%CI:0.59~0.89、p<0.0001、Cox回帰モデル)、ジャディアンス10mg群の優越性が検証されました。
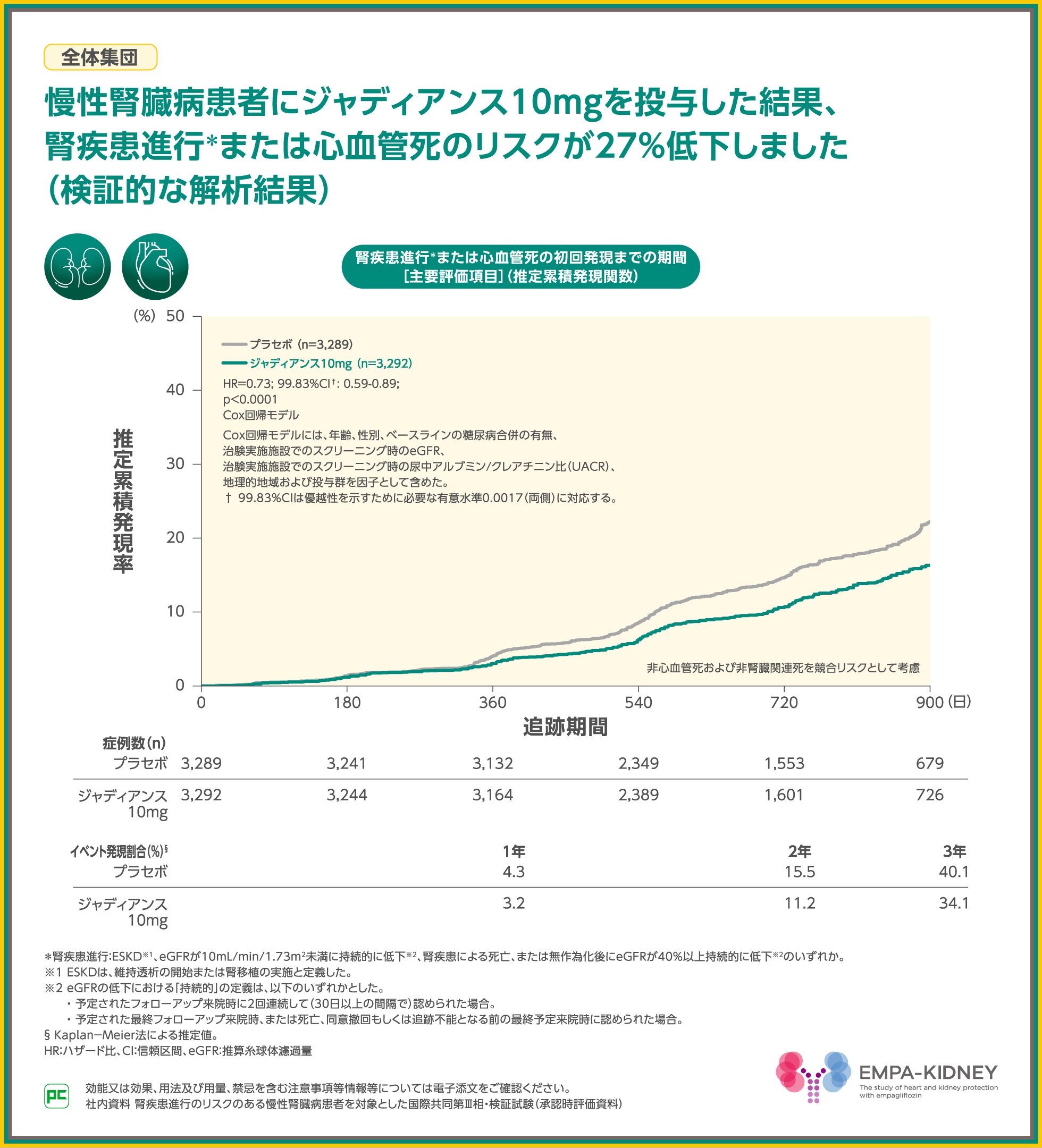
日本人集団解析では、主要評価項目について、56%のリスク低下が認められました(p=0.0004、名目上のp値、Cox回帰モデル)。
なお、日本人集団のRAS阻害薬使用群において、プラセボ群と比較したジャディアンス10mg群のハザード比は0.44でした。

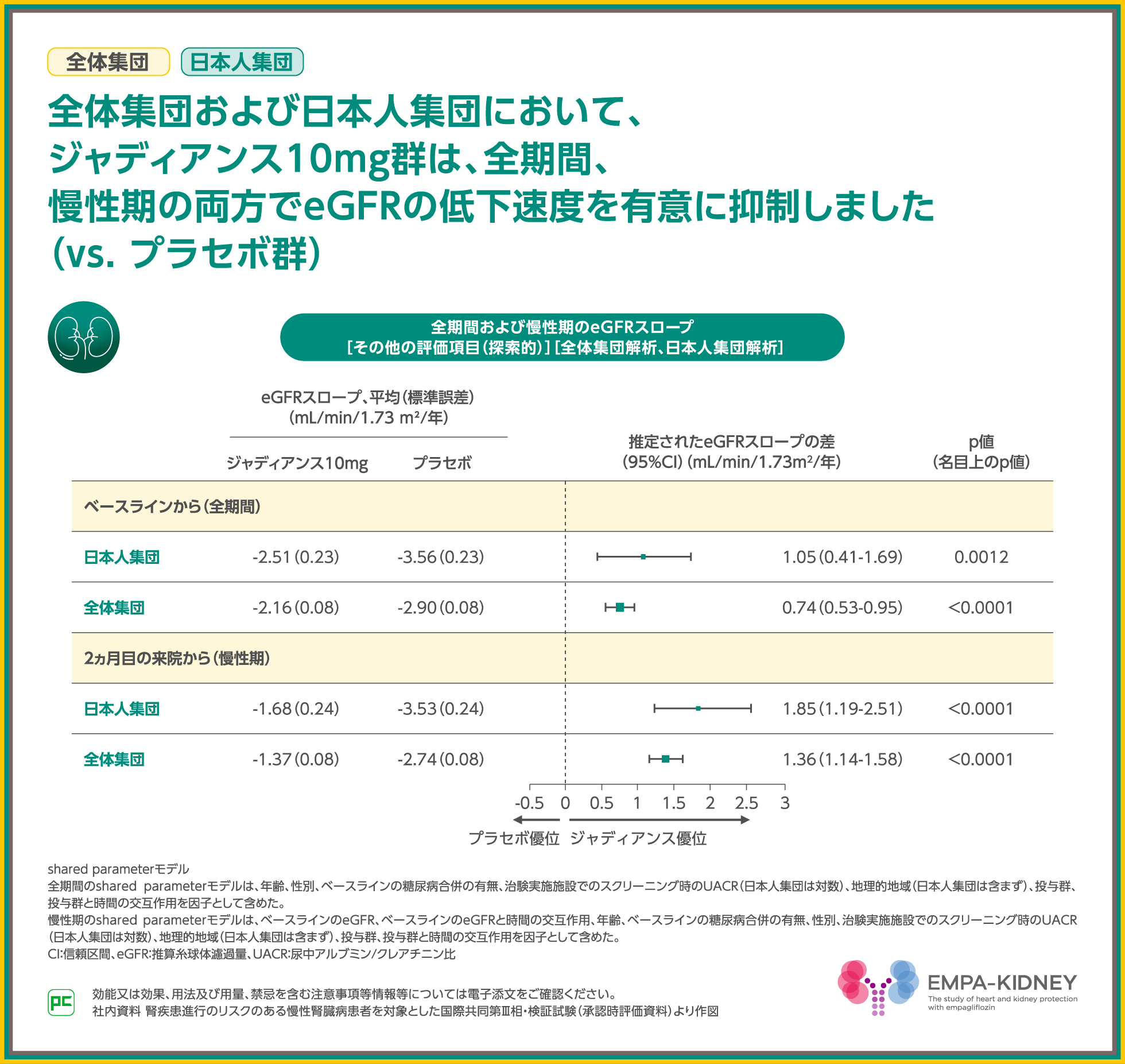
全体集団および日本人集団において、全期間、慢性期の両方で、ジャディアンス10mg群は、eGFRの低下速度を有意に抑制しました(vs. プラセボ群、全体集団の全期間・慢性期および日本人集団の慢性期:p<0.0001、日本人集団の全期間:p=0.0012、いずれも名目上のp値、shared parameterモデル)。
また、正常アルブミン尿(UACR<30mg/gCr)のジャディアンス10mg群は、正常アルブミン尿のプラセボ群と比較してeGFRスロープを0.78mL/min/ 1.73m2抑制し、UACRにかかわらず、ジャディアンス10mg群は、慢性期におけるeGFRの低下速度を有意に抑制したことが示されました(正常群:p=0.0008、微量および顕性アルブミン尿群:各p<0.0001、いずれも名目上のp値、shared parameterモデル)。
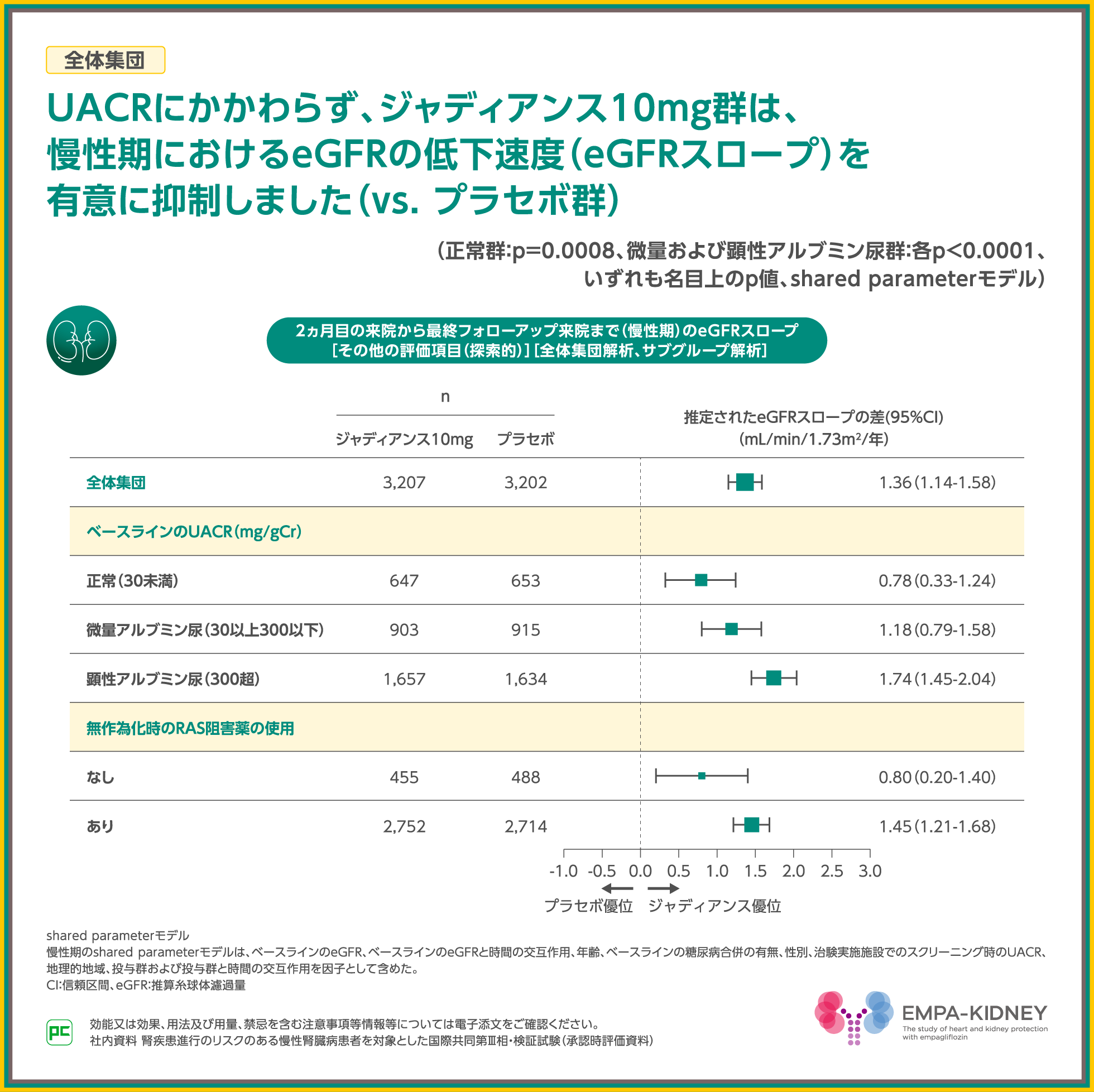
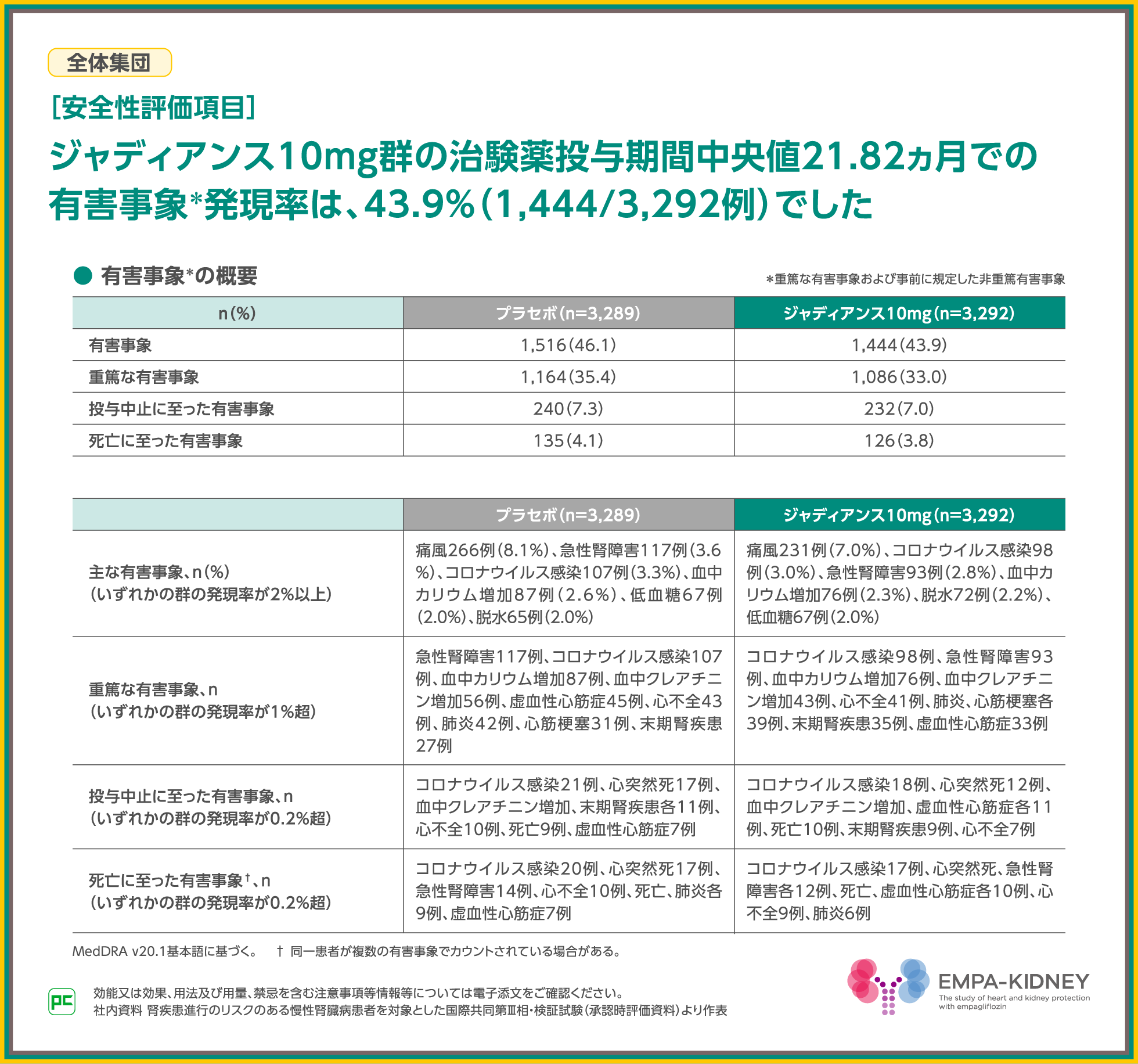
EMPA-KIDNEY試験において、事前に規定した非重篤有害事象および全ての重篤な有害事象に限定して有害事象を収集した結果、全体集団での発現率はジャディアンス10mg群で43.9%でした。
主な有害事象は、ジャディアンス10mg群で痛風7.0%、コロナウイルス感染3.0%、急性腎障害2.8%等でした。
また、重篤な有害事象は、ジャディアンス10mg群でコロナウイルス感染98例、急性腎障害93例、血中カリウム増加76例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
EMPA-KIDNEY試験における日本人集団での発現率はジャディアンス10mg群で37.7%でした。
主な有害事象は、ジャディアンス10mg群で低血糖3.1%、白内障手術2.7%、脱水2.1%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で白内障手術8例、末期腎疾患5例、動静脈シャント手術4例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。

2025年
ジャディアンスは、10年間で血糖管理・心保護・腎保護の3領域にまたがるエビデンスを構築しました
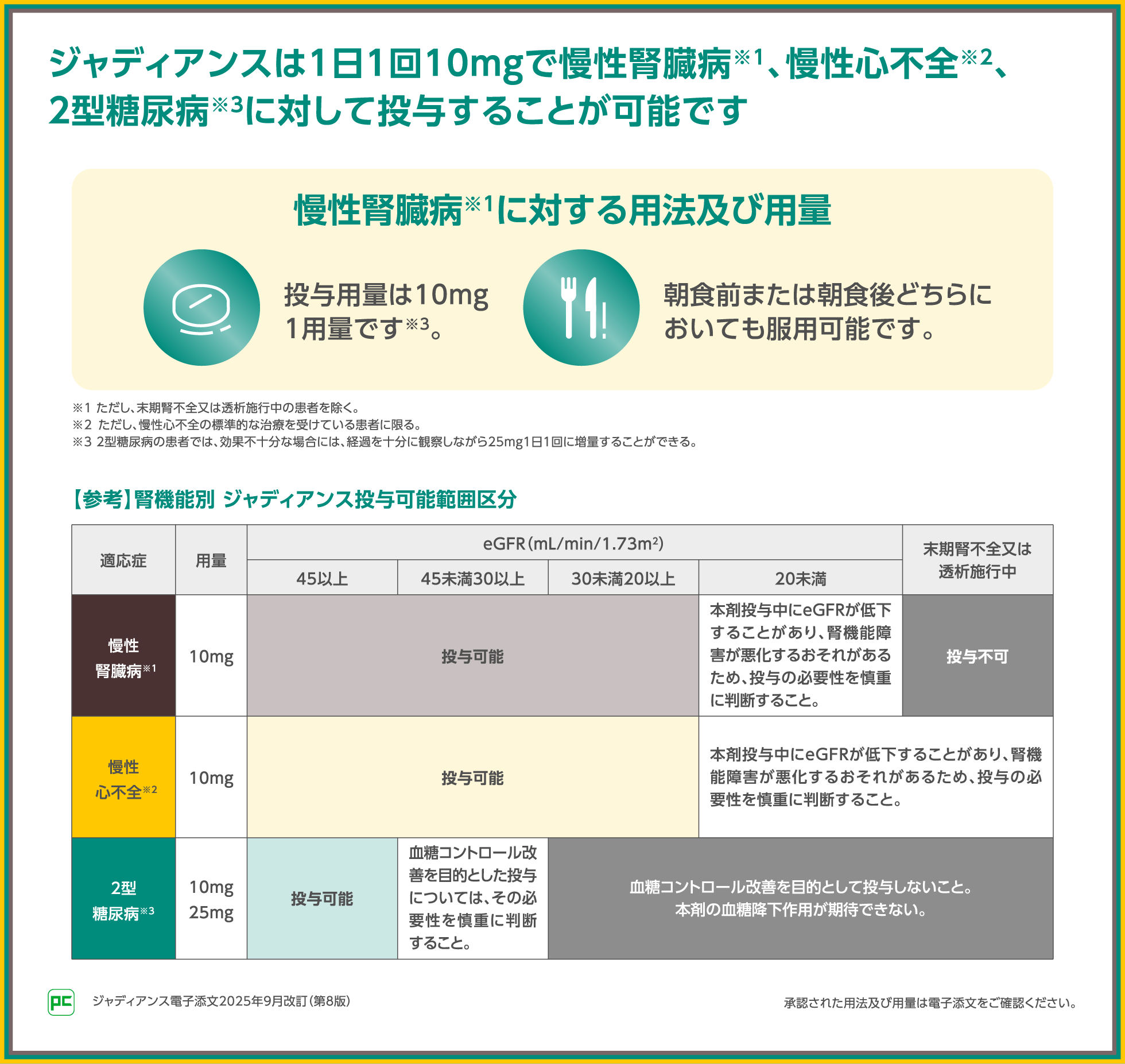
ジャディアンスは、2型糖尿病、慢性腎臓病※1、慢性心不全※2の3つの疾患に対する適応を有しています。
慢性腎臓病※1、慢性心不全※2に対しては、1日1回10mg、2型糖尿病に対しては1日1回10mgまたは25mgの用量が設定されており、2型糖尿病に対しては治療強化が可能です。
※1 ただし、末期腎不全又は透析施行中の患者を除く。
※2 ただし、慢性心不全の標準的な治療を受けている患者に限る。
また、ジャディアンスは2015年以降の10年間で血糖管理、心保護、腎保護の3つの領域において、有効性や安全性を検討するための複数の臨床試験を実施し、エビデンスを構築してきました。
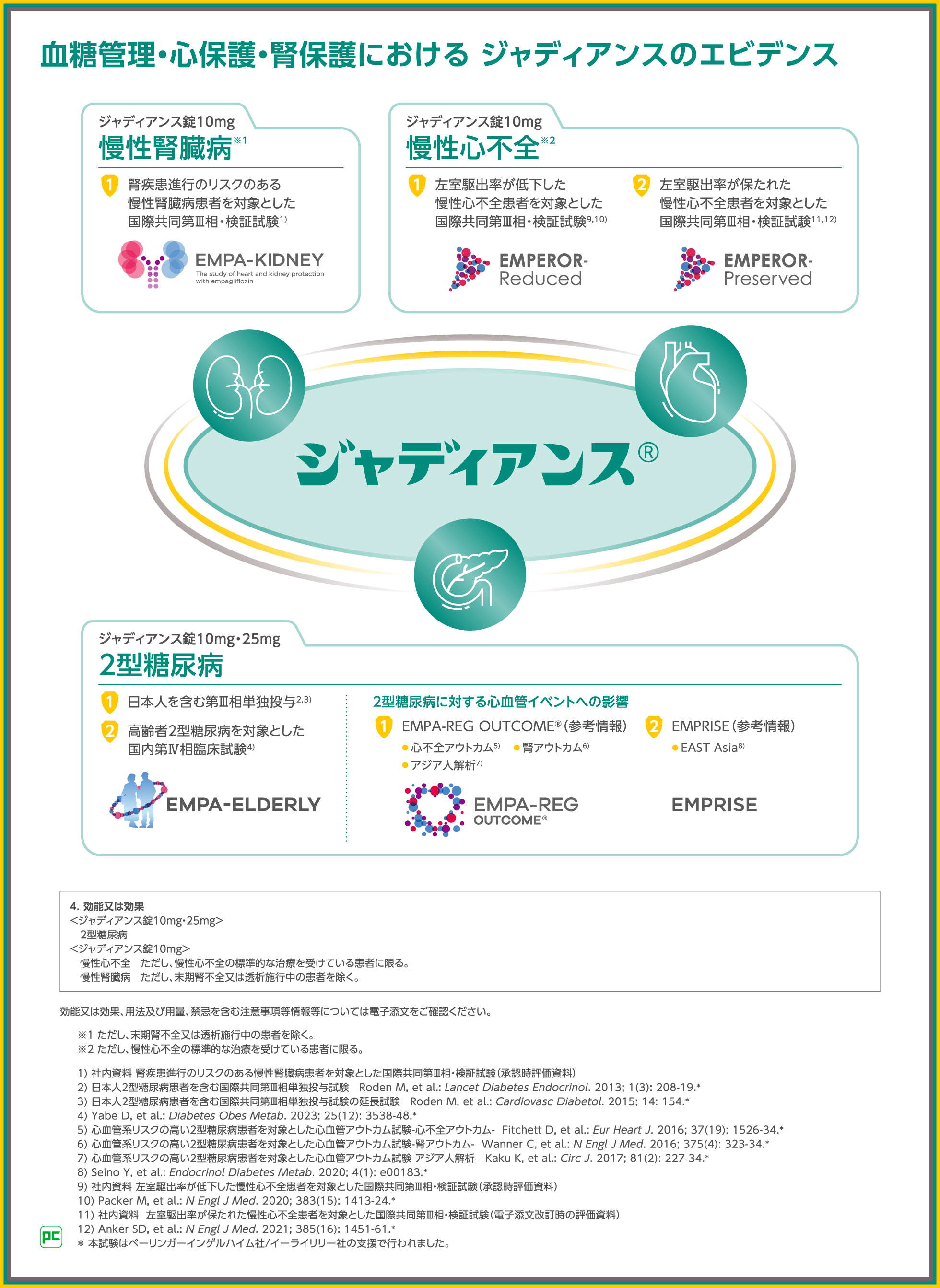
中でも、ジャディアンスの腎アウトカムへの影響を検討した2つの試験、EMPA-REG OUTCOME®とEMPA-
KIDNEY試験では、その両方で正常アルブミン尿を対象として組み入れることを事前規定しており、本コンテンツでもご紹介したとおり、両試験のサブグループ解析にて、正常アルブミン尿群、微量アルブミン尿群、顕性アルブミン尿群それぞれのエビデンスを有しています。
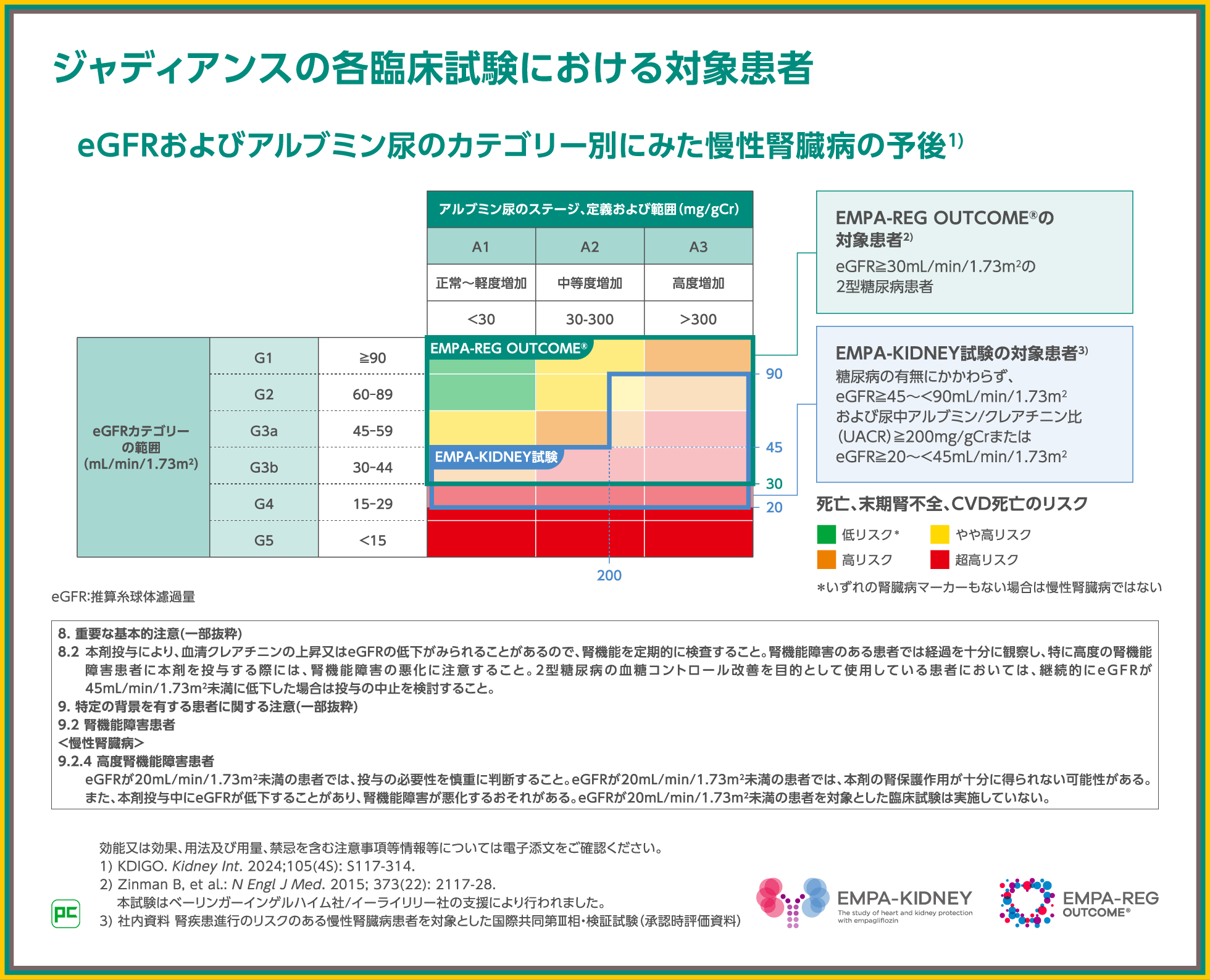
EMPA-REG OUTCOME®とEMPA-KIDNEY試験にて正常アルブミン尿を含めたエビデンスを持つジャディアンス10mgを、アルブミン尿の有無にかかわらず、慢性腎臓病を併発している2型糖尿病のある方の治療にお役立てください。

最後に、ジャディアンスの慢性心不全※2に対する効果として、2つの試験をご紹介します。
※2 ただし、慢性心不全の標準的な治療を受けている患者に限る。
2021年
左室駆出率が低下した(LVEF≦40%)慢性心不全患者に対する有効性を検証したEMPEROR-Reduced試験
ジャディアンスは、EMPEROR-Reduced試験が評価され、2021年11月に慢性心不全※2の効能又は効果の追加が承認されました。
LVEF≦40%の慢性心不全患者を対象としたEMPEROR-Reduced試験では、標準治療に加えてジャディアンス10mgを1日1回経口投与した時の有効性および安全性についてプラセボ群との比較検討を行いました。
※2 ただし、慢性心不全の標準的な治療を受けている患者に限る。

主要評価項目である心血管死または心不全による入院の初回発現までの期間のプラセボ群に対するジャディアンス10mg群のハザード比は0.75(95.04%CI:0.65~0.86)、p<0.0001(Cox比例ハザード回帰モデル)であり、ジャディアンス10mg群の優越性が検証されました。
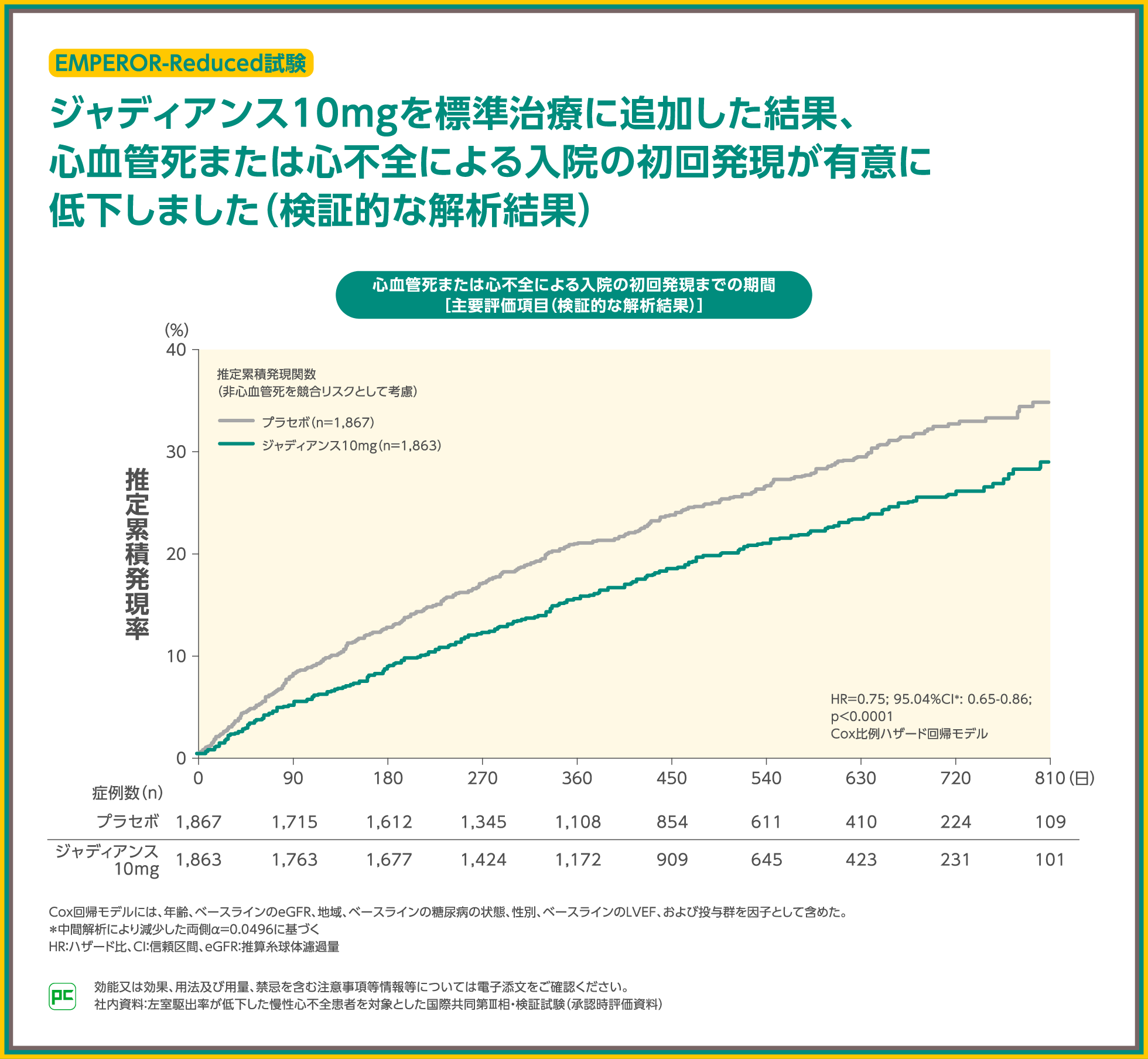
EMPEROR-Reduced試験における有害事象の発現率はジャディアンス10mg群で76.2%でした。
主な有害事象は、ジャディアンス10mg群で心不全17.8%、低血圧7.0%、腎機能障害5.6%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で心不全332例、心室性頻脈55例、肺炎53例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。

慢性心不全※2の適応追加から5ヵ月後、ジャディアンスは、
左室駆出率が保たれた慢性心不全への有効性が評価されました。
※2 ただし、慢性心不全の標準的な治療を受けている患者に限る。
2022年
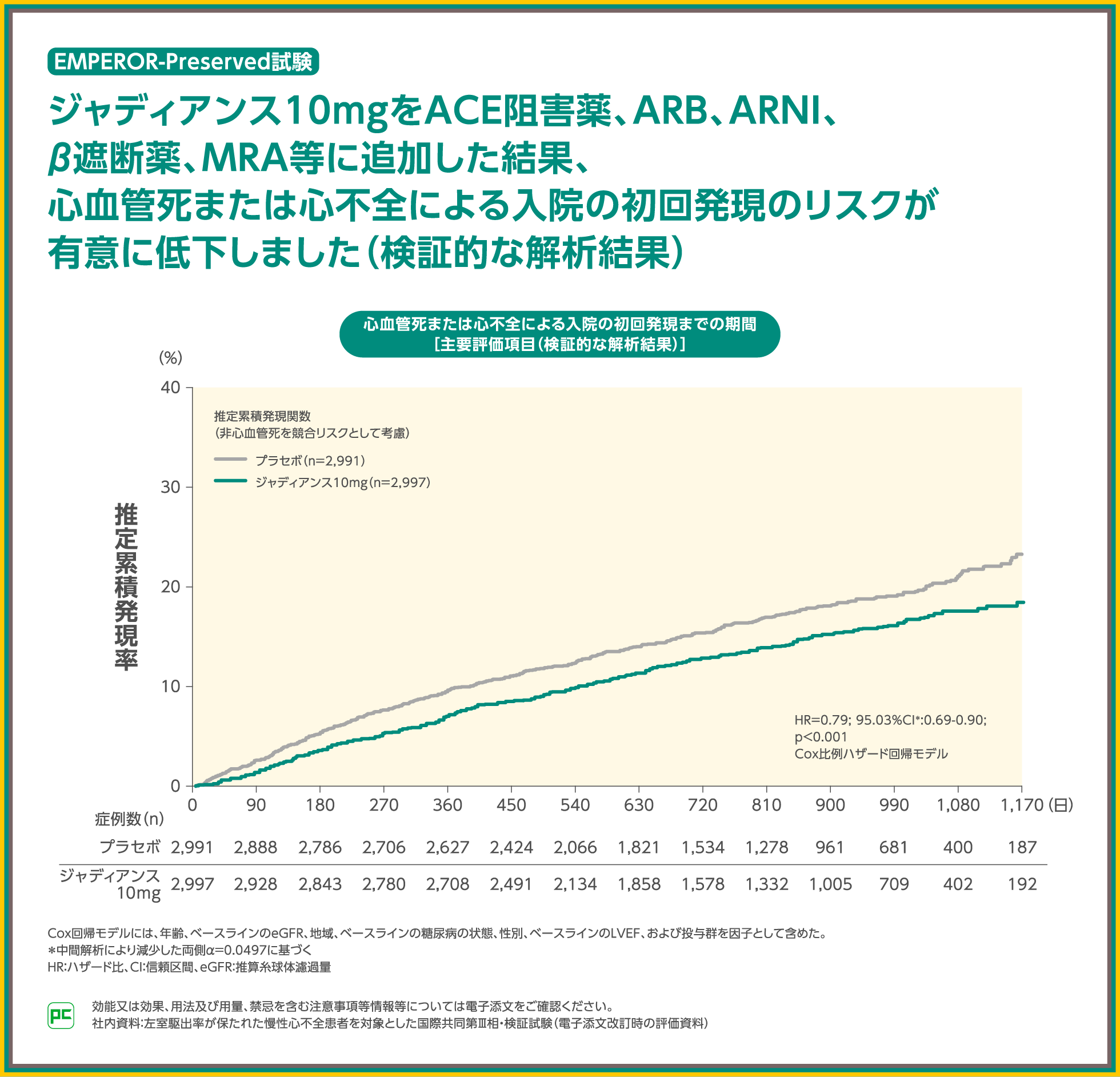
左室駆出率が保たれた(LVEF>40%)慢性心不全患者に対する有効性を検証したEMPEROR-Preserved試験
2022年4月には、EMPEROR-Preserved試験による左室駆出率が保たれた慢性心不全への有効性が評価され、電子添文の改訂が行われました。
LVEF>40%の慢性心不全患者を対象としたEMPEROR-Preserved試験では、ACE阻害薬、ARB、ARNI、β遮断薬、MRA等に追加してジャディアンス10mgを1日1回経口投与した時の有効性および安全性についてプラセボ群との比較検討を行いました。

主要評価項目である心血管死または心不全による入院の初回発現までの期間のプラセボ群に対するジャディアンス10mg群のハザード比は0.79(95.03%CI:0.69~0.90)、p<0.001(Cox比例ハザード回帰モデル)であり、ジャディアンス10mg群の優越性が検証されました。
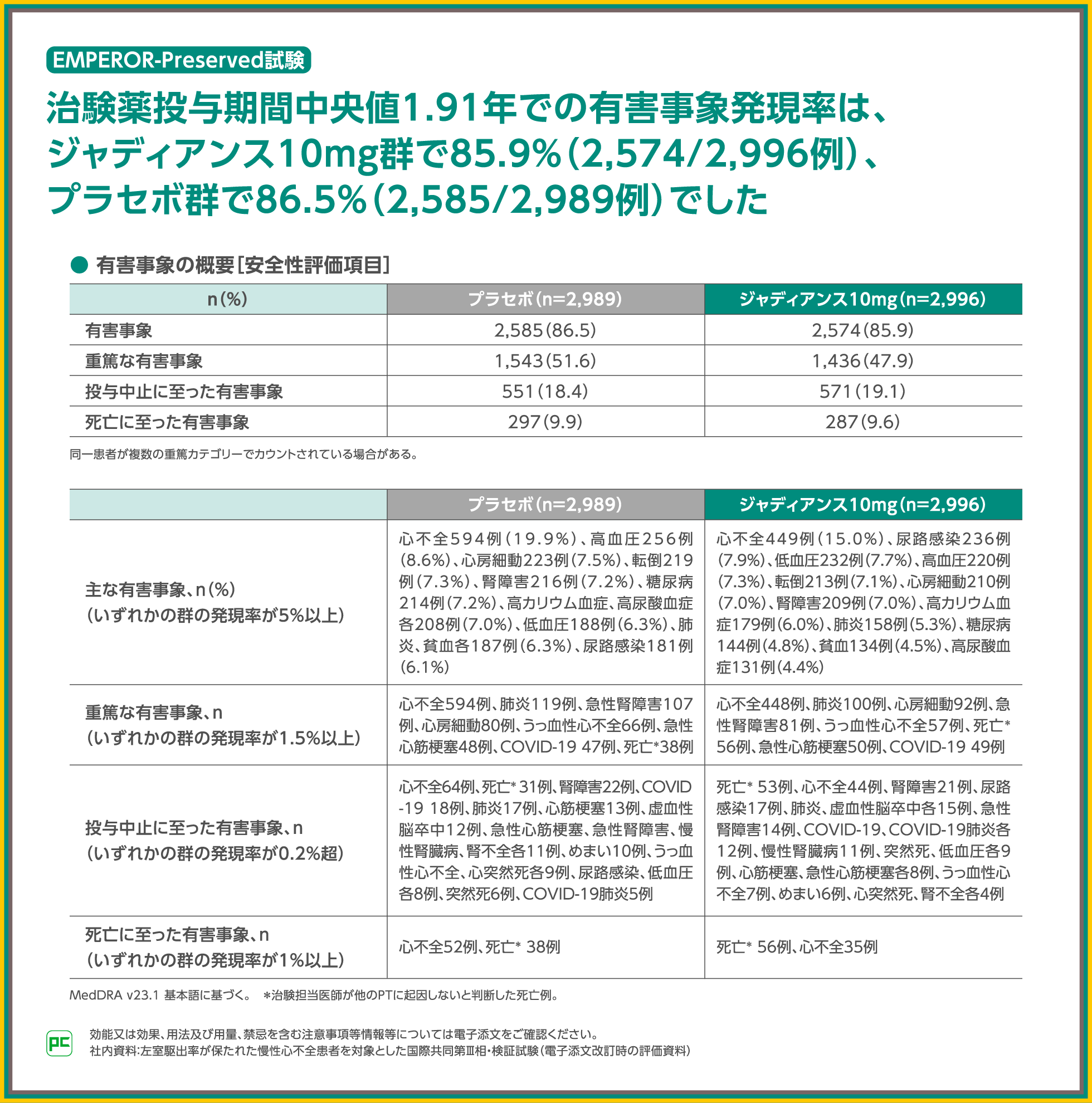
EMPEROR-Preserved試験における有害事象の発現率はジャディアンス10mg群で85.9%でした。
主な有害事象は、ジャディアンス10mg群で心不全15.0%、尿路感染7.9%、低血圧7.7%等でした。
また、重篤な有害事象は、ジャディアンス10mg群で心不全448例、肺炎100例、心房細動92例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
2015年の国内発売から10年の間に構築されたジャディアンスのエビデンスを心腎代謝疾患の治療戦略とともにご紹介しました。
ジャディアンスを、日常診療でお役立てください。
その他の関連情報


eGFR計算ツール・eGFRスロープ計算ツール・CKDイベントリスクシミュレーションツール
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



