CTD-ILDコンセンサスステートメント 疾患別管理アルゴリズム(静止画)
サイトへ公開:2024年07月17日 (水)
クイックリンク
ご監修:坂東 政司先生(自治医科大学 内科学講座 呼吸器内科学部門 教授)

2024年、日本の本領域のエキスパートのコンセンサスに基づいた、全身性強皮症に伴う間質性肺疾患(SSc-ILD)、関節リウマチに伴う間質性肺疾患(RA-ILD)、多発性筋炎/皮膚筋炎に伴う間質性肺疾患(PM/DM-ILD)の管理アルゴリズムが発表されました1)。
本アルゴリズムでは、日本国内の実臨床でより活用しやすいように、2023年に発表された包括的な膠原病に伴う間質性肺疾患(CTD-ILD)の管理アルゴリズム2)の内容が各疾患別に再整理されています。なお、本アルゴリズムの利用時の注意点として、日本の実臨床のエキスパートがデルファイ法※1で作成した点が挙げられています※2。
今回は、CTD-ILDコンセンサスステートメント 疾患別管理アルゴリズムについて紹介します。
※1 デルファイ法:アンケートやインタビューを繰り返すことで、専門家の意見を集約する技法3)。
※2 本アルゴリズムは日本国内の医師によって作成されたため、海外への一般化可能性はまだ検証されていない1)。
CTD-ILDコンセンサスステートメント 疾患別管理アルゴリズム
全体の構成
CTD-ILDコンセンサスステートメント 疾患別管理アルゴリズムでは、日本国内の日常臨床における実用性を考慮し、まず、「1. リスク因子」「2. スクリーニングツール」「3-1. 診断」「3-2. 重症度評価」「3-3 .進行リスク評価」の順に紹介されています。
次に、「SSc-ILD、RA-ILD、慢性PM/DM-ILD」と「急性/亜急性PM/DM-ILD」に分けて提示されています。
SSc-ILD、RA-ILD、慢性PM/DM-ILDについては、「4a. フォローアップとモニタリング」「5a .治療開始と治療が推奨される要因」「6a. 疾患進行」の順に紹介されています。一方で、急性/亜急性PM/DM-ILDについては、発症早期に治療介入が必要であることが考慮され、「4b. 治療開始と治療が推奨される要因」「5b. フォローアップとモニタリング」「6b. 疾患進行」の順に紹介されています(図1)。
図1
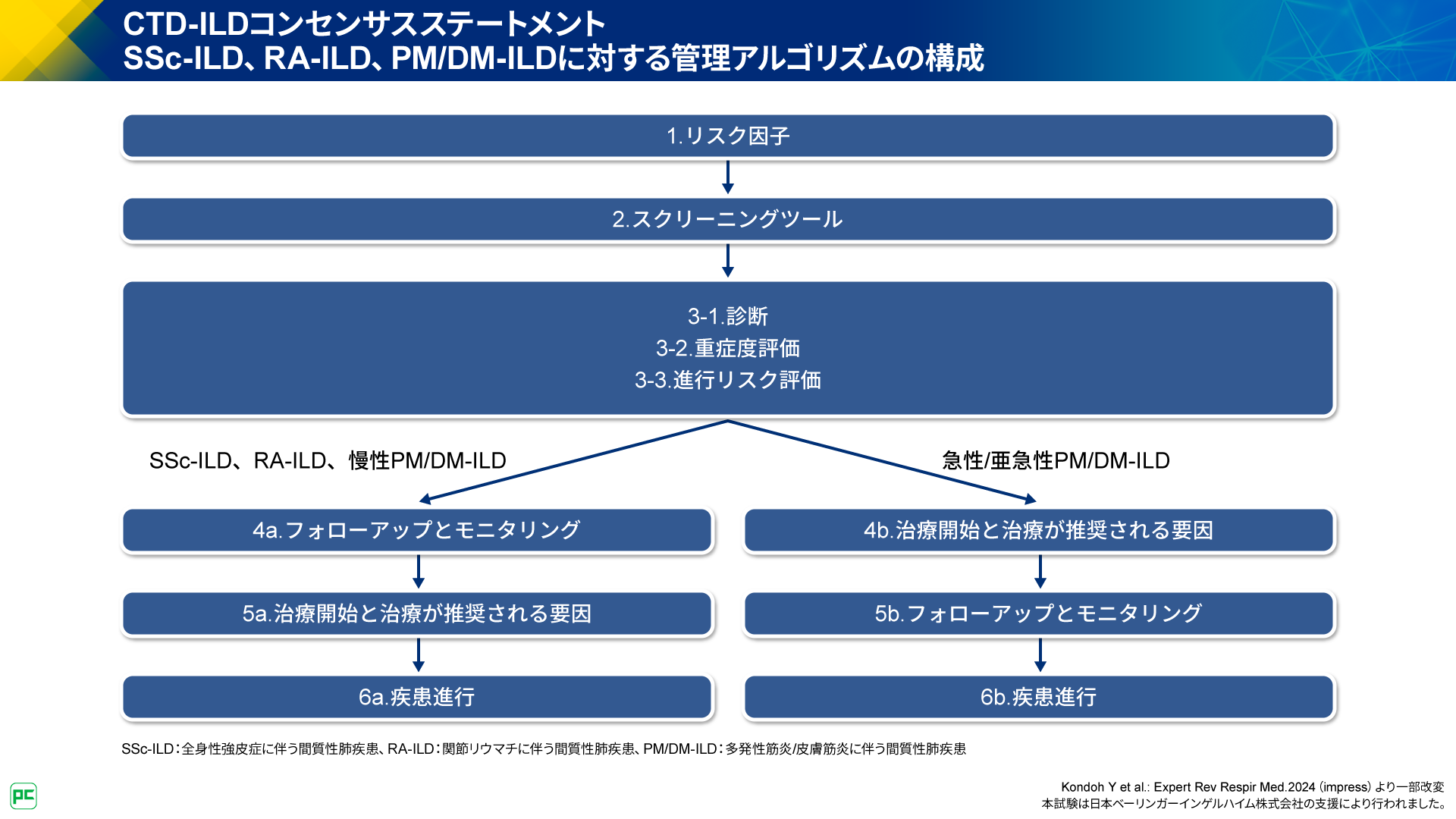
本アルゴリズムでは、SSc-ILD、RA-ILD、PM/DM-ILDの管理において共通する内容と疾患特異的な内容がまとめられています。
詳しくみていきましょう(図表内、各項目の★マークはコンセンサスレベル※3を示しています)。
※3 CTD-ILDコンセンサスステートメントの作成にあたっては、呼吸器科、リウマチ科、放射線科、病理科の専門医22名の日本人パネリストが参加する修正デルファイ法による検討が実施された。パネリストが回答した各コンセンサスステートメントに対する同意レベル(0[強く同意しない]~100[強く同意する])の平均値をコンセンサスレベルとした2)。
1. リスク因子
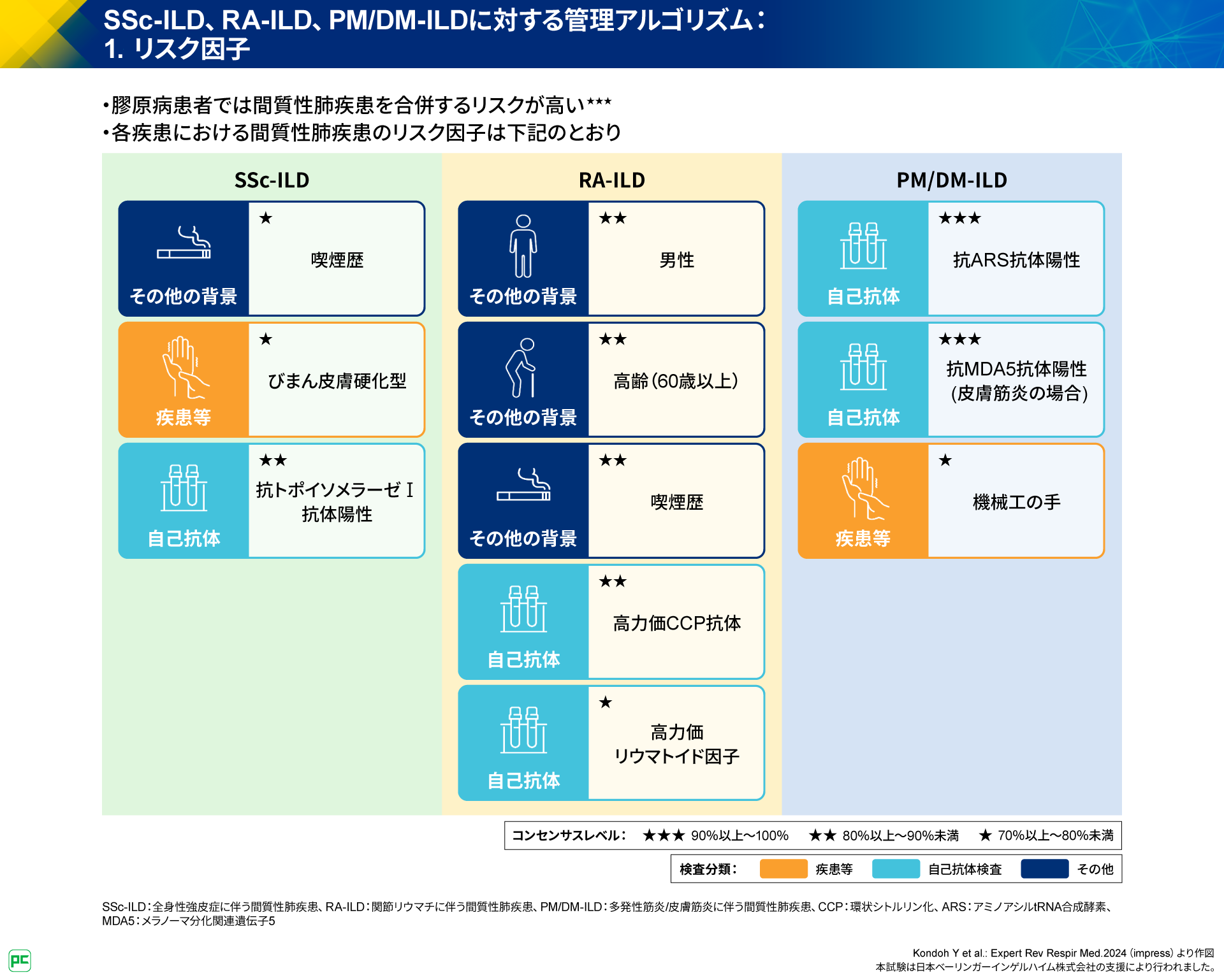
まず、膠原病に共通して間質性肺疾患(ILD)を合併するリスクが高いことが記載されています。
次に、SSc-ILD、RA-ILD、PM/DM-ILDの疾患別に、リスク因子が提示されています(図2)。
図2
2. スクリーニングツール
SSc-ILD、RA-ILD、PM/DM-ILDに共通するILDのスクリーニングツールとして、持続する呼吸器症状や胸部聴診、胸部X線検査、KL-6の測定、胸部高分解能CT(HRCT)検査が挙げられています(図3)。
KL-6:ケーエル6
図3

3-1. 診断
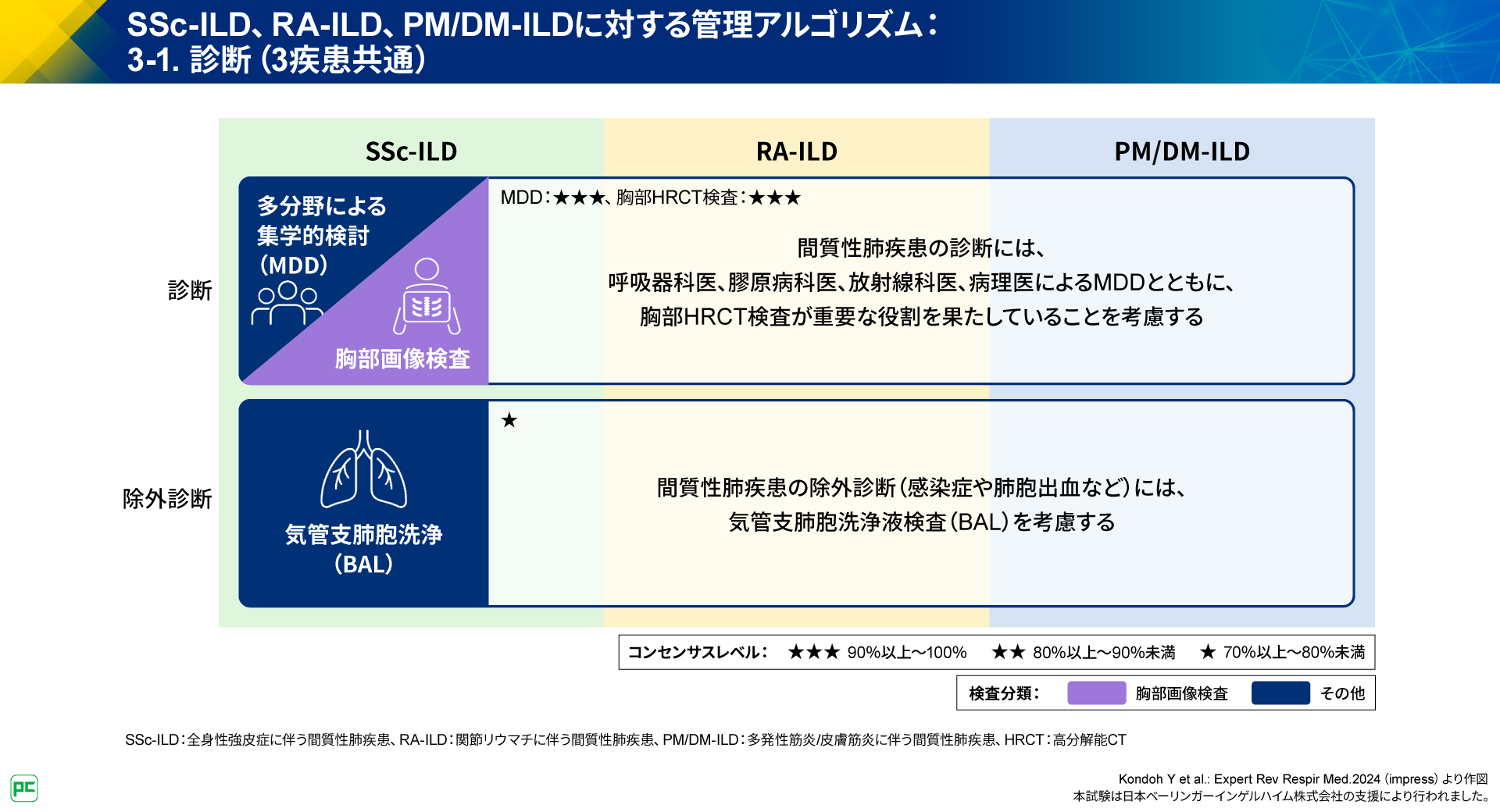
SSc-ILD、RA-ILD、PM/DM-ILDに共通して、診断に関して、「呼吸器科医、膠原病科医、放射線科医、病理医による多分野による集学的検討(MDD)とともに、胸部HRCT検査が重要な役割を果たしていることを考慮する」と記載されています。
また、ILDの除外診断として気管支肺胞洗浄液検査(BAL)を考慮することも記載されています(図4)。
図4
3-2. 重症度評価
SSc-ILD、RA-ILD、PM/DM-ILDに共通する重症度評価において有用な項目として、胸部HRCT検査とFVCの測定が挙げられています。
また、SSc-ILDではSADLモデル、RA-ILDでは胸部HRCT画像における網状影及び蜂巣肺スコアが重症度評価において有用な項目として挙げられています。PM/DM-ILDでは、抗MDA5抗体陽性の皮膚筋炎(DM)の場合に血清フェリチン値が重症度評価において有用な項目となることが挙げられています(図5)。
FVC:努力肺活量
SADL:smoking history(喫煙歴)・age(年齢)・ DLco (一酸化炭素肺拡散能)
MDA5:メラノーマ分化関連遺伝子5
図5
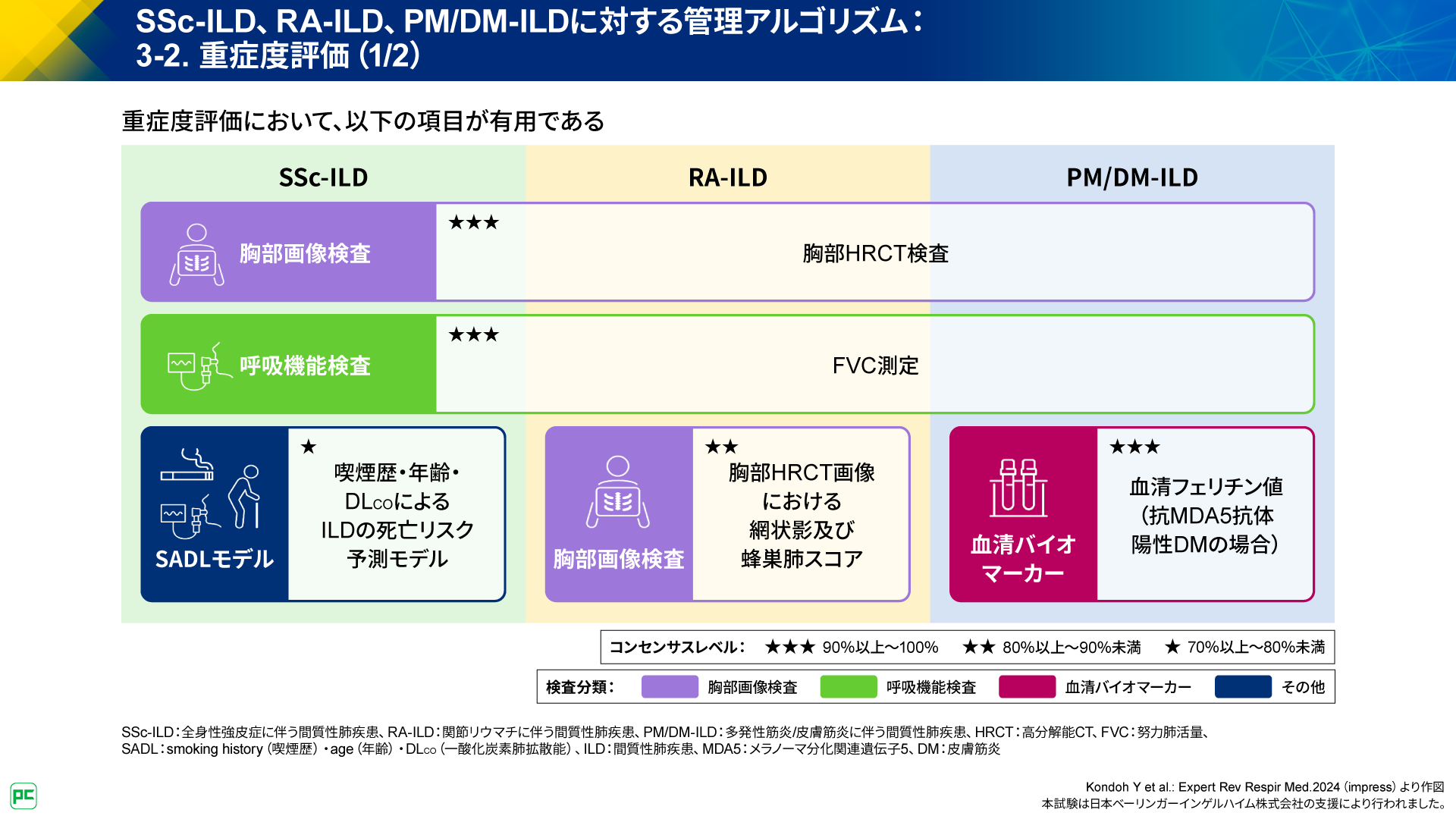
さらに、SSc-ILD、RA-ILD、PM/DM-ILDに共通する重症度評価において考慮すべき項目も挙げられています(図6)。
図6
3-3. 進行リスク評価
進行リスク評価に関しては疾患別に紹介されています。
<SSc-ILD>
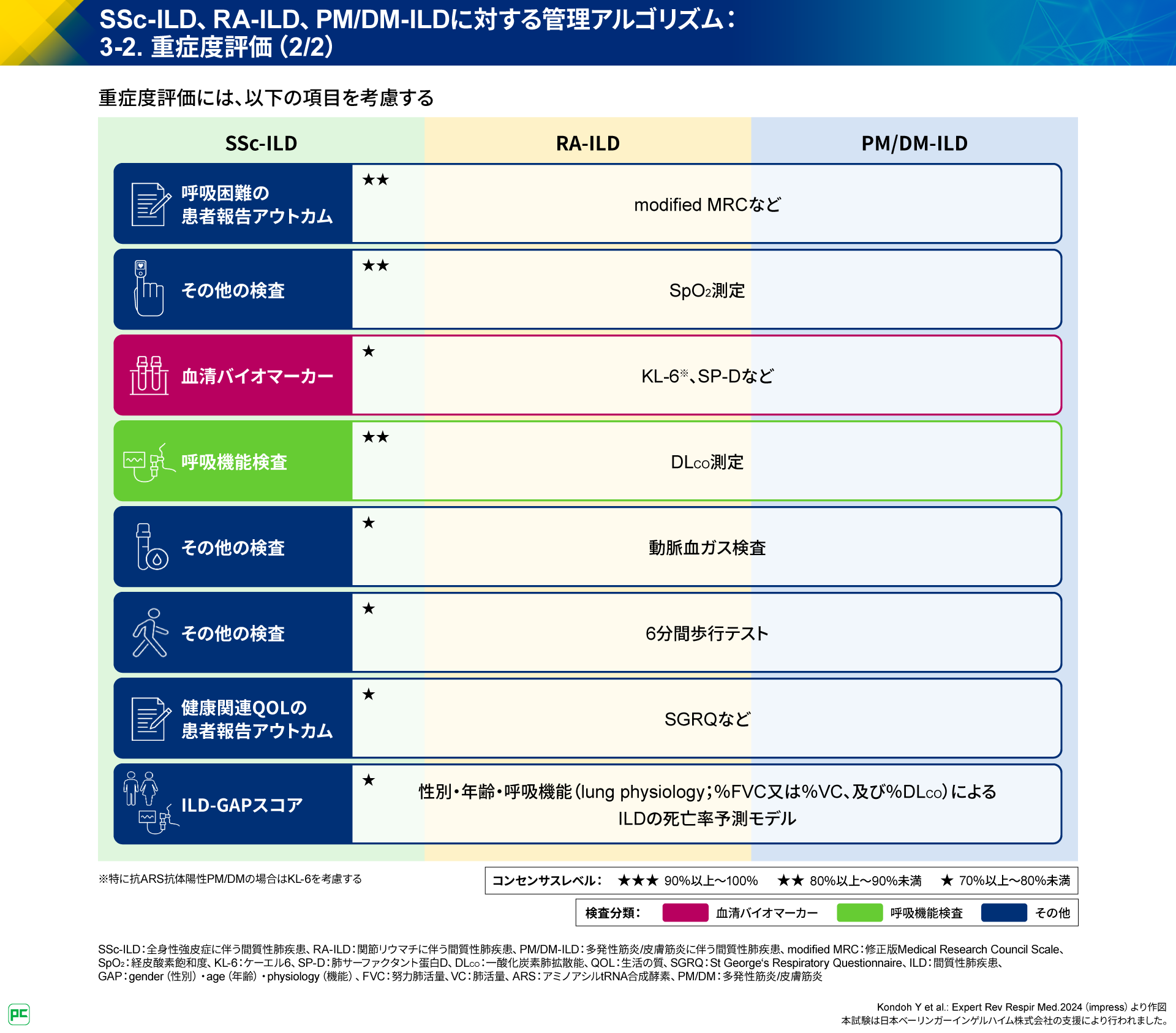
SSc-ILDでは、進行/予後不良を予測する項目として、血清KL-6高値、ベースライン胸部HRCT画像における病変の広がり、ベースラインDLcoの低下が挙げられています。
また、進行を予測する項目として、mRSS高値とSPARモデル、予後不良を予測する項目として、ベースラインFVCの低下、肺高血圧症、SADLモデルが挙げられています(図7)。
さらに、ILDの進行予測を示唆する因子として高齢、進行/予後不良の予測を示唆する因子として男性が提示されています(図7)。
DLco:一酸化炭素肺拡散能
mRSS:modified Rodnan total skin thickness score
SPAR:SpO2(経皮酸素飽和度)・arthritis(関節炎)
図7
<RA-ILD>
RA-ILDでは、胸部HRCT画像におけるUIPパターンが急性増悪及び予後不良を予測する因子として提示されています(図8)。
UIP:通常型間質性肺炎
図8

<PM/DM-ILD>
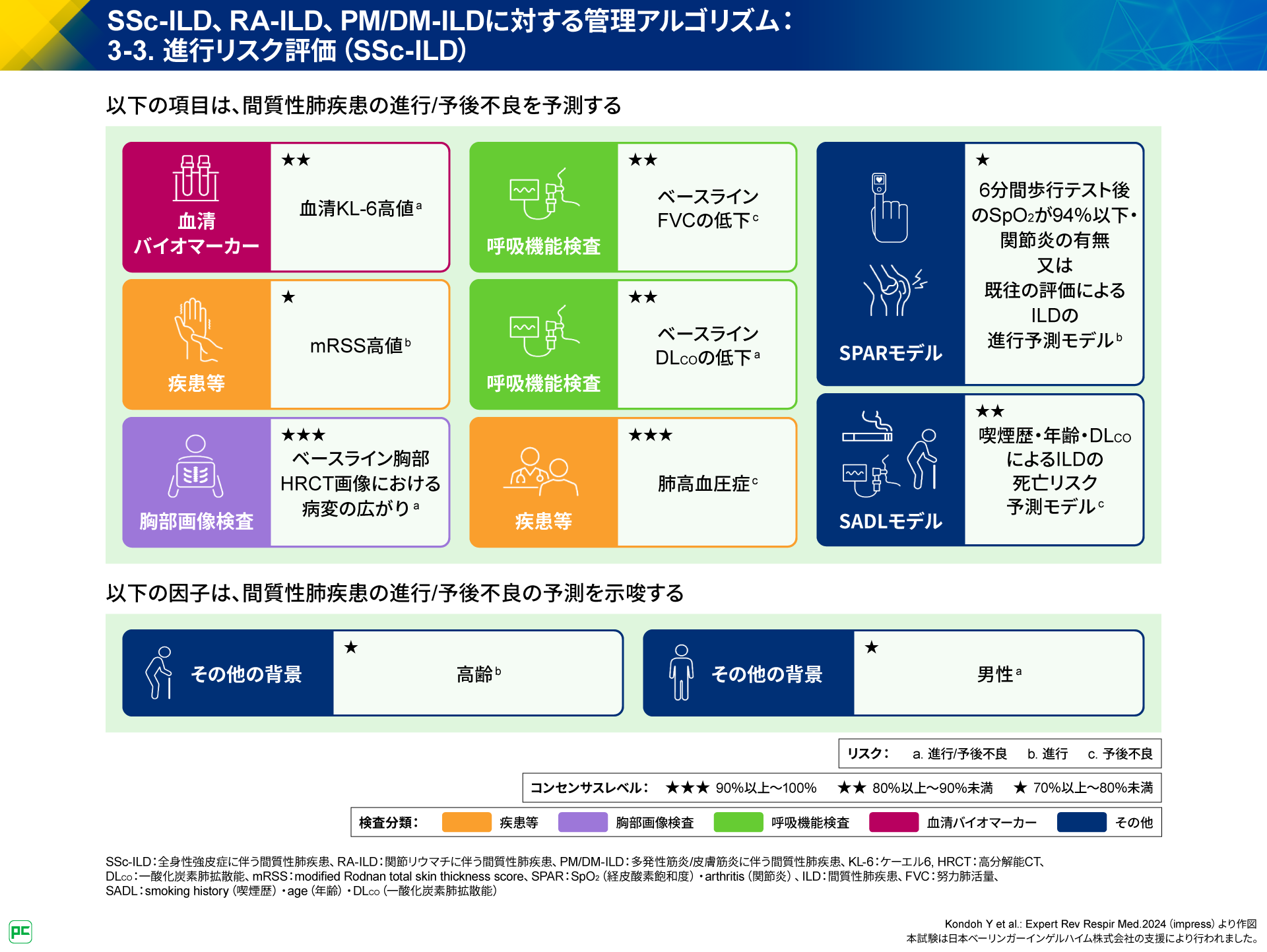
PM/DM-ILDでは、臨床的に筋症状を欠く皮膚筋炎、血清フェリチン高値、抗MDA5抗体陽性がILDの急性進行を予測する因子として提示されています(図9)。
また、ILDの予後不良のリスクを高める因子として、高齢(60歳以上)、SpO2の低下(<95%)、血清CRPの上昇(≧1.0mg/dL)、血清フェリチン高値(≧500ng/dL)、血清KL-6高値(≧1000U/mL)、DMの場合の抗MDA‐5抗体陽性が提示されています(図9)。
SpO2:経皮酸素飽和度
CRP:C反応性蛋白
図9
① SSc-ILD、RA-ILD、慢性PM/DM-ILD
ここからは、①SSc-ILD、RA-ILD、慢性PM/DM-ILDと②急性/亜急性PM/DM-ILDに分けてアルゴリズムをみていきましょう。
4a. フォローアップとモニタリング
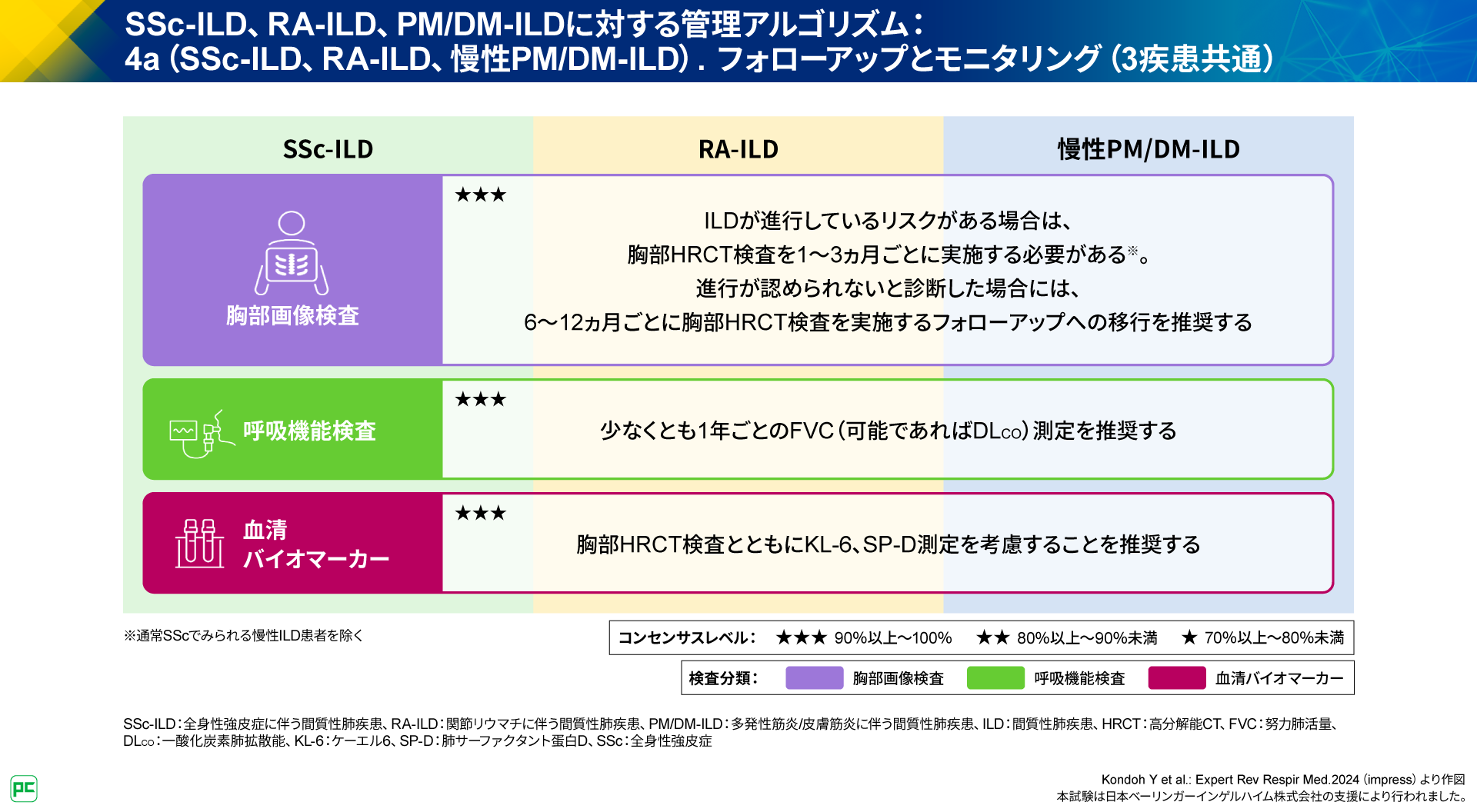
SSc-ILD、RA-ILD、慢性PM/DM-ILDに共通して、胸部画像検査と呼吸機能検査、血清バイオマーカーの測定に関する推奨事項が記載されています。
胸部画像検査については、「ILDが進行しているリスクがある場合は、胸部HRCT検査を1〜3ヵ月ごとに実施する必要がある※4。進行が認められないと診断した場合に、6~12ヵ月ごとに胸部HRCT検査を実施するフォローアップへの移行を推奨する」と記載されています。
呼吸機能検査については、「少なくとも1年ごとのFVC(可能であればDLco)測定を推奨する」と記載されています。
血清バイオマーカーについては、「胸部HRCT検査とともにKL-6、SP-D測定を考慮することを推奨する」と記載されています(図10)。
※4 通常SScでみられる慢性ILD患者を除く
SP-D:肺サーファクタント蛋白D
図10
5a. 治療開始と治療が推奨される要因
SSc-ILD、RA-ILD、慢性PM/DM-ILDに共通する、ILDの治療開始決定に有用な項目として、呼吸器症状や健康関連QOL、胸部HRCT画像、FVC、DLco、及びKL-6の総合評価や臨床経過(疾患進行)の評価、個別のリスク・ベネフィットの評価、FVCの測定、呼吸器科医、膠原病科医、放射線科医、病理医によるMDD、重症度の評価が挙げられています(図11)。
QOL:生活の質
図11

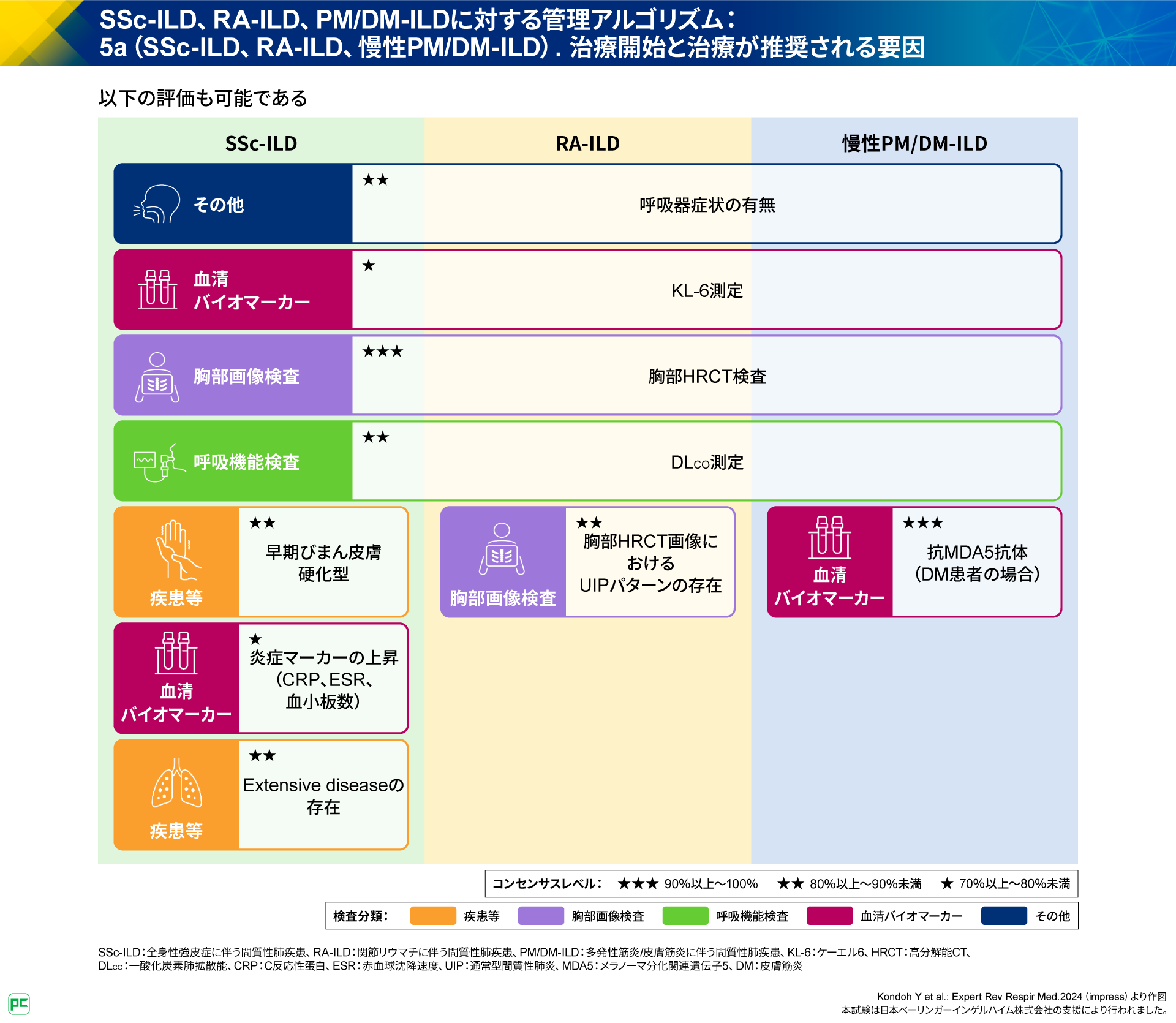
さらに、SSc-ILD、RA-ILD、慢性PM/DM-ILDに共通する、治療開始の評価が可能な項目として、呼吸器症状の有無の確認やKL-6の測定、胸部HRCT検査、DLcoの測定が挙げられています。
これらに加えて、SSc-ILDについては、早期びまん皮膚硬化型や、CRPやESR、血小板数といった炎症マーカーの上昇、Extensive diseaseの存在によって、RA-ILDについては、胸部HRCT画像におけるUIPパターンの存在によって、治療開始の評価が可能であると記載されています。慢性PM/DM-ILDについては、DMの場合に抗MDA-5抗体によって治療開始の評価が可能であると記載されています(図12)。
ESR:赤血球沈降速度
図12
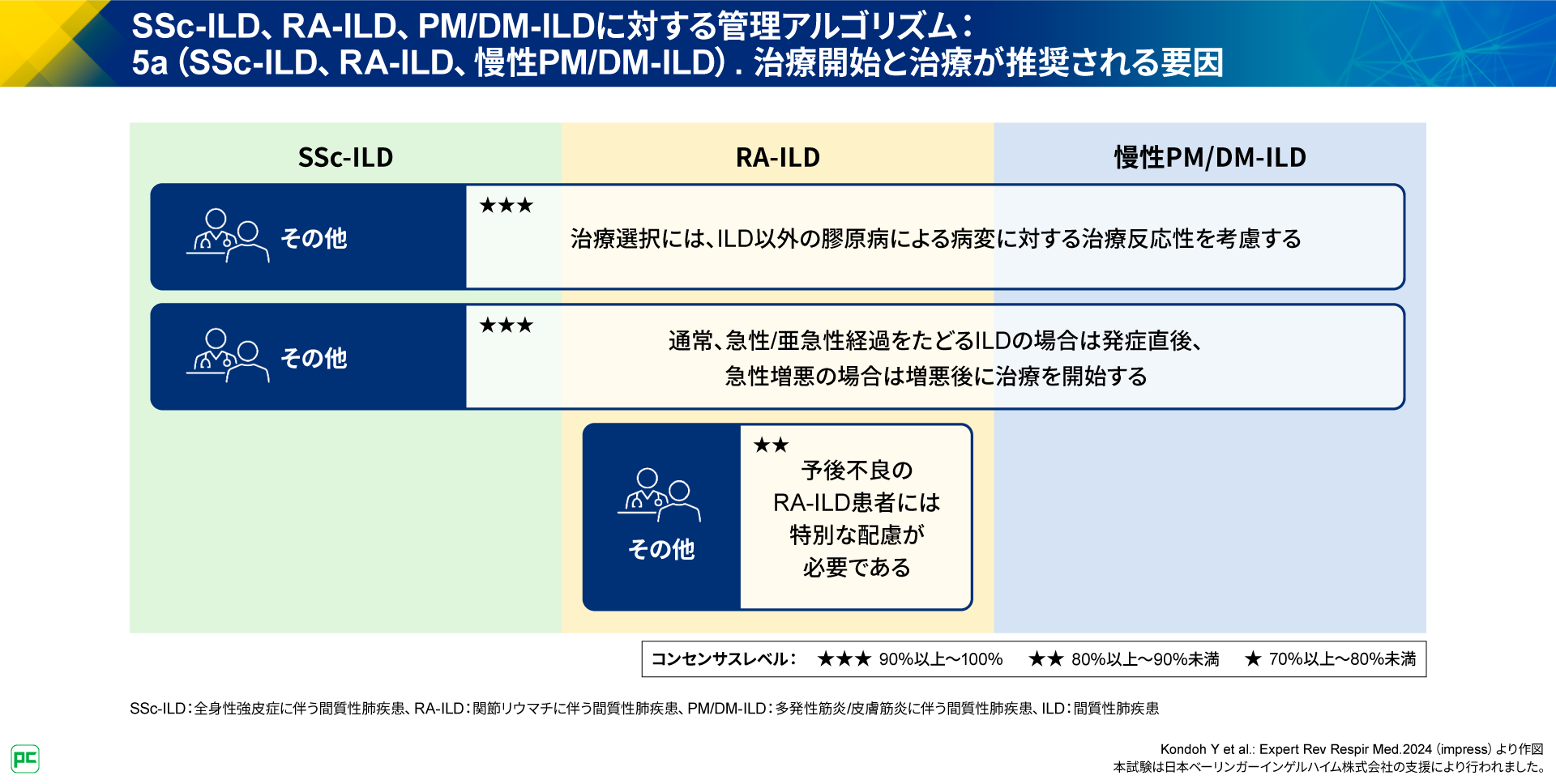
その他の治療開始と治療が推奨される要因は、図13のとおりです。
RA-ILDについては、「予後不良のRA-ILD患者には特別な配慮が必要である」こともあわせて記載されています(図13)。
図13
6a. 疾患進行
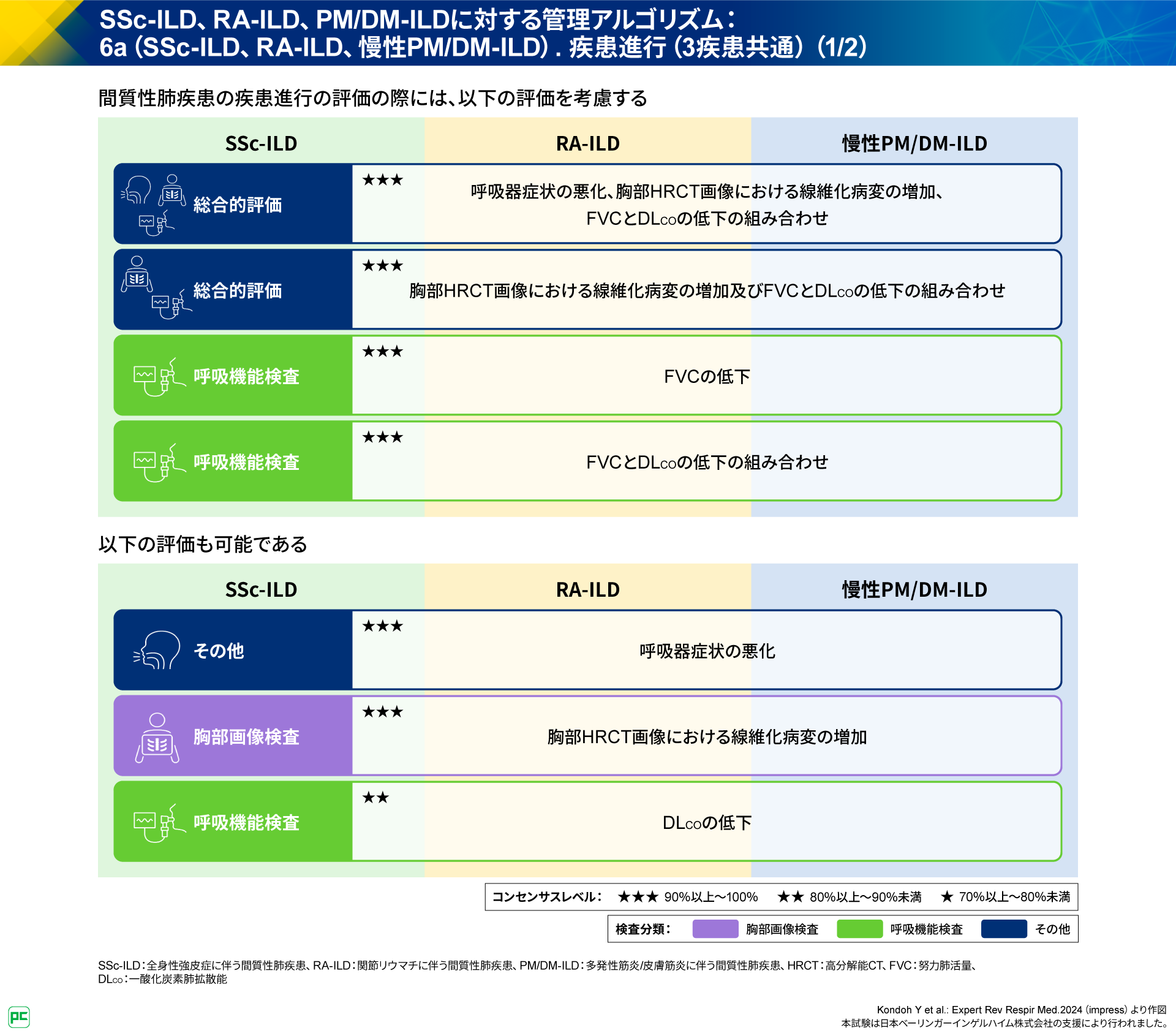
SSc-ILD、RA-ILD、慢性PM/DM-ILDに共通する、ILDの疾患進行の評価の際に考慮する項目として、「呼吸器症状の悪化、胸部HRCT画像における線維化病変の増加、FVCとDLcoの低下の組み合わせ」などのいくつかの検査を組み合わせた評価やFVCの低下が挙げられています。
また、疾患進行の評価が可能な項目として、呼吸器症状の悪化、胸部HRCT画像における線維化病変の増加、DLcoの低下が挙げられています(図14)。
図14
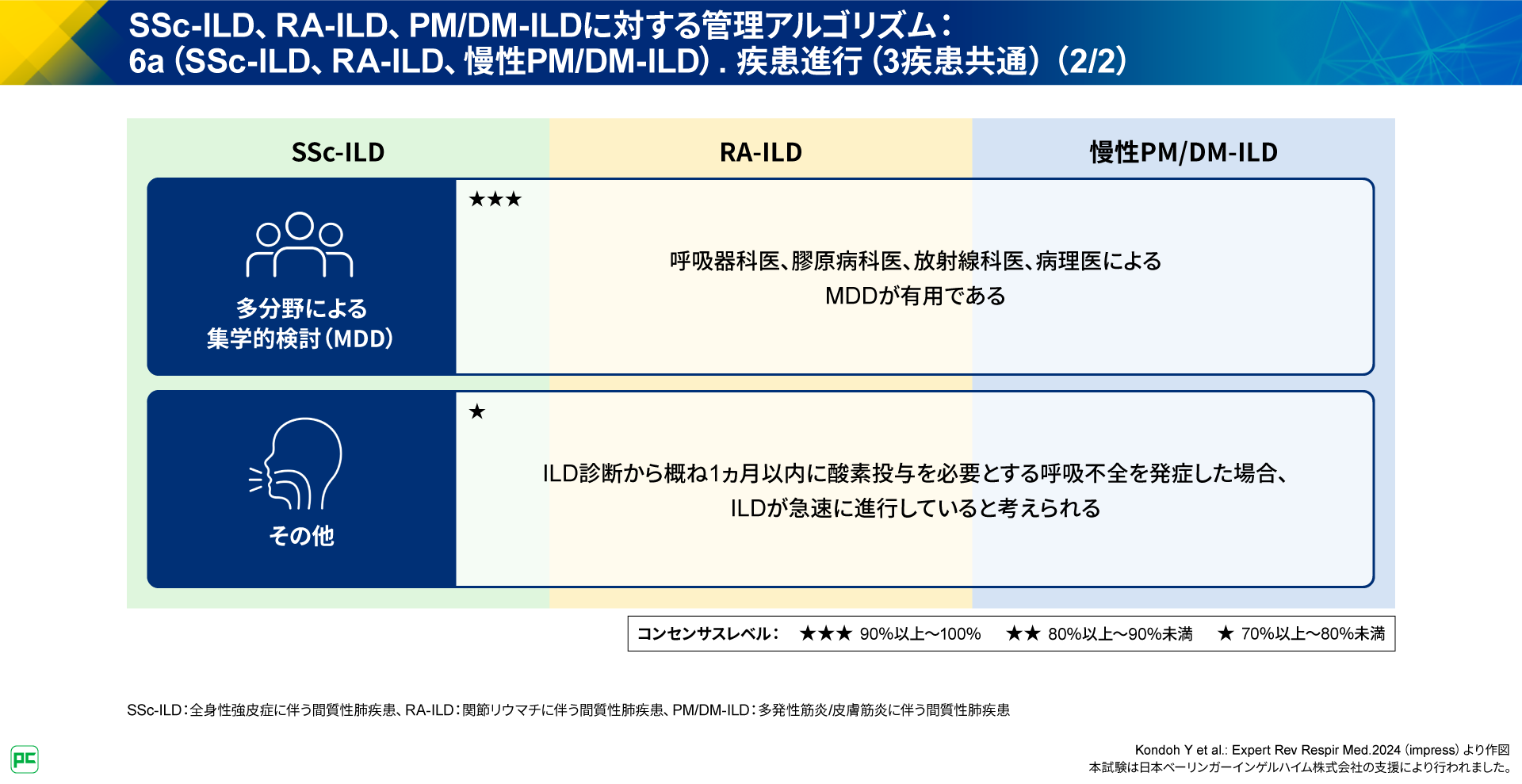
さらに、「呼吸器科医、膠原病科医、放射線科医、病理医によるMDDが有用である」こと、「ILD診断から概ね1ヵ月以内に酸素投与を必要とする呼吸不全を発症した場合、ILDが急速に進行していると考えられる」ことも記載されています(図15)。
図15
② 急性/亜急性PM/DM-ILD
4b. 治療開始と治療が推奨される要因
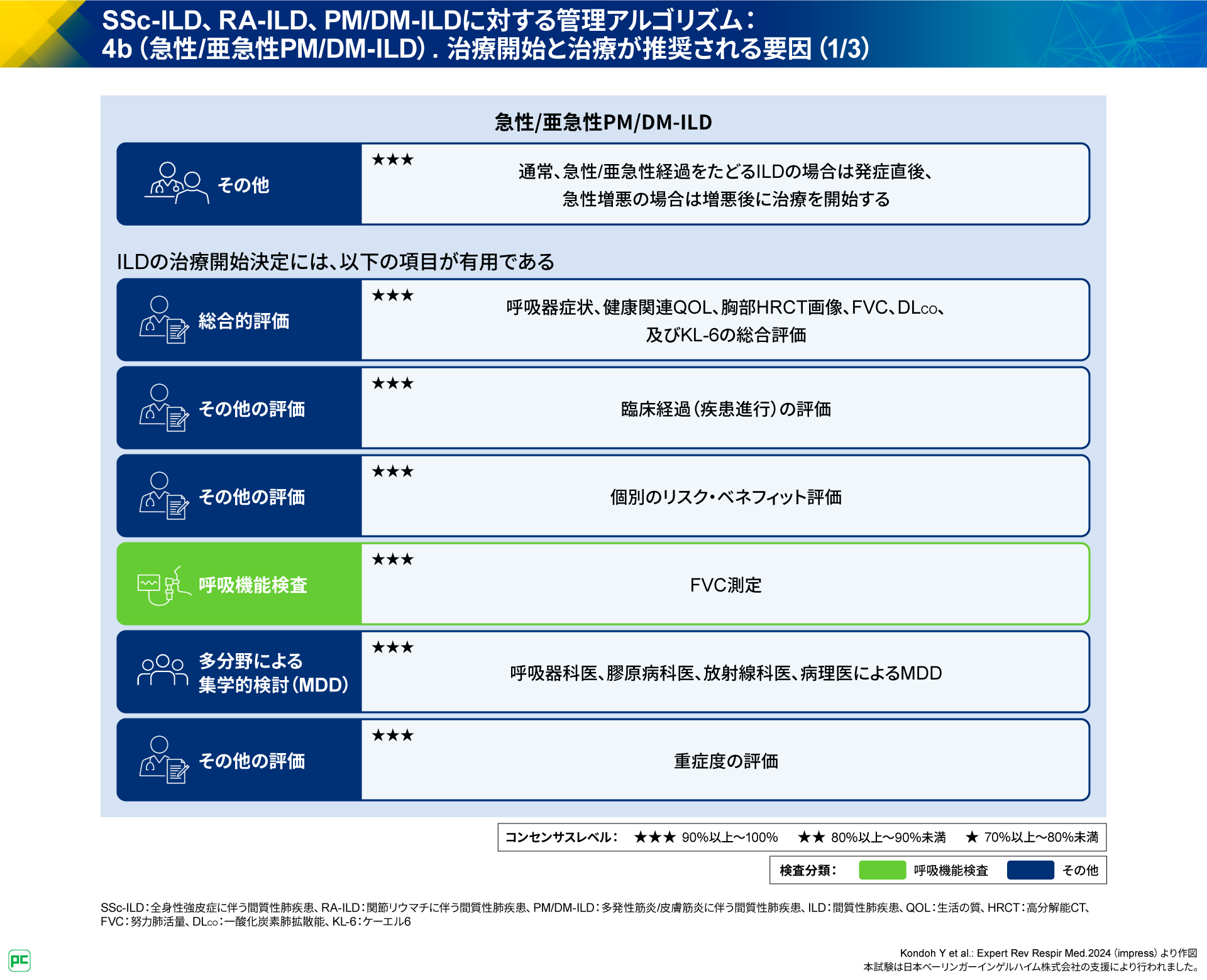
急性/亜急性PM/DM-ILDのアルゴリズムでは、冒頭に「通常、急性/亜急性経過をたどるILDの場合は発症直後、急性増悪の場合は増悪後に治療を開始する」ことが記載されています。
ILDの治療開始の決定に有用な項目として、呼吸器症状や健康関連QOL、胸部HRCT画像、FVC、DLco、及びKL-6の総合評価や、臨床経過(疾患進行)の評価、個別のリスク・ベネフィット評価、FVCの測定、呼吸器科医、膠原病科医、放射線科医、病理医によるMDD、重症度の評価が挙げられています(図16)。
図16
治療開始の評価が可能な項目については、図17のとおりです。
なお、DM患者の場合は抗MDA5抗体によっても治療開始の評価が可能と記載されています(図17)。
図17

さらに、「治療選択には、ILD以外の膠原病による病変に対する治療反応性を考慮する」と記載されています(図18)。
図18

5b. フォローアップとモニタリング
胸部画像検査と呼吸機能検査、血清バイオマーカーの測定に関する推奨事項が記載されています。
胸部画像検査については、「急性/亜急性経過をたどるILDの場合は(特に抗MDA5抗体陽性DM患者)、数日から1ヵ月ごとの胸部X線検査及び胸部HRCT検査の実施を推奨する」「ILDが進行しているリスクがある場合は、胸部HRCT検査を1〜3ヵ月ごとに実施する必要がある。進行が認められないと診断した場合に、6~12ヵ月ごとに胸部HRCT検査を実施するフォローアップへの移行を推奨する」と記載されています。
呼吸機能検査については、「少なくとも1年ごとのFVC(可能であればDLco)測定を推奨する」と記載されています。
血清バイオマーカーについては、「胸部HRCT検査とともにKL-6、SP-D測定を考慮することを推奨する」と記載されています(図19)。
図19

6b. 疾患進行
疾患進行については、「ILD診断から概ね1ヵ月以内に酸素投与を必要とする呼吸不全を発症した場合、ILDが急速に進行していると考えられる」こと、「縦隔気腫の発症は、ILDの急速進行を示唆する」ことが記載されています(図20)。
図20

まとめ
CTD-ILDコンセンサスステートメント 疾患別管理アルゴリズムでは、CTD-ILDのスクリーニングや診断のための項目が網羅的にまとめられています。SSc-ILD、RA-ILD、PM/DM-ILDに共通する項目だけでなく疾患別の項目もまとめられていますので、日本国内の実臨床において活用しやすくなっているのではないでしょうか。
CTD-ILD診療の際には、ぜひ本アルゴリズムの内容を参考にしてください。
なお、本アルゴリズムの使用時の注意点として、日本のエキスパートがデルファイ法で作成した点が挙げられていることにご留意ください。
今回ご紹介した内容を、CTD-ILD患者さんのご診療にお役立ていただけますと幸いです。
【参考文献】
- Kondoh Y et al.: Expert Rev Respir Med. 2024 (impress) 本試験は日本ベーリンガーインゲルハイム株式会社の支援により行われました。
- Kuwana M et al.: Expert Rev Respir Med. 2023;17(1):71-80. 本試験は日本ベーリンガーインゲルハイム株式会社の支援により行われました。
- Dalkey N and Helmer O.: Management science 1963;9(3): 458-467.
この記事はお役に立ちましたか?
その他の関連情報

日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。


