
数字で見る、慢性心不全治療 第1回(静止画)
サイトへ公開:2024年06月27日 (木)
クイックリンク
心不全患者におけるCKD割合

先生は、このような腎機能が低下している患者さんに対する今後の心不全治療をどのようにお考えになりますか?
この患者さんのeGFRは43.8mL/min/1.73m2です。心不全患者において、eGFR<60mL/min/1.73m2の割合はどれくらいだと思われますか?
心不全患者におけるeGFR<60mL/min/1.73m2の割合は・・・
↓
71.2%
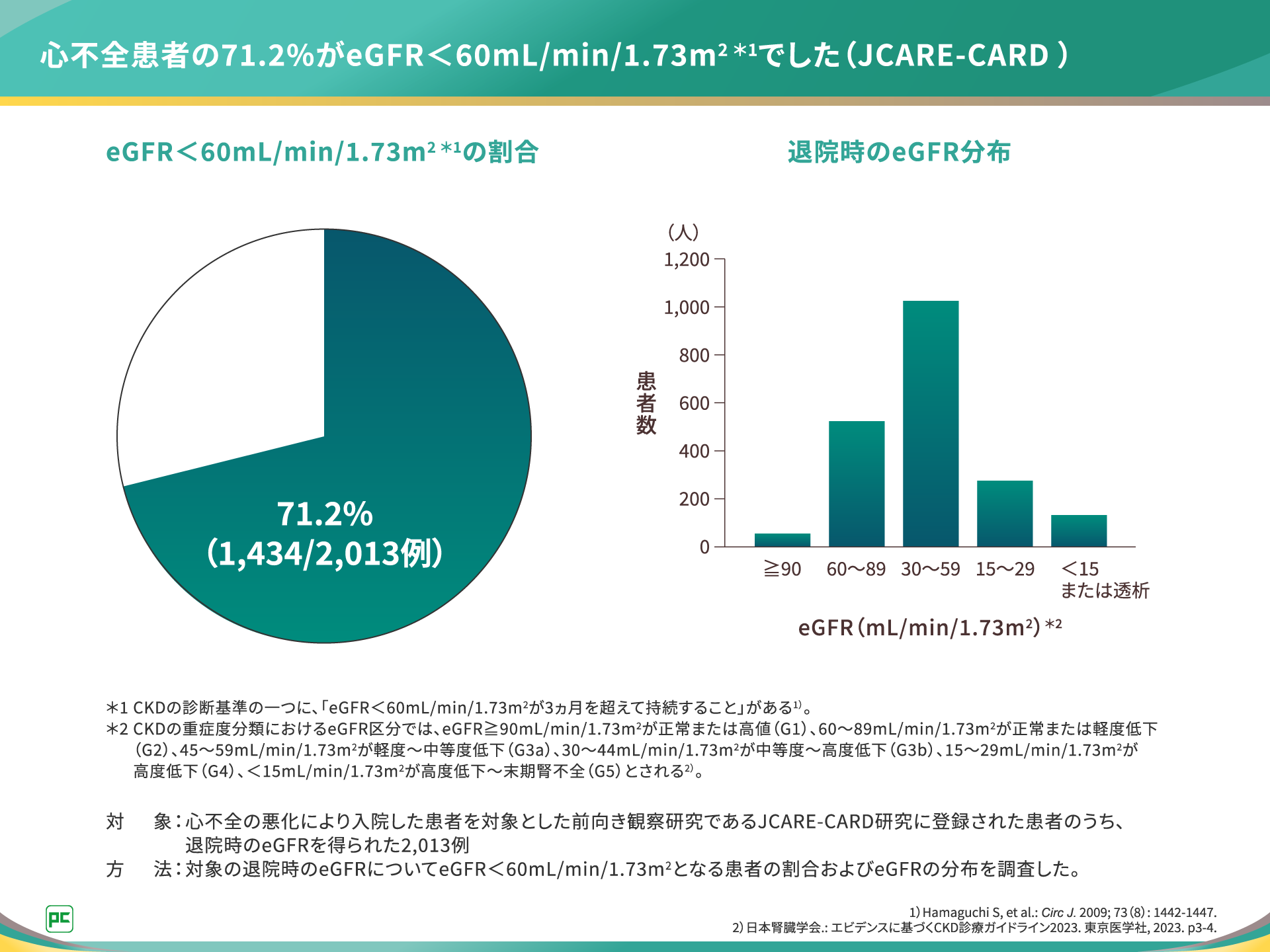
本邦の前向き観察研究JCARE-CARD研究では、心不全の悪化により入院した患者の71.2%が退院時にeGFR<60mL/min/1.73m2でした1)。
今回は、このような腎機能低下がみられる心不全患者のリスクと心腎連関の重要性についてご紹介します。

心不全患者における腎機能低下のリスク
腎機能低下が心不全患者の予後に悪影響を及ぼす危険因子であることは、過去の多くの疫学研究から示唆されています1-5)。
心不全患者を対象としたJCARE-CARD研究では、対象の71.2%がeGFR<60mL/min/1.73m2であり、退院時のeGFR分布のピークは30~59mL/min/1.73m2の範囲にありました(図1)。
図1
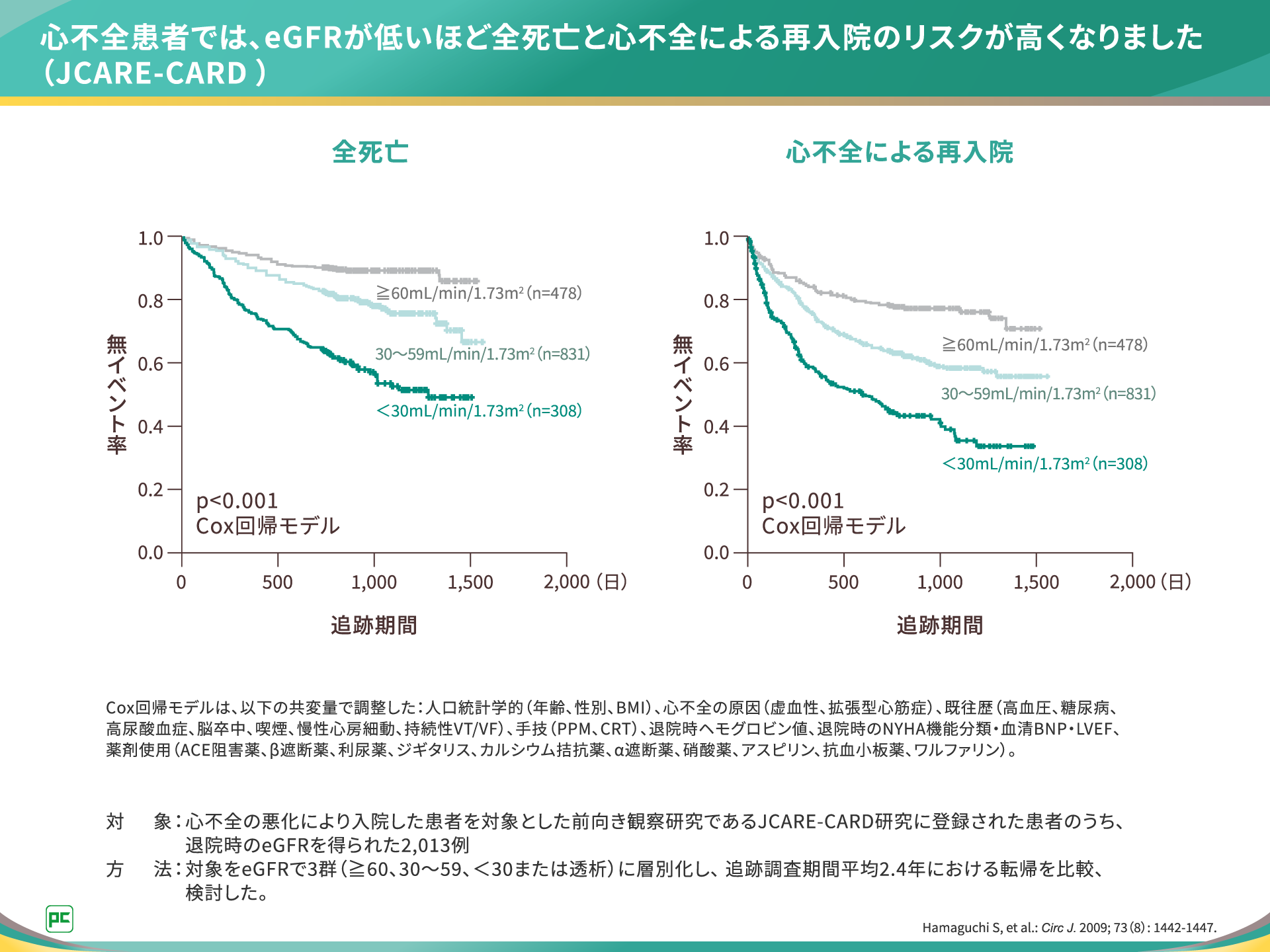
本研究では、eGFRが低いほど全死亡および心不全による再入院のリスクが高かったことが報告され、eGFR別の生存曲線はそれぞれご覧のとおりでした(図2)。
図2
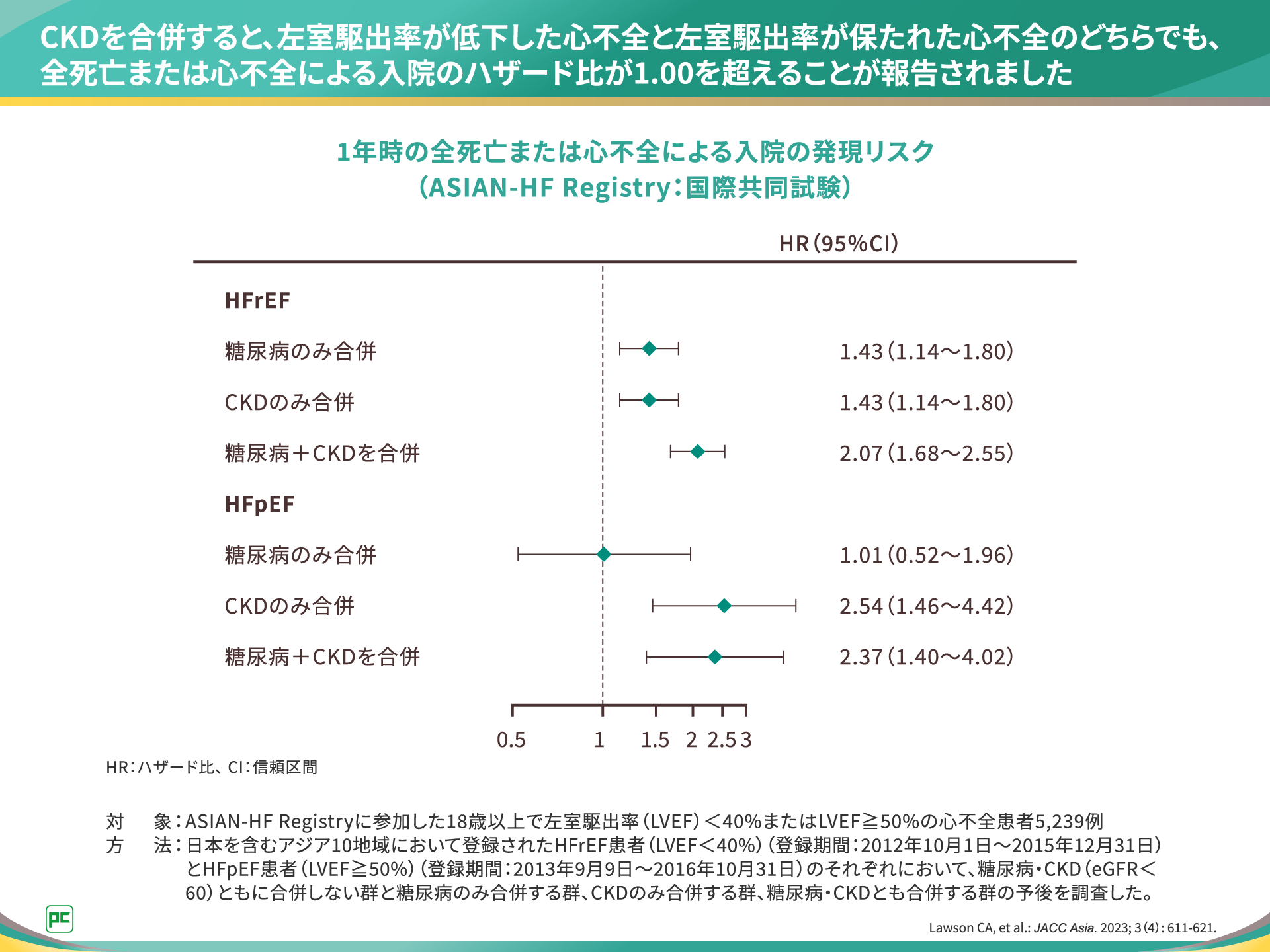
こうした腎機能低下によるリスクは、左室駆出率の低下の有無にかかわらずみられる可能性が示唆されています。
ASIAN-HF Registryに参加した心不全患者を対象とした調査では、HFrEFおよびHFpEFのどちらにおいても全死亡または心不全による入院のハザード比が1.00を超えることが報告されました(図3)。
図3
心腎連関による悪循環
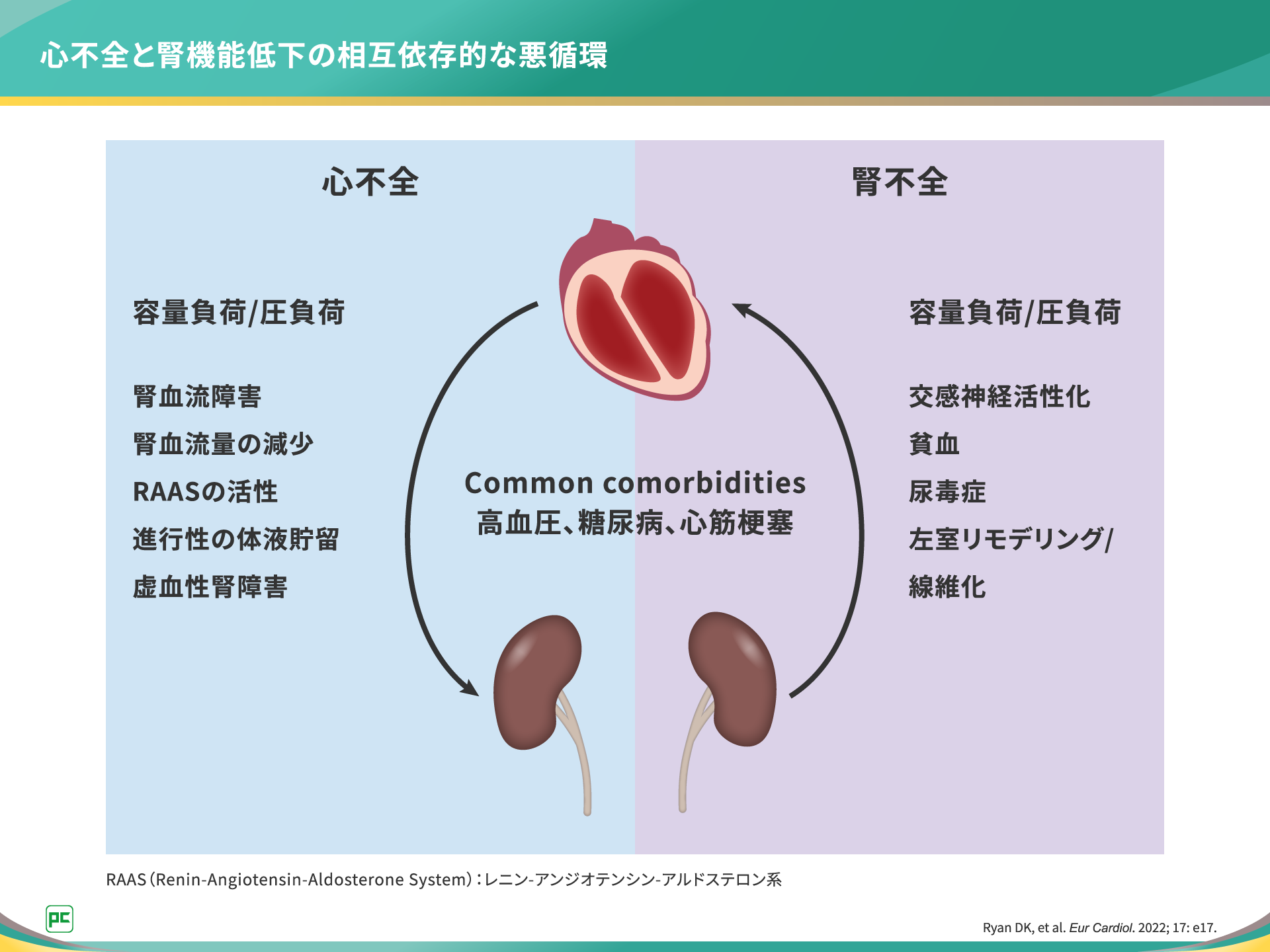
心不全患者における腎機能低下によるリスクは、各病態によって生じる生理学的作用の相互依存的な悪循環によって説明されると考えられています6)。
心不全では、腎血流量の減少や腎血流障害およびその結果として生じる虚血性腎障害によって、腎機能低下が促進されます。一方、慢性腎臓病(CKD)では、体液過剰(fluid overload)、貧血、尿毒症、レニン-アンジオテンシン-アルドステロン系(RAAS)および交感神経の活性化の結果として、左室リモデリング/線維化、心機能不全が促進されます(図4)。
図4
こうした悪循環を断ち切るためにも、心不全患者では腎機能を含めた管理が重要であると考えられます。
心腎連関を意識した心不全治療にジャディアンスという選択肢
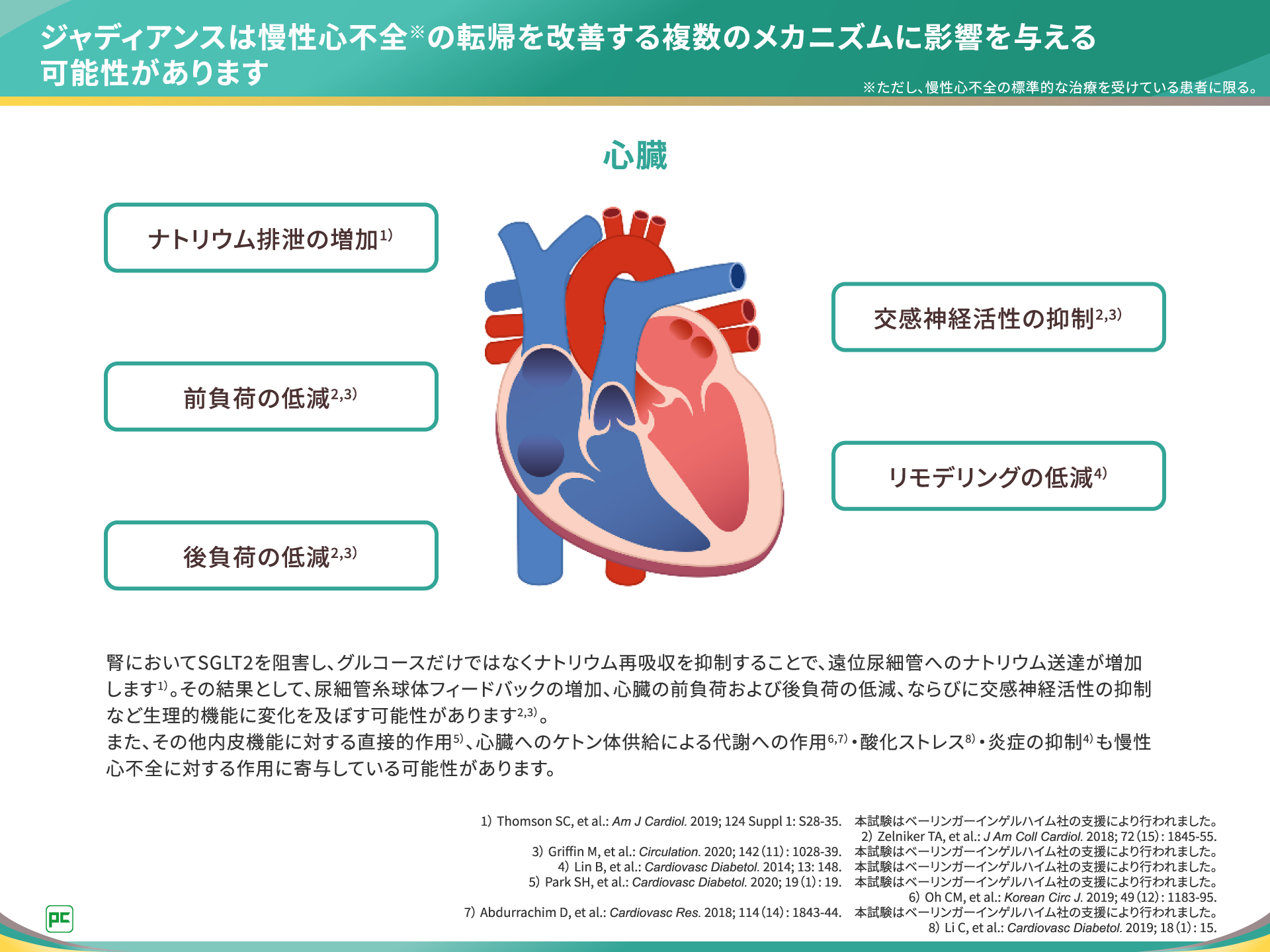
ジャディアンスは、慢性心不全※1の転帰を改善する複数のメカニズムに影響を与える可能性があります。
腎においてグルコースのみならずナトリウム再吸収を抑制することで、尿細管糸球体フィードバックの増加、心臓の前負荷および後負荷の低減、ならびに交感神経活性の抑制など生理的機能に変化を及ぼす可能性があります (図5)。
図5
また、ジャディアンス10mgは、2024年2月に慢性腎臓病※2の効能又は効果が追加承認されました。
そこで、本追加承認の根拠となったEMPA-KIDNEY試験の結果をご紹介します。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。
腎疾患進行のリスクのある慢性腎臓病患者を対象としたEMPA-KIDNEY試験
国際共同第Ⅲ相・検証試験のEMPA-KIDNEY試験では、腎疾患進行のリスクのある慢性腎臓病(CKD)患者6,581例を対象に、ジャディアンス10mgを1日1回経口投与したときの腎疾患進行または心血管死の初回発現までの期間に対する有効性および安全性をプラセボと比較検討しました(図6)。
図6
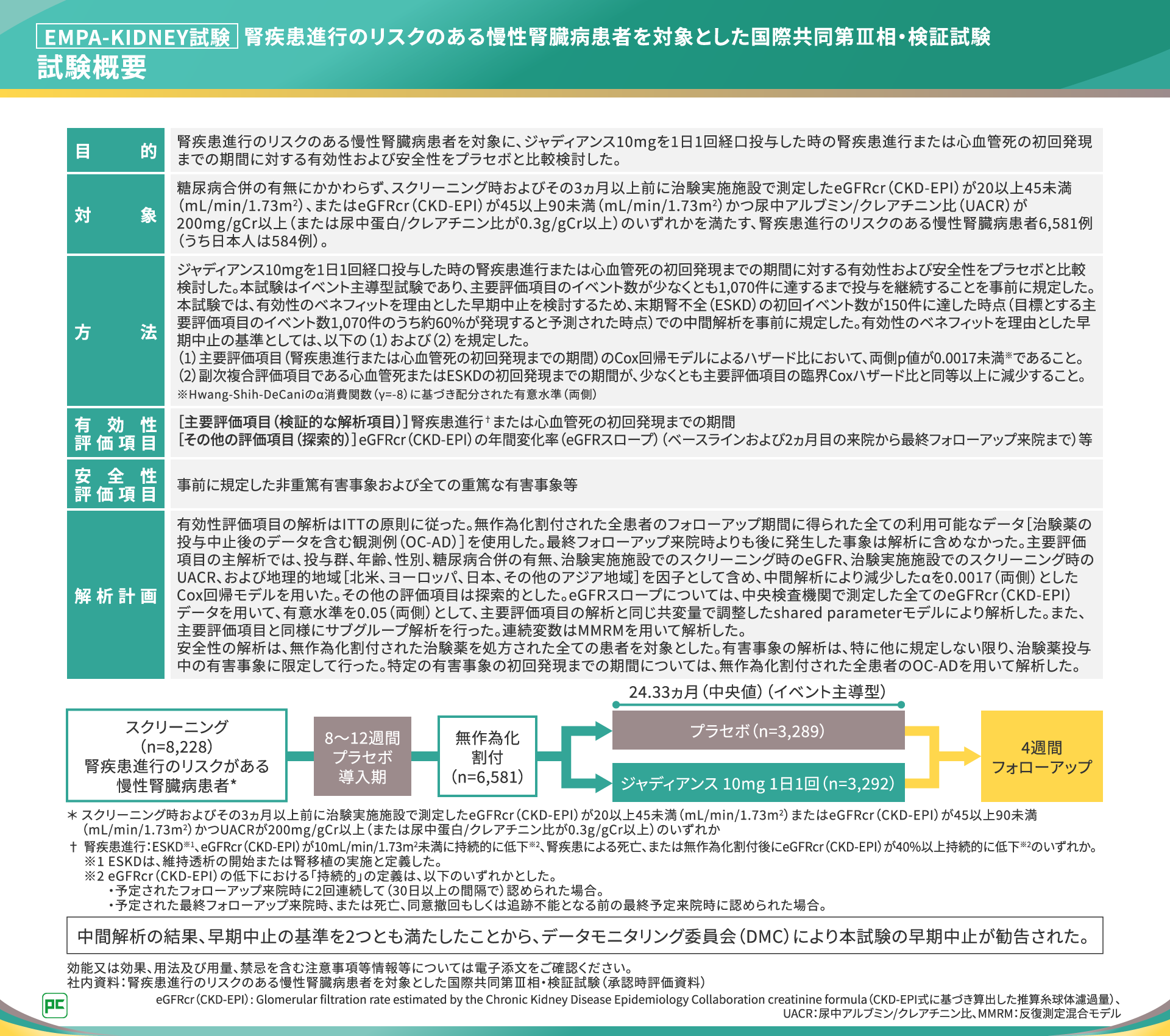
主要評価項目は腎疾患進行※3または心血管死の初回発現までの期間であり、その他の評価項目としてeGFRcr(CKD-EPI)の年間変化率(eGFRスロープ)が評価されました。
なお、本試験は、有効性の中間解析の結果、事前に規定した2つの早期中止の基準をいずれも満たし、早期中止となりました。
※3 腎疾患進行:ESKD*1、eGFRcr(CKD-EPI)が10mL/min/1.73m2未満に持続的に低下*2、腎疾患による死亡、または無作為化割付後にeGFRcr(CKD-EPI)が40%以上持続的に低下*2のいずれか。
*1 ESKDは、維持透析の開始または腎移植の実施と定義した。
*2 eGFRcr(CKD-EPI)の低下における「持続的」の定義は、以下のいずれかとした。
・予定されたフォローアップ来院時に2回連続して(30日以上の間隔で)認められた場合。
・予定された最終フォローアップ来院時、または死亡、同意撤回もしくは追跡不能となる前の最終予定来院時に認められた場合。
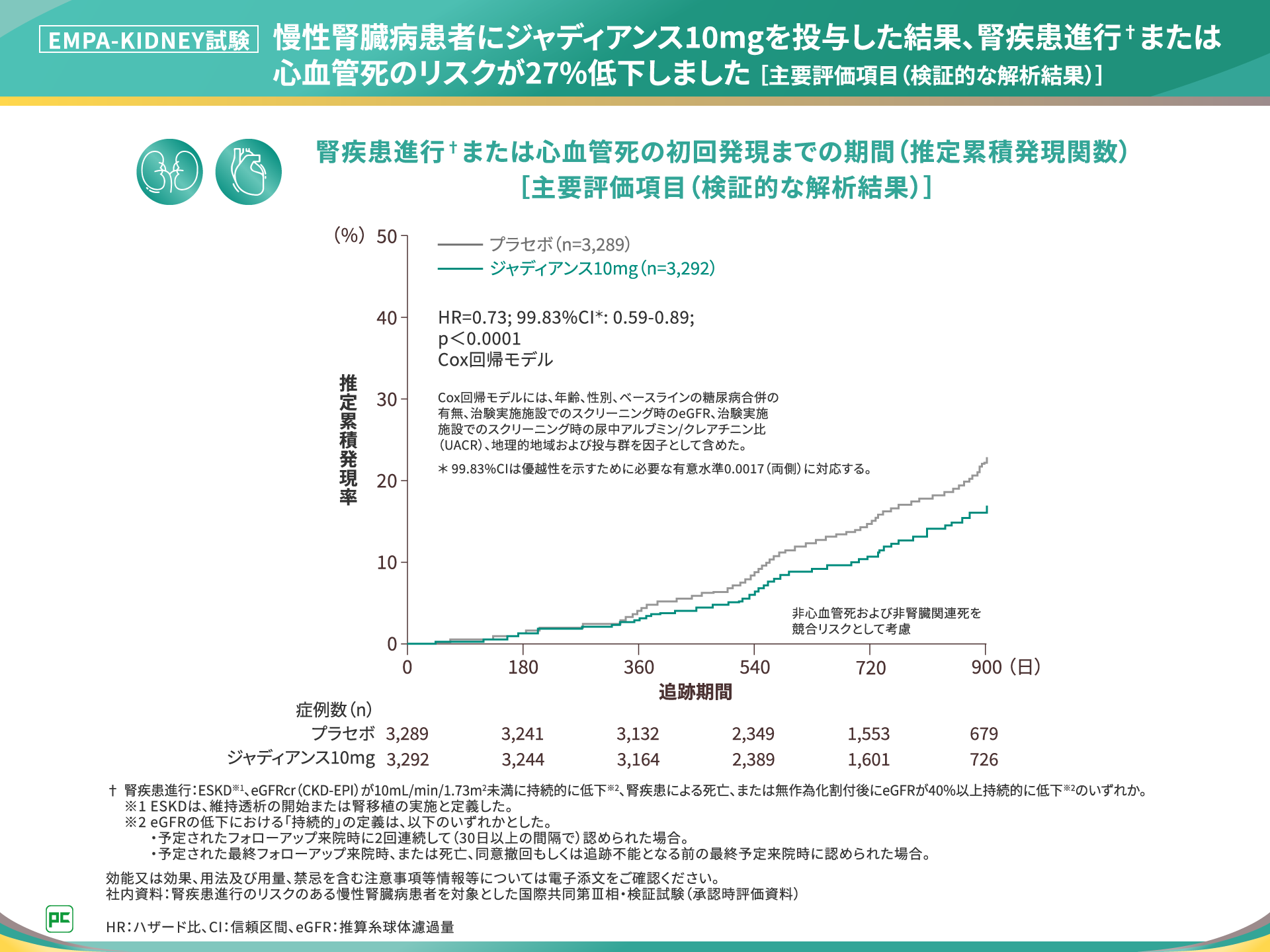
本試験の結果、主要評価項目である腎疾患進行または心血管死のリスクは、ジャディアンス10mg群で27%低下し、プラセボ群に対するジャディアンス10mg群の優越性が検証されました(HR=0.73; 99.83%CI: 0.59-0.89;p<0.0001、Cox回帰モデル)(図7)。
図7
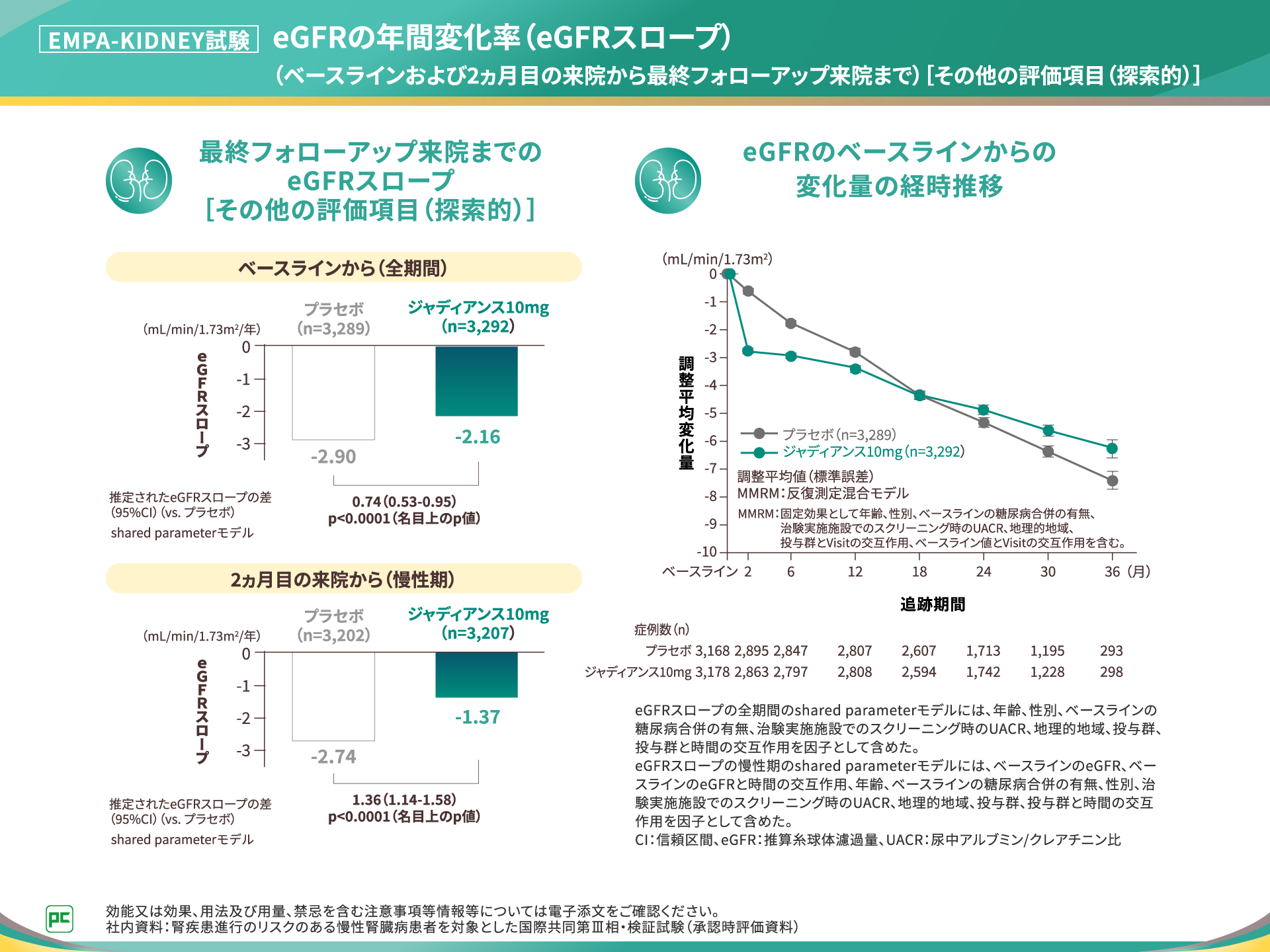
その他の評価項目であるベースラインから最終フォローアップ来院までの全期間のeGFRスロープはジャディアンス10mg群で-2.16、プラセボ群で-2.90、2ヵ月目の来院から最終フォローアップ来院までの慢性期のeGFRスロープはジャディアンス10mg群で-1.37、プラセボ群で-2.74でした。また、eGFRのベースラインからの変化量の経時推移はご覧のとおりでした(図8)。
図8
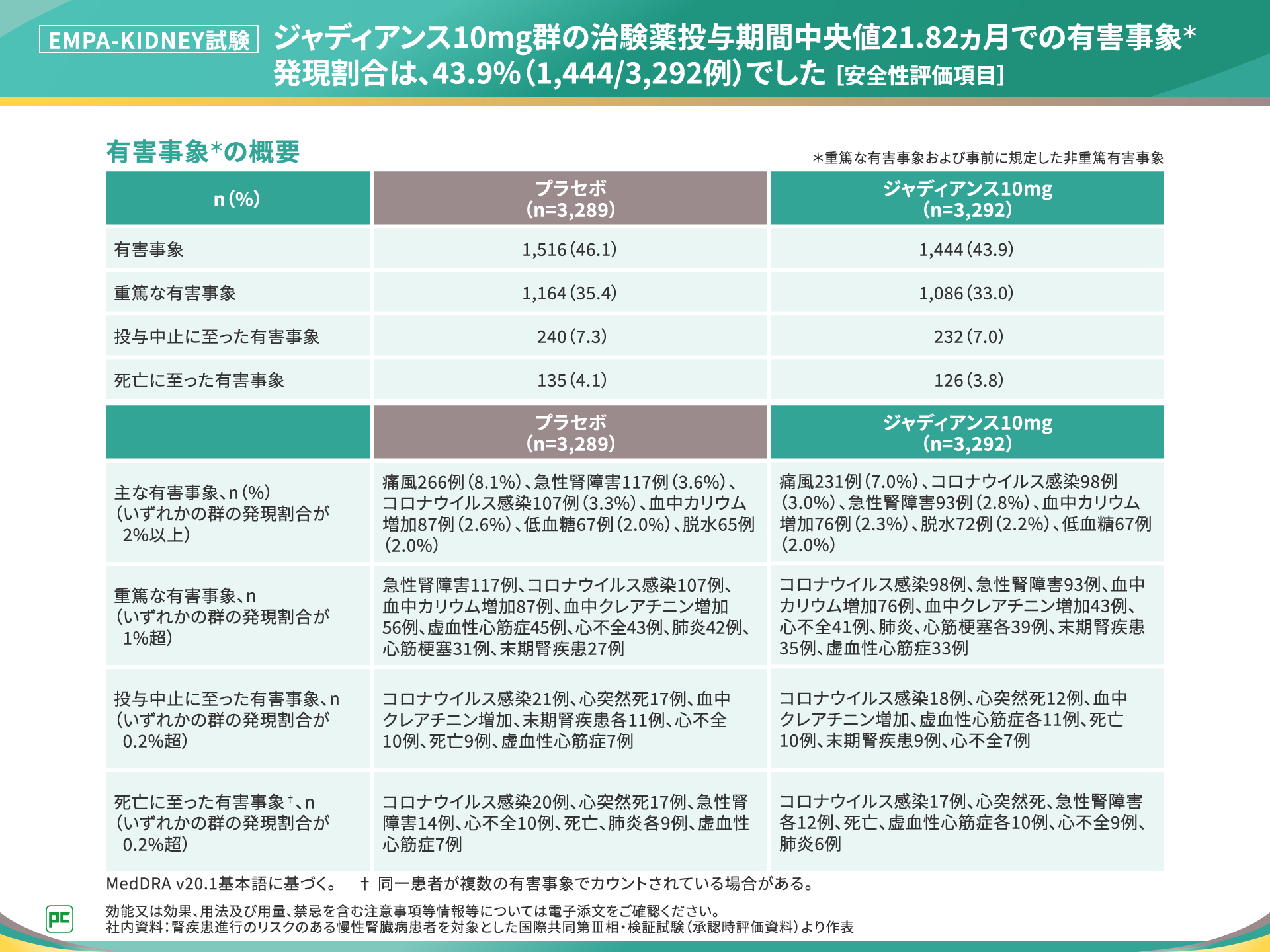
本試験における治験薬投与期間中央値21.82ヵ月での有害事象発現割合は、ジャディアンス10mg群43.9%、プラセボ群46.1%でした。ジャディアンス10mg群で発現割合が2%以上の有害事象は、痛風7.0%、コロナウイルス感染3.0%、急性腎障害2.8%などでした。
ジャディアンス10mg群では重篤な有害事象が33.0%、投与中止に至った有害事象が7.0%、死亡に至った有害事象が3.8%に認められ、各内訳はご覧のとおりでした(図9)。
図9
【参考情報】CKD患者の体液量に対するジャディアンスの影響
また、本試験の対象患者のうち、生体インピーダンス測定を実施した患者を対象に、生体インピーダンス測定値より導出した「体液過剰」および脂肪量に対するSGLT2阻害薬の影響を評価した結果をお示しします。
試験概要はご覧のとおりです(図10,11)。
図10

図11

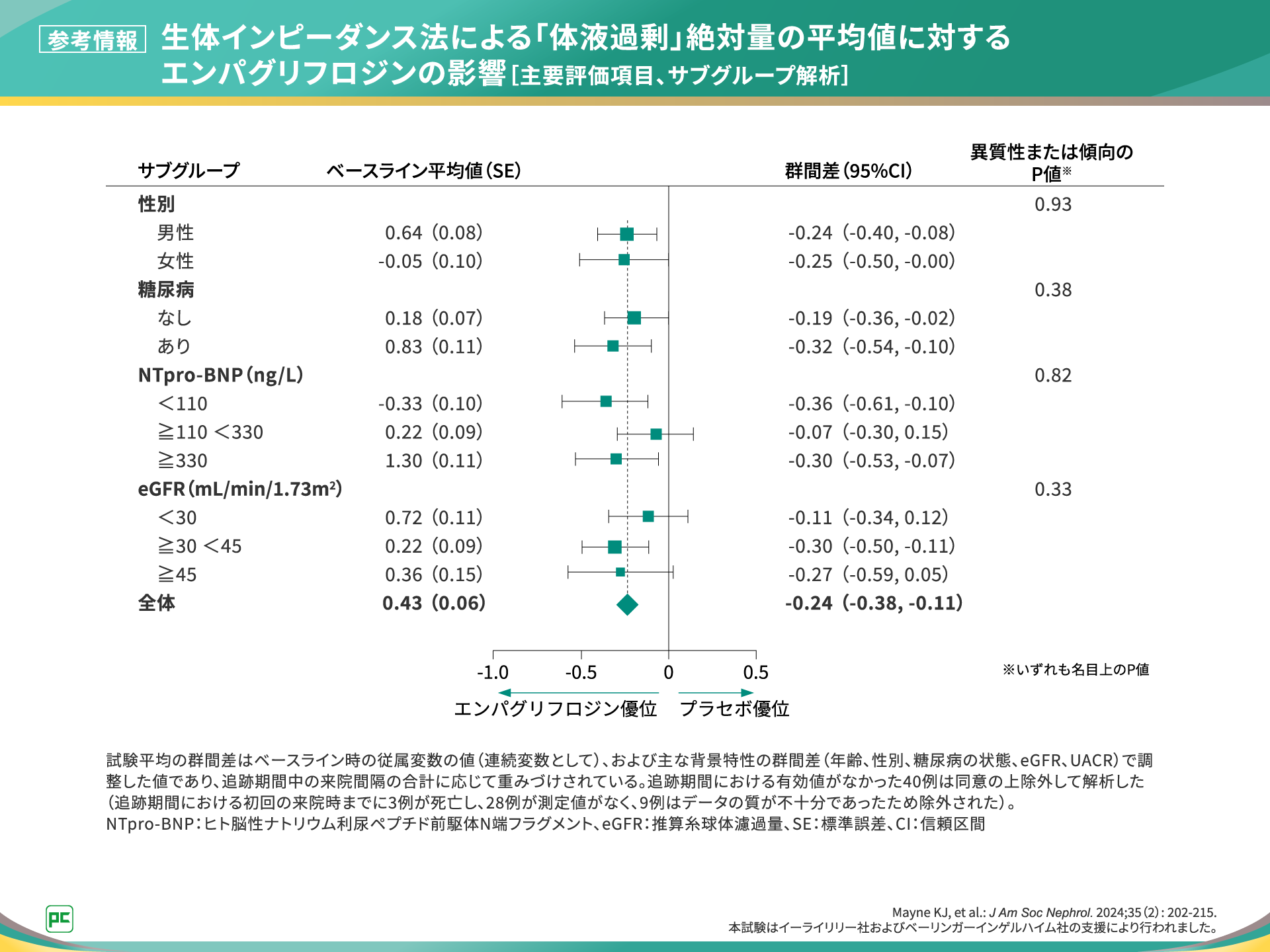
本解析の主要評価項目である生体インピーダンス法による「体液過剰」絶対量の平均値に対するジャディアンスの影響と、そのサブグループ解析はそれぞれご覧の結果でした(図12,13)。
なお、本解析では安全性に対する評価は行われませんでした。
図12
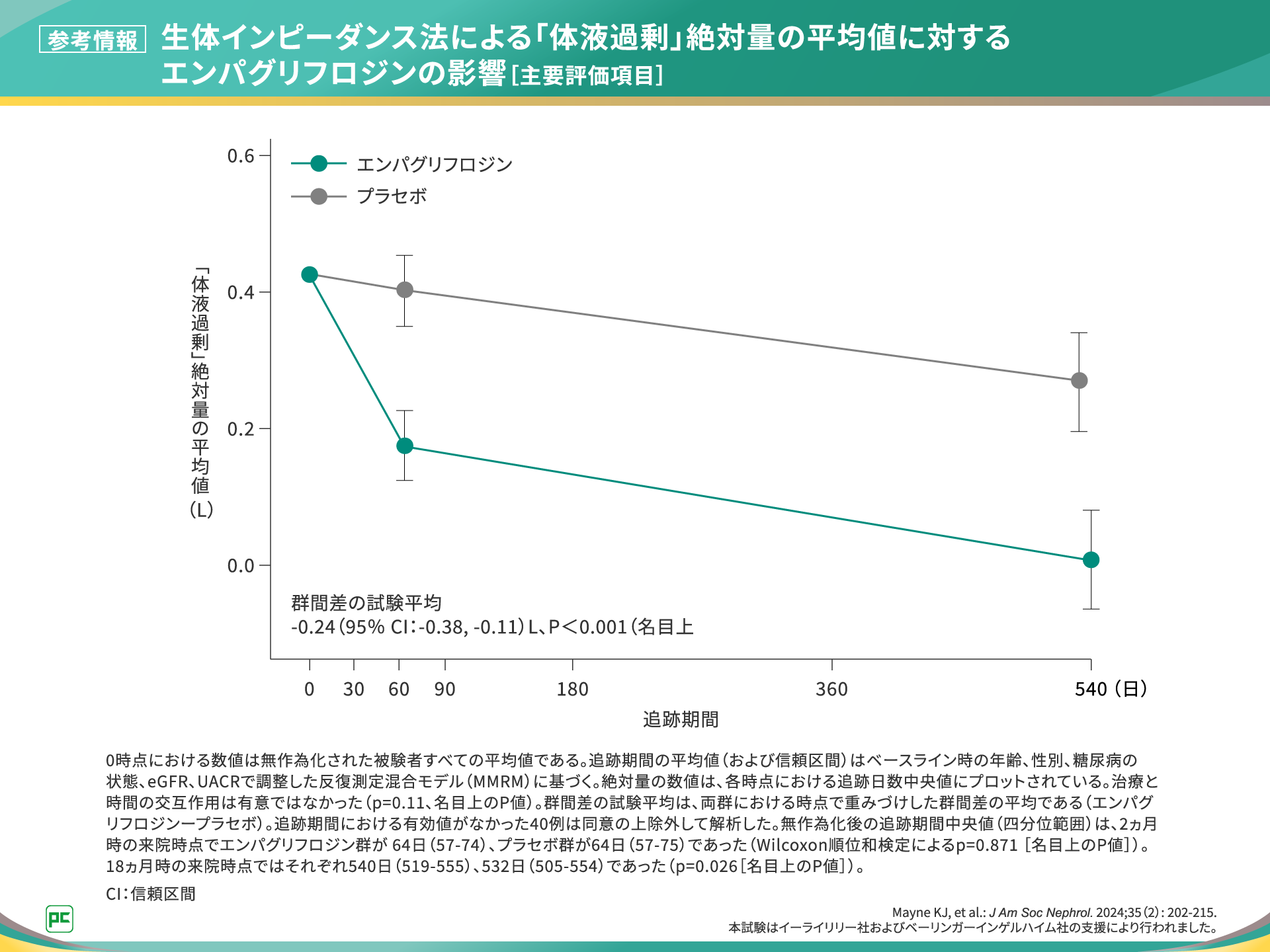
図13
腎機能を含めた管理が求められる慢性心不全※1患者の治療選択肢のひとつとして、慢性腎臓病※2の効能又は効果が追加承認されたジャディアンス錠10mgを、ぜひお役立てください。
※1 ただし、慢性心不全の標準的な治療を受けている患者に限る。
※2 ただし、末期腎不全又は透析施行中の患者を除く。
【引用】
- Hamaguchi S, et al.: Circ J. 2009; 73(8): 1442-1447.
- Hillege HL, et al.: Circulation. 2000; 102(2): 203-210.
- McAlister FA, et al.: Circulation. 2004; 109(8): 1004-1009.
- Go AS, et al.: Circulation. 2006; 113(23): 2713-2723.
- Ahmed A, et al.: Am J Cardiol. 2007; 99(3): 393-398.
- Ryan DK, et al. Eur Cardiol. 2022; 17: e17.
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。


